17.2: Las tasas de reacción suelen cambiar con el tiempo
- Page ID
- 70627
Asegúrese de comprender a fondo las siguientes ideas esenciales que se han presentado anteriormente. Es especialmente imortante que conozcas los significados precisos de todos los términos resaltados en verde en el contexto de este tema.
- Describir los roles contrastantes de la termodinámica y la cinética en la comprensión del cambio químico.
- Dada una ecuación neta equilibrada, escribir una expresión para la velocidad de una reacción.
- Haga un boceto de una curva que muestre cómo la velocidad instantánea de una reacción podría cambiar con el tiempo.
- Determinar el orden de una reacción de la forma A → B + C a partir de datos experimentales para las concentraciones de sus productos en tiempos sucesivos.
- Describir la velocidad inicial y los métodos de aislamiento para determinar los órdenes de los reactivos individuales en una reacción que involucra múltiples reactivos.
- Explicar la diferencia entre las leyes de tasas diferenciales e integrales.
- Dibuje una gráfica que muestre cómo la concentración de un componente ([A] o ln [A]) que sigue la cinética de primer orden cambiará con el tiempo. Indicar cómo la magnitud de la constante de velocidad afecta a esta parcela
- Definir la vida media de una reacción.
- Dada la vida media para una reacción de primer orden A → productos junto con el valor inicial de [A] o, encontrar [A] t en un momento posterior un número entero de semividas después.
- Describir las condiciones bajo las cuales una reacción puede parecer tener un orden de cero.
En esta página extendemos el concepto de leyes de tasas diferenciales introducidas en la página anterior a leyes de tasas integrales y vida media de reacción que son de gran importancia en la mayoría de las aplicaciones prácticas de la cinética.
Leyes de tarifas diferenciales e integrales
Medir tasas instantáneas como hemos descrito en la página anterior de esta unidad es la forma más directa de determinar la ley de velocidad de una reacción, pero no siempre es conveniente, y puede que ni siquiera sea posible hacerlo con ninguna precisión.
- Si la reacción es muy rápida, su velocidad puede cambiar más rápidamente que el tiempo requerido para medirla; la reacción puede terminar incluso antes de que se pueda observar una velocidad inicial.
- En el caso de reacciones muy lentas, los cambios observables en las concentraciones ocurren tan lentamente que la observación de una tasa verdaderamente “instantánea” se vuelve poco práctica.
La ley de tasa ordinaria (más precisamente conocida como la ley de tasa instantánea o diferencial) nos dice cómo la velocidad de una reacción depende de las concentraciones de los reactivos. Pero para muchos propósitos prácticos, es más importante saber cómo cambian con el tiempo las concentraciones de reactivos (y de productos). Por ejemplo, si estás realizando una reacción a escala industrial, querrías saber cuánto tiempo tardará, digamos, en que 95% de los reactivos se conviertan en productos.
Este es el propósito de una ley de tasa integrada.
Integrando la ley tarifaria
Esto es fácil de hacer, pero sólo algunos cursos esperan que sepas cómo hacerlo. Para una revisión rápida, haga clic aquí. Si has tenido incluso un poco de cálculo, ¡aquí tienes la oportunidad de ponerlo en uso!
Expresar la “velocidad” de una reacción: la vida media
¿Cuánto tiempo tarda una reacción química en ocurrir bajo un determinado conjunto de condiciones? Al igual que con muchas preguntas “simples”, no se puede dar una respuesta significativa sin ser más precisos. En este caso,
¿Cómo definimos el punto en el que se “completa” la reacción?
Una reacción se “completa” cuando ha alcanzado el equilibrio, es decir, cuando las concentraciones de los reactivos y productos ya no cambian. Si la constante de equilibrio es bastante grande, entonces la respuesta se reduce a una forma más simple: la reacción se completa cuando la concentración de un reactivo cae a cero. En aras de la simplicidad, asumiremos que este es el caso en lo que resta de esta discusión.
“¿Cuánto tiempo?” puede ser demasiado largo
Si la reacción tiene lugar muy lentamente, el tiempo que tarda en desaparecer cada última molécula reaccionante puede ser demasiado largo para que la respuesta sea práctica. En este caso, podría tener más sentido definir “completado” cuando la concentración de un reactivo ha caído a alguna fracción arbitraria de su valor inicial —90%, 70%, o incluso solo 20%.
La fracción particular que se selecciona depende del costo de los reactivos en relación con el valor de los productos, equilibrado con el costo de operar el proceso por un tiempo más largo o el inconveniente de esperar más producto. Este tipo de consideraciones es especialmente importante en los procesos industriales en los que los saldos de estos costos afectan la rentabilidad de la operación.
La vida media de una reacción
En lugar de tratar de identificar el tiempo requerido para que la reacción se complete, es mucho más práctico especificar el tiempo requerido para que la concentración de un reactivo caiga a la mitad de su valor inicial. Esto se conoce como la vida media (o medio tiempo) de la reacción.
Reacciones de primer orden
La ley del cambio exponencial
La velocidad a la que se consume un reactivo en un proceso de primer orden es proporcional a su concentración en ese momento. Esta relación general, en la que una cantidad cambia a un ritmo que depende de su valor instantáneo, se dice que sigue una ley exponencial.
Las relaciones exponenciales están muy extendidas en la ciencia y en muchos otros campos. El consumo de un reactivo químico o la desintegración de un isótopo radiactivo siguen la ley de desintegración exponencial. Su inversa, la ley del crecimiento exponencial, describe la manera en que el dinero en una cuenta bancaria continuamente compuesta crece con el tiempo, o el crecimiento poblacional de una colonia de organismos reproductores.
La razón por la que la función exponencial y=e x describe de manera tan eficiente tales cambios deriva de la notable propiedad de que dy/dx = e x; es decir, e x es su propia derivada, por lo que la tasa de cambio de y es idéntico a su valor en cualquier punto. Una buena discusión de esta propiedad se puede encontrar aquí.
La ley de tarifas integradas de primer orden
La ley de tarifas integradas para una reacción de primer orden
A → productos
es un ejemplo común de la ley del cambio exponencial. Para un reactivo A, su concentración [A] t en el tiempo t viene dada por
[A] t = [A] o × e — kt
en el que [A] o es su concentración inicial y k es la constante de velocidad de primer orden.
La “e” en el término exponencial es por supuesto la base de los logaritmos naturales, y el signo negativo en su exponente significa que el valor de este término disminuye a medida que t aumenta, como esperaríamos para cualquier tipo de proceso de decaimiento.
Una forma más conveniente de la ley de tasa integrada se obtiene tomando el logaritmo natural de ambos lados:
ln [A] = — kt + ln [A] o (4-1)
Esto tiene la forma de una ecuación para una línea recta
y = mx + b
en el que la pendiente m corresponde a la constante de velocidad k. Esto significa que, para una reacción de primer orden, una parcela de ln [A] en función del tiempo da una línea recta con una pendiente de — k.
Vida media
Después de un periodo de una vida media, t = t ½ y podemos escribir
(en la que expresamos lo exponencial como una función para que se destaque más prominentemente.) Tomando logaritmos de ambos lados (recuerde que
ln e x = x) rinde
Resolviendo para la vida media, obtenemos la relación simple
lo que nos dice que la vida media de una reacción de primer orden es una constante. Esto significa que 100,000 moléculas de un reactivo se reducirán a 50,000 en el mismo intervalo de tiempo necesario para que diez molcules se reduzcan a cinco.
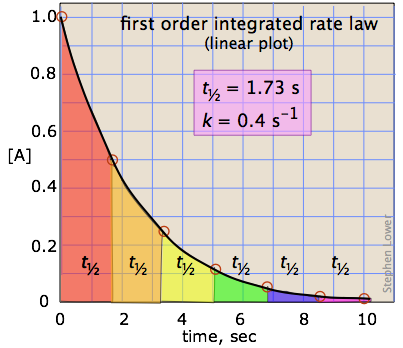
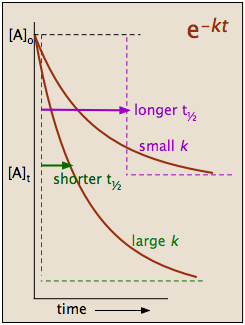
Debe quedar claro que la constante de velocidad y la semivida de un proceso de primer orden están inversamente relacionadas.
Se encontró que la vida media de una reacción de primer orden fue de 10 min a cierta temperatura. ¿Cuál es su constante de velocidad en segundos recíprocos?
Solución:
De la ecuación anterior, k = —0.693/ (600 s) = 0.00115 s —1
La desintegración de los núcleos radiactivos es siempre un proceso de primer orden.
El isótopo masa-241 del americio, ampliamente utilizado como fuente ionizante en detectores de humo, tiene una vida media de 432 años.
a) ¿Qué fracción del Am 241 en un detector de humo habrá decaído después de 50 años?
b) ¿Cuánto tiempo tardará en que la actividad disminuya al 80% de su valor inicial?
c) ¿Cuál sería la “séptima vida” de Am 241?
Solución:
a)
Reacciones de segundo orden
Integración de la ley de tasa de segundo orden
rendimientos
que se reordena fácilmente en una forma de la ecuación para una línea recta (¡intente mostrarlo usted mismo!) y rinde parcelas similares a la que se muestra a la izquierda de abajo.
La vida media viene dada por
(ver aquí para más detalles)
Observe que la vida media de una reacción de segundo orden depende de la concentración inicial, en contraste con su constancia para una reacción de primer orden. Por esta razón, el concepto de vida media para una reacción de segundo orden es mucho menos útil.
Procesos de orden cero
En algunas reacciones, la velocidad es aparentemente independiente de la concentración del reactivo, en cuyo caso
[A] t = [A] 0 — k t
tasa = k [A] 0 = k
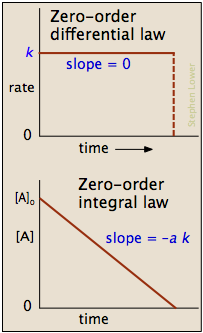
Obsérvese la palabra “aparentemente” en la frase anterior; la cinética de orden cero es siempre un artefacto de las condiciones bajo las cuales se lleva a cabo la reacción. Por esta razón, las reacciones que siguen la cinética de orden cero a menudo se denominan reacciones de orden pseudo-cero.
Claramente, un proceso de orden cero no puede continuar después de que se haya agotado un reactivo. Justo antes de que se alcance este punto, la reacción volverá a otra ley de velocidad en lugar de caer directamente a cero como se representa en la parte superior izquierda.
Hay dos condiciones generales que pueden dar lugar a tasas de orden cero:
Esta situación ocurre comúnmente cuando una reacción es catalizada por la unión a una superficie sólida (catálisis heterogénea) o a una enzima.
Por ejemplo, la descomposición del óxido nitroso
→ N 2 (g) + ½ O 2 (g)en presencia de un alambre de platino caliente (que actúa como catalizador) es de orden cero, pero sigue una cinética más convencional cuando se lleva a cabo íntegramente en fase gaseosa.
En este caso, las moléculas de N 2 O que reaccionan se limitan a las que se han adherido a la superficie del catalizador sólido. Una vez que todos los sitios en la superficie limitada del catalizador han sido ocupados, las moléculas adicionales en fase gaseosa deben esperar hasta que la descomposición de una de las moléculas adsorbidas libere un sitio superficial.
Las reacciones catalizadas por enzimas en organismos comienzan con la unión del sustrato al sitio activo de la enzima, lo que lleva a la formación de un complejo enzima-sustrato. Si el número de moléculas enzimáticas está limitado en relación con las moléculas de sustrato, entonces la reacción puede parecer de orden cero.
Esto se ve con mayor frecuencia cuando dos o más reactivos están involucrados. Así, si la reacción
A + B → productos
es de primer orden en ambos reactivos para que
tasa = k [A] [B]
entonces si B está presente en gran exceso, la reacción parecerá ser de orden cero en B (y de primer orden general). Esto ocurre comúnmente cuando B es H 2 O y la reacción se lleva a cabo en solución acuosa.
- Solo una pequeña fracción de las moléculas reaccionantes se encuentran en un lugar o estado en el que son capaces de reaccionar, y esta fracción se repone continuamente desde el charco más grande.
- Cuando están involucrados dos o más reactivos, las concentraciones de algunos son mucho mayores que las de otros
Resumen
En la siguiente tabla se comparan los parámetros de velocidad de reacciones de cero, primer y segundo orden de la forma A → productos. Consulta también esta excelente página de Purdue University que muestra tramas de [A], ln [A], y 1/ [A] para cada orden de reacción.
| orden cero | primer orden | segundo orden | |
|---|---|---|---|
| ley de tasa diferencial | tasa = k | tasa = k [A] | tasa = k [A] 2 |
| ley de tasa integrada | [A] = [A] ο = — akt |
|
|
| vida media |
|
|
|
| parcela que da línea recta | [A] vs. t | Ln [A] vs. t | 1/ [A] vs. t |
| parcela, mostrando interpretación de pendiente e intercepción |  |


