3.6: Dobles enlaces carbono-oxígeno
- Page ID
- 79147
La clase más grande de moléculas que contienen oxígeno son los compuestos de carbonilo, que contienen enlaces C=O. Un estiramiento C=O normalmente es fácil de encontrar en un espectro IR, porque es muy fuerte y aparece en una parte del espectro que no está abarrotada de otros picos. Los ejemplos de compuestos carbonílicos incluyen 2-octanona, una cetona y butanal, un aldehído. En un aldehído, el carbonilo está al final de una cadena, con un hidrógeno unido al carbono del carbonilo.
Si nos fijamos en el espectro IR de 2-octanona:
- hay modos de estiramiento sp 3 C-H y flexión CH 2 a 2900 y 1500 cm -1.
- hay un pico muy fuerte alrededor de 1700 cm -1.
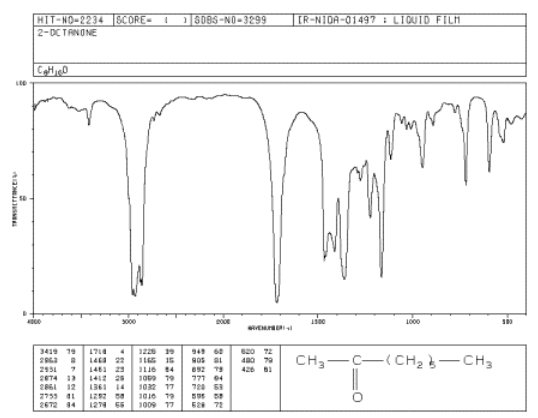
Fuente: SDBSWeb: http://riodb01.ibase.aist.go.jp/sdbs/ (Instituto Nacional de Ciencia y Tecnología Industrial Avanzada de Japón, 14 de julio de 2008)
Aunque solo hay un enlace C=O, el tramo carbonilo suele ser el pico más fuerte en el espectro. Eso hace que los compuestos carbonílicos sean fáciles de identificar mediante espectroscopia IR.
Si nos fijamos en el espectro IR del butanal:
- hay modos de estiramiento sp 3 C-H y flexión CH 2 a 2900 y 1500 cm -1.
- hay un pico C=O muy fuerte alrededor de 1700 cm -1.
- hay un par de picos medios alrededor de 2700 y 2800 cm -1. Este es el modo de estiramiento de aldehído C-H.
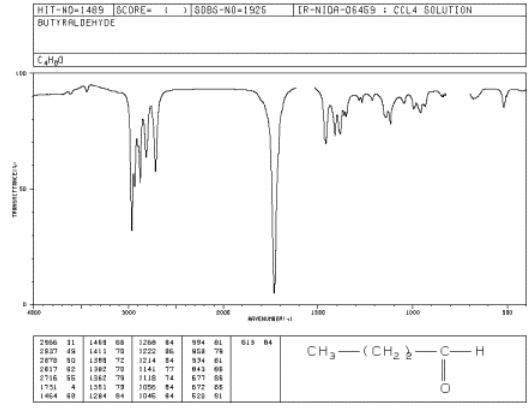
Fuente: SDBSWeb: http://riodb01.ibase.aist.go.jp/sdbs/ (Instituto Nacional de Ciencia y Tecnología Industrial Avanzada de Japón, 14 de julio de 2008)
El enlace aldehído C-H absorbe a dos frecuencias porque puede vibrar en fase con el enlace C=O (un tramo simétrico) y desfasado con el enlace C=O (un estiramiento asimétrico), y estas vibraciones son de diferentes energías. La probabilidad del estiramiento simétrico y el estiramiento asimétrico son aproximadamente iguales, por lo que los dos picos son siempre aproximadamente del mismo tamaño. Este inusual pico C-H a menudo se puede utilizar para distinguir entre un aldehído y una cetona.

