5.5: Proteínas
- Page ID
- 79175
Las estructuras proteicas pueden ser complicadas. Sus espectros de RMN pueden ser muy complicados. Por esa razón, a menudo se utilizan técnicas de RMN multidimensional para determinar las estructuras proteicas. En esta página, veremos solo algunas de las técnicas, entre ellas COSY, TOCSY y HNCA.
Tenga en cuenta que HNCA no es un ejemplo de RMN 2D. Es un ejemplo de RMN 3D. Muestra una correlación entre un protón amida, el nitrógeno amida al que está unido y los carbonos que están unidos al nitrógeno de amida. Los datos de HNCA se visualizan en rebanadas, en las que solo observamos un nitrógeno a la vez. Un eje muestra el desplazamiento del protón unido a ese nitrógeno, y el otro eje muestra los desplazamientos de los carbonos unidos al nitrógeno.
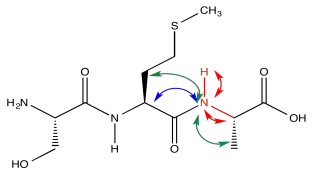
Considera un tripéptido simple.
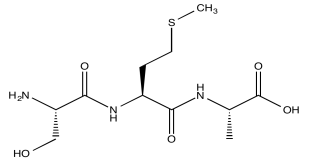
HNCA explota una transferencia de magnetización, similar al proceso utilizado en un experimento COSY o HMBC. En este caso, el experimento involucra tres tipos diferentes de núcleos. Se irradia un protón amida (H); transfiere información al nitrógeno unido (N) y luego al carbono alfa (CA).
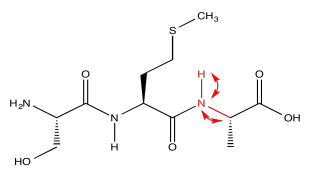
Los resultados del experimento HNCA muestran la relación entre estos tres núcleos. Hemos visto cómo se puede mostrar un experimento bidimensional, pero mostrar un experimento tridimensional requeriría un eje z. Eso podría ser difícil. En cambio, los resultados de HNCA se muestran como “rebanadas”. Un corte muestra solo los datos de 13 C y 1 H relacionados con una resonancia particular de 15 N.
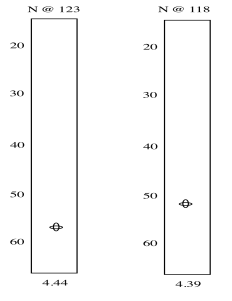
Entonces vemos que hay un nitrógeno amida que aparece a 123 ppm en el espectro de 15 N. Se une a un carbono que se muestra a 57 ppm en el espectro de 13 C y a un protón que se muestra a 4.44 ppm en el espectro de 1 H. Un segundo corte muestra resultados similares para el segundo grupo amida H-N-Cα en el tripéptido.
Los experimentos de HNCA son complicados. La forma en que se ejecuta el experimento permite obtener diferentes tipos de información, al igual que un HMBC y HMQC muestran información diferente de métodos fundamentalmente similares.
Ejecutando el HNCA de otra manera, en realidad podemos ver el carbono alfa en el otro lado del carbonilo, además del carbono alfa adyacente a la posición amida que estamos viendo.
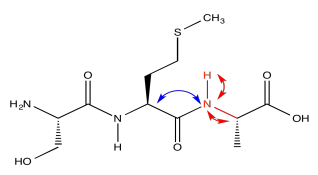
Los picos rojos de abajo son los que tuvimos del experimento anterior. Demuestran esa relación entre el protón amida, el nitrógeno amida y el carbono alfa. El pico azul muestra el carbono alfa en el otro lado del carbonilo. Observe que el pico azul en el corte de la derecha es el mismo que el pico rojo en el corte de la izquierda. Por supuesto, en un tripéptido, uno de los aminoácidos está justo al lado del otro.
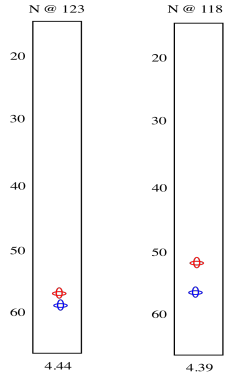
Todavía puede no estar claro qué rebanada proviene de qué nitrógeno amida. Sin embargo, hay otra variación en este experimento que puede ayudar. Esta muestra no solo los carbonos alfa en ambos lados del nitrógeno de la amida, sino también los carbonos beta.
En las rebanadas de abajo, además de los picos rojos y los picos azules que teníamos antes, ahora tenemos un par de picos verdes. Esos picos verdes muestran los carbonos beta en cada lado.
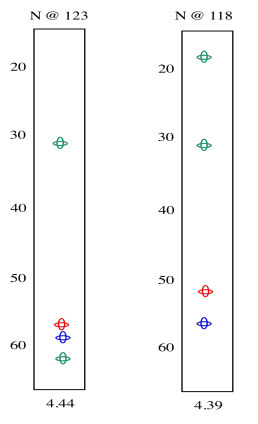
En la rebanada izquierda, hay un pico verde a los 30 y uno a los 62. El pico a 62 debe ser el carbono beta de la serina, ya que está al lado de un oxígeno. El pico a los 30 es probablemente el carbono beta en la metionina. En la rodaja derecha, el pico a 20 debe ser el carbono metílico en alanina. El carbono beta de la metionina vuelve a aparecer, debido a que la metionina se encuentra en medio de este tripéptido —está al lado de ambas posiciones amida—. Ahora podemos ver que el corte izquierdo vino de la posición amida izquierda en el tripéptido, como se dibujó arriba, mientras que el corte de la derecha vino de la posición amida derecha.
Ejercicio\(\PageIndex{1}\)
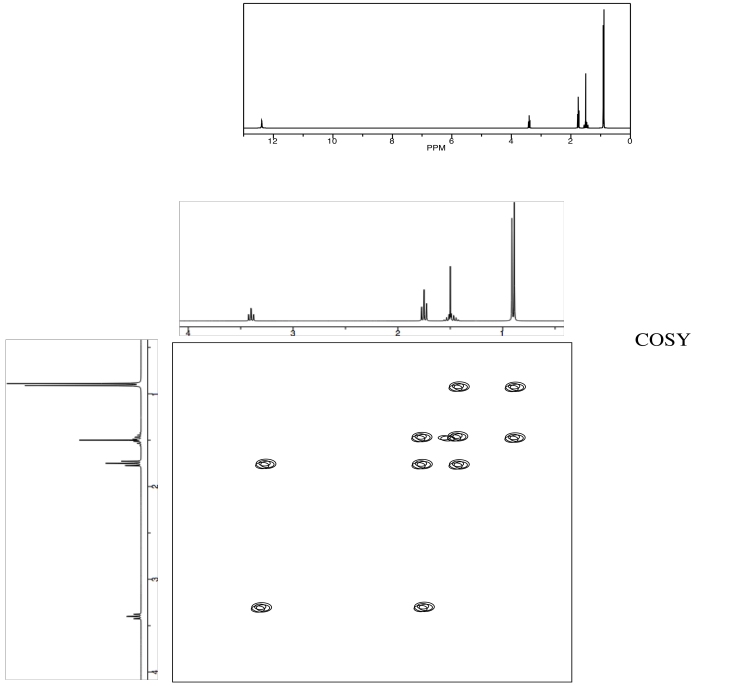
Identificar el siguiente aminoácido.
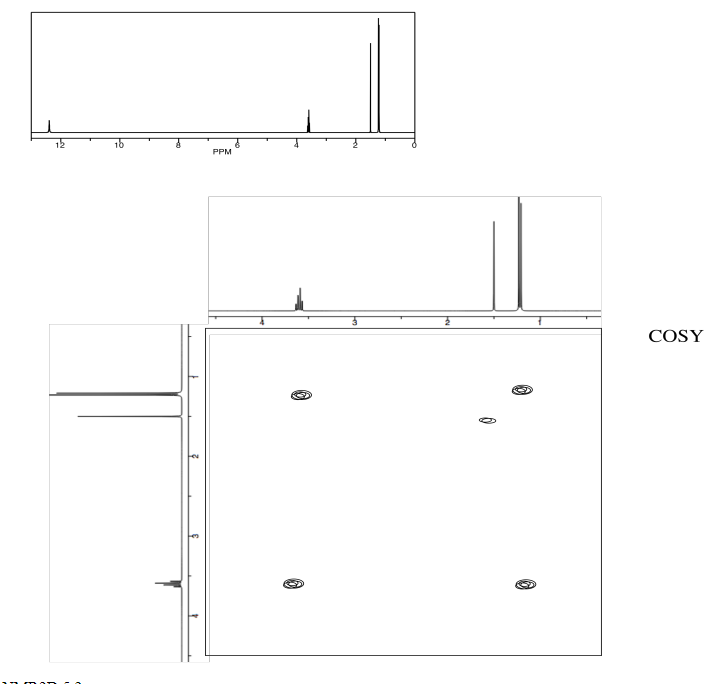
- Contestar
-
Ejercicio\(\PageIndex{2}\)
Identificar el siguiente aminoácido.
- Contestar
-
Ejercicio\(\PageIndex{3}\)
Identificar el siguiente aminoácido.
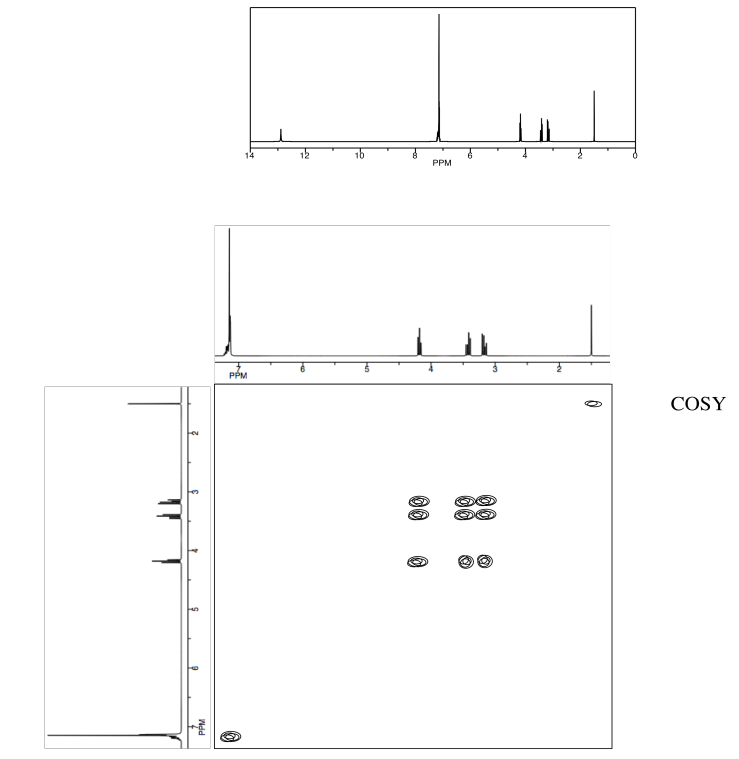
- Contestar
-
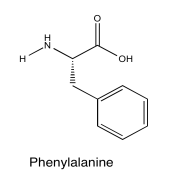
Ejercicio\(\PageIndex{4}\)
Identificar este dipéptido.
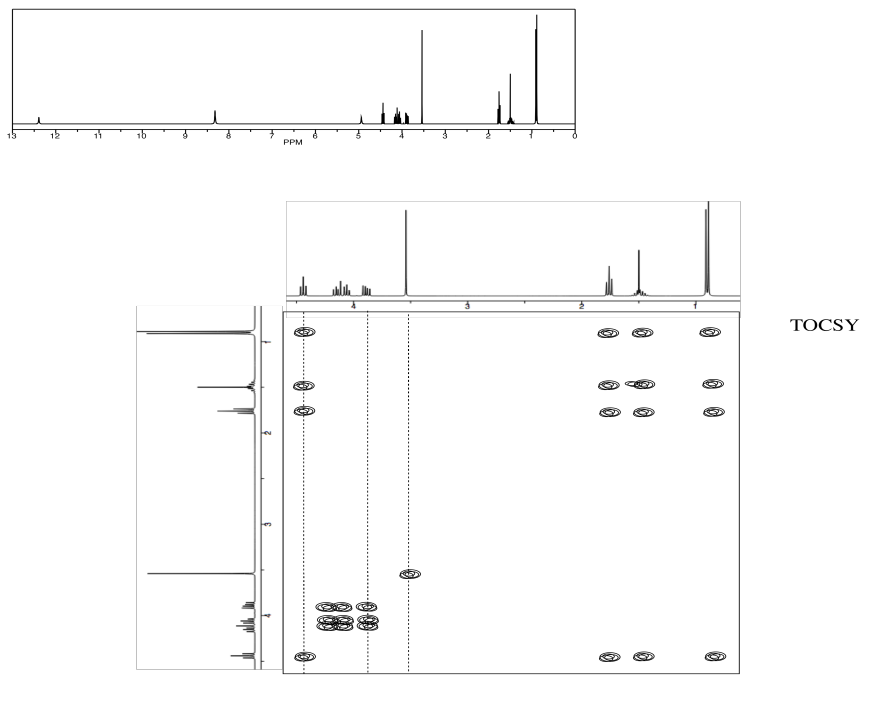
- Utilice el TOCSY para identificar los dos aminoácidos involucrados.
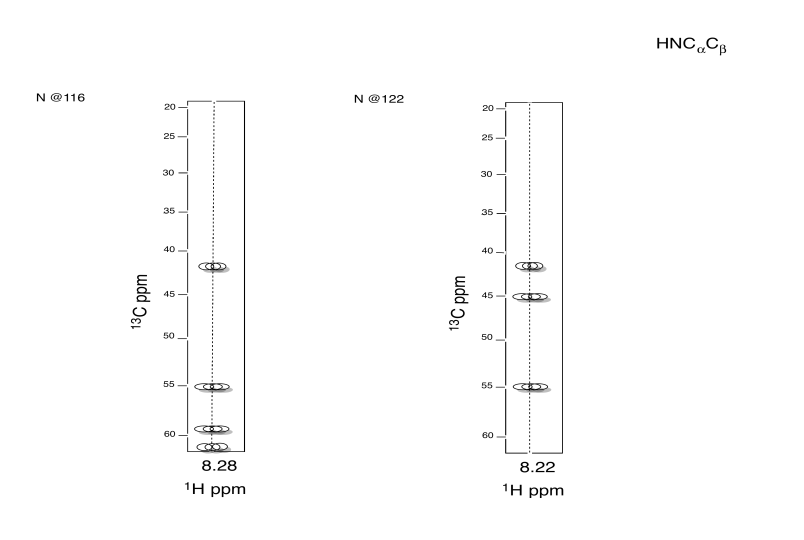
- Utilice HNCA para determinar la conectividad.
Referencias Útiles
- TOCSY/COSY de aminoácidos: http://www.bp.uni-bayreuth.de/NMR/nmr_aminotocsy.html
- TOCSY de todos los AA: http://www.bp.uni-bayreuth.de/NMR/nmr_alltocsy.html
- Turnos Estándar para AA: http://www.bmrb.wisc.edu/ref_info/statsel.htm
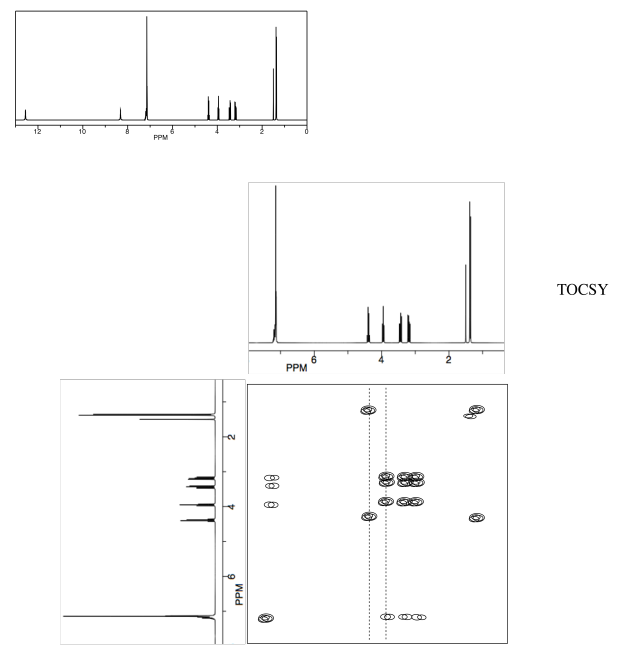
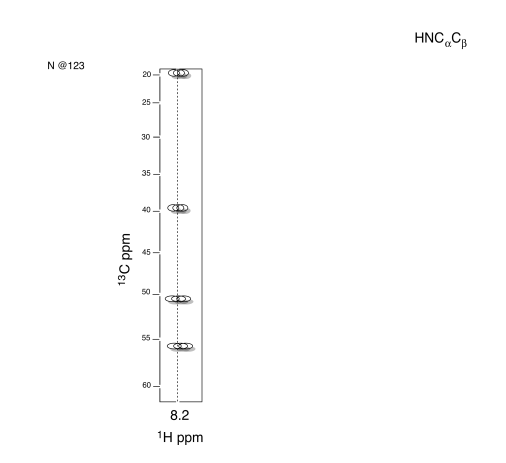
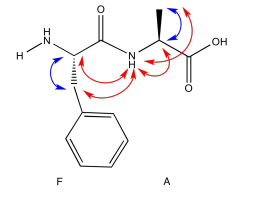
- Contestar
-
Ejercicio\(\PageIndex{5}\)
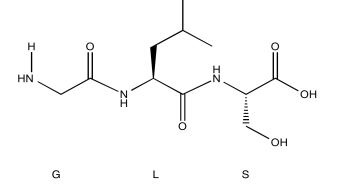
Identificar este tripéptido.
- Utilice el TOCSY para identificar los dos aminoácidos involucrados.
- Utilice HNCA para determinar la conectividad.
- Contestar
-
Fuentes
Espectros de RMN 1H, TOCSY, HNCA y COSY simulados.

