3.2.4: Empaque Cierre de Ligando
- Page ID
- 81301
Introducción
La teoría del empaque cercano de ligandos (LCP) es complementaria a VSEPR, excepto que el LCP se centra en las repulsiones entre átomos colgantes (átomos “externos” que no están unidos directamente entre sí), en lugar de enfocarse en el entorno químico alrededor del átomo central en una molécula. Tanto los modelos LCP como los VSEPR fueron desarrollados por Robert Gillespie.
El modelo LCP asume que los ligandos (o átomos colgantes) se “empaquetan” lo más cerca posible alrededor de un átomo central. Un ligando dado tendrá un radio atómico específico cuando se une a un átomo central. La distancia entre dos ligandos alrededor del mismo átomo central es simplemente la suma de los radios atómicos de los átomos colgantes. Por lo tanto, para un conjunto específico de ligandos alrededor de un átomo central específico, las distancias ligando-ligando son constantes a pesar del número de coordinación o ángulos de enlace. Es decir, para una serie de moléculas similares con el mismo átomo central, mientras que los ángulos de enlace y las distancias de enlace de los átomos colgantes pueden cambiar, las distancias entre dos átomos colgantes siguen siendo las mismas.
Según LCP, las distancias entre dos átomos colgantes son similares...
- incluso cuando el número estérico cambia
- incluso cuando los ángulos de unión cambian
- Motivo: los átomos colgantes “empaquetan” alrededor del átomo central.
Ligando Cerrar Empaque y Distancia de Enlace
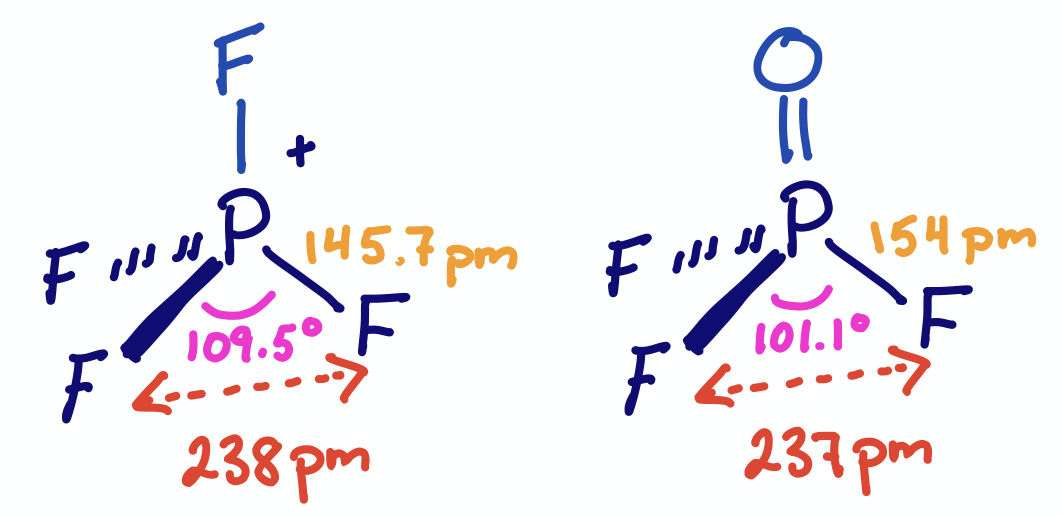
Si la distancia entre los átomos no enlazados permanece constante incluso mientras cambian los ángulos de enlace, entonces la longitud del enlace entre el átomo colgante y el átomo central debe cambiar para acomodarse. Por ejemplo,\(\ce{PF4+}\) y\(\ce{PF3O}\) tienen\(\ce{F - F}\) distancias casi idénticas de 238 y 237pm, respectivamente. Como se esperaba de VSEPR, el ángulo de\(\ce{F - P - F}\) unión adentro\(\ce{PF4+}\) es de 109.5°. El ángulo de\(\ce{F - P - F}\) unión en\(\ce{PF3O}\) (101.1°) es menor debido a la mayor repulsión del doble enlace de oxígeno. Por lo tanto, las longitudes de enlace P-F deben ser diferentes. De hecho, las distancias de enlace P-F son 145.7 pm adentro\(\ce{PF4+}\) y 154pm adentro\(\ce{PF3O}\).
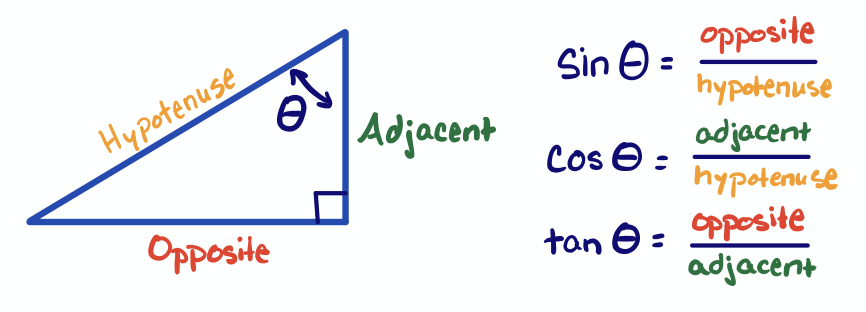
La relación entre los ángulos de unión, las longitudes de unión y la distancia de empaquetamiento cercano se describe mediante trigonometría de ángulo recto (recordar SOA-CAH-TOA). En un triángulo rectángulo, la hipotenusa es el lado más largo, opuesto al ángulo recto. Para cualquiera de los otros dos ángulos del triángulo, el ángulo (\(\theta\)) y las longitudes de los lados (opuestos y adyacentes a\(\theta\)) están relacionados por las funciones trigométricas mostradas en la Figura\(\PageIndex{2}\).
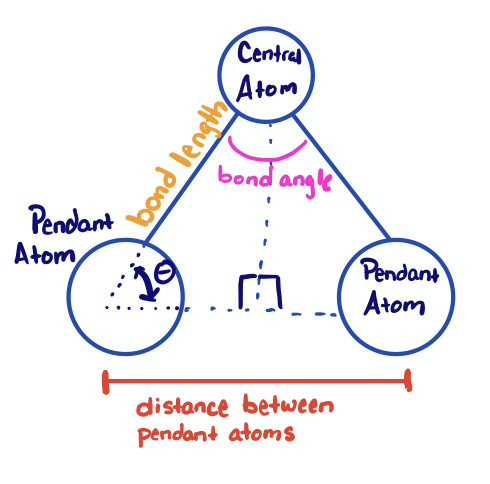
En el caso de una molécula, podemos aplicar trigonometría de ángulo recto imaginando que el ángulo de unión se divide en dos ángulos rectos, como se ilustra en la Figura\(\PageIndex{2}\). La hipotenusa de los triángulos es la longitud de unión, el lado opuesto es la mitad de la distancia de empaquetamiento cercano y\(\theta\) es la mitad del ángulo de unión.
La distancia entre los átomos F es de 212pm en ambos\(\ce{NF4+}\) y\(\ce{NF3}\). Los ángulos de unión son 109.5° y 102.3°, respectivamente. ¿Cuáles son las longitudes de\(\ce{N - F}\) unión esperadas?
- Responder
-
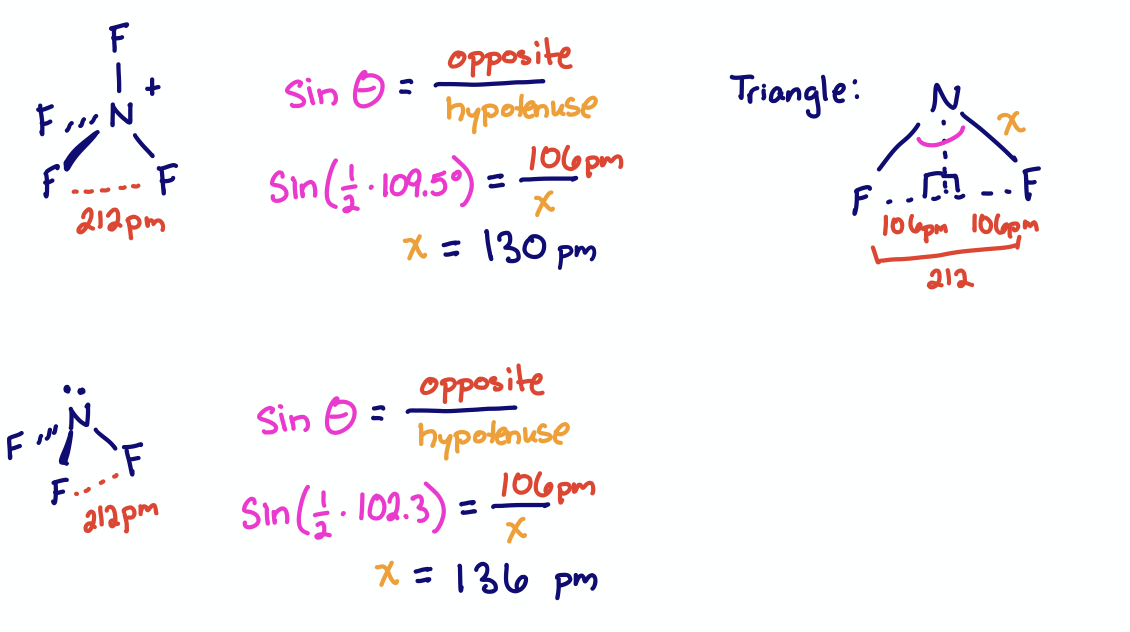
Las longitudes reales de unión medidas son 130pm para\(\ce{NF4+}\) y 136.5 pm para\(\ce{NF3}\).


