11.3.2: Diagramas de correlación
- Page ID
- 81135
División de términos en un campo octaédrico

Hasta el momento solo hemos considerado términos de iones libres, lo que significa términos sin la presencia de un campo ligando. Pensemos a continuación sobre la influencia de un campo octaédrico en un término. Los términos son ondulaciones, al igual que los orbitales, y por lo tanto se comportan como orbitales en un campo de ligandos. Por ejemplo, los\(d\) -orbitales se dividen en\(t_{2g}\) y\(e_g\) orbitales en un campo de ligando octaédrico. A\(D\) -term se comporta de manera similar. Se divide en\(T_{2g}\) y\(E_g\) términos (¡anote las letras mayúsculas que describen término, y las letras minúsculas que describen orbitales!). \ Los\(p\) orbitales son triple-degenerados, teniendo\(T_{1g}\) simetría en el grupo de puntos\(O_h\) (octaédricos), y no se dividen en energía: dan los\(t_{1g}\) orbitales bajo un campo octaédrico. De igual manera, los\(P\) términos -tienen la misma simetría y tampoco se dividen. El\(P\) -término se convierte en un\(T_{1g}\) término en un campo octaédrico.
Siguiendo argumentos análogos, los\(S\) términos se convierten en\(A_{1g}\) términos. \(F\)los términos se dividen en energía como\(f\) -orbitales y se convierten\(T_{1g}\),\(T_{2g}\), y\(A_{2g}\) términos. En general, la presencia del campo octaédrico incrementa el número de términos de cuatro a siete (Figura\(\PageIndex{1}\)). Es fácil ver que el campo del ligando conduce a muchos estados, y muchas transiciones potenciales de electrones. Así, esperaríamos espectros bastante complicados. Para otros campos de ligandos, los términos también se comportan de manera análoga a los orbitales. Por ejemplo, en un campo tetraédrico los términos D se dividen en términos E y T 2, y así sucesivamente.
División a término para complejos metálicos octaédricos d 2
Ahora pensemos en cómo cambia el término energías de nuestro ion d 2 libre cuando se coloca en un campo ligando octaédrico, dependiendo de la fuerza del campo del ligando. Podemos expresarlo mediante un diagrama de correlación (Figura\(\PageIndex{2}\)). En un diagrama de correlación, trazamos las energías de los términos relativos a la intensidad de campo.
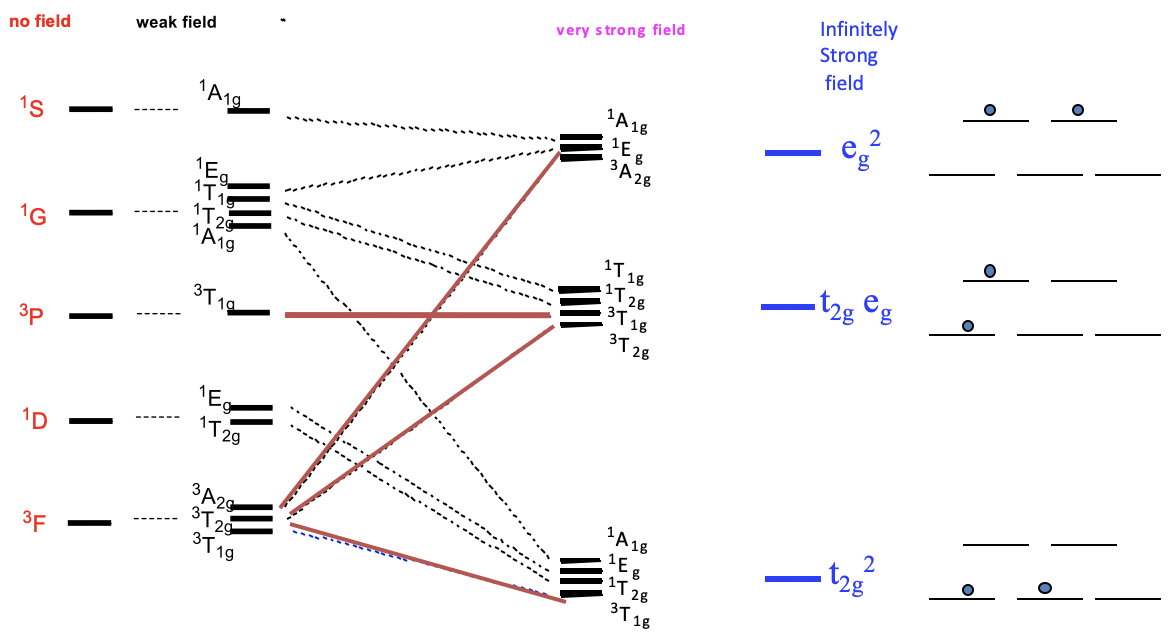
En el lado izquierdo trazamos los términos sin ningún campo de acuerdo a sus energías. En el caso de un ion d 2, las energías son
\[\ce{^{3}F < ^{1}D < ^{3}P < ^{1}G < ^{1}S}. \nonumber\]
A continuación, trazamos las energías relativas en un campo de ligando octaédrico débil y etiquetamos los términos según su simetría. Podemos ver que los términos D, F y G se dividen en energía, mientras que los términos S y P no lo hacen. Debido al campo débil, las diferencias de energía son muy pequeñas. Ahora aumentemos la fuerza del campo del ligando continuamente, hasta que hayamos alcanzado un campo de ligando muy fuerte. Vemos que algunos de los términos se mueven hacia arriba en energía, mientras que otros términos bajan a medida que aumenta el campo de ligandos. Por ejemplo, dos de los tres términos resultantes de los términos F aumentan en energía mientras que uno disminuye. También es posible que un término no cambie su energía. Por ejemplo, el término 3 T 1g del término 3 P no cambia su energía. En campo ligando muy fuerte hay tres grupos de términos que tienen energía similar. En el caso hipotético de un campo ligando infinitamente fuerte, los términos que pertenecen a un grupo particular se vuelven idénticos en energía. En este caso, sólo hay tres estados para los electrones posibles. El campo se considera tan fuerte que la energía asociada con las interacciones electrón-electrón se vuelve insignificante en comparación con la energía del campo. Los electrones se comportan como si no hubiera interacciones electrón-electrón. Por lo tanto, podemos llamar al estado de energía más bajo el estado t 2g 2. Es equivalente al estado de los dos electrones que están en los orbitales t 2g. El segundo estado se llama estado t 2g e g. Es equivalente al estado de que un electrón esté en el t 2g y un electrón en los orbitales e g. El tercer estado se llama el estado e g 2, que es equivalente al estado con ambos electrones en los orbitales e g 2.


