4.5: Estructura y Función (Ejercicios)
- Page ID
- 77381
Se trata de ejercicios de tarea para acompañar al Capítulo 4 del LibreTexto de la Universidad de Kentucky para CHE 103 - Química para la Salud Aliada. Las soluciones están disponibles debajo de las preguntas.
Preguntas
(Haga clic aquí para obtener soluciones)
Q4.1.1
Describir una estructura de Lewis.
Q4.1.2
¿Cuántos enlaces suelen formar cada elemento?
- azufre
- hidrógeno
- nitrógeno
- fósforo
Q4.1.3
¿Cuántos enlaces tiende a formar el oxígeno? ¿Qué combinaciones de enlaces (simples, dobles, triples) puede tener?
Q4.1.4
¿Cuántos enlaces tiende a formar el carbono? ¿Qué combinaciones de enlaces (simples, dobles, triples) puede tener?
Q4.1.5
Utilizando la Tabla 4.1.1, dibuje la estructura de Lewis para cada molécula.
a. H 2 S
b. CCl 4
c. PF 3
d. C 2 H 4
(haga clic aquí para obtener soluciones)
Q4.2.1
Dado un tipo de estructura (Lewis, condensada o esquelética), dibuje los otros dos.
| a. | CH 3 CH 2 CH 3 |
| b. |  |
| c. | 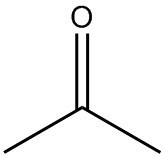 |
| d. | CH 3 CHBrCH 2 CH 2 CHClCH 3 |
| e. | CH 2 (OH) CH 2 CH 2 CH 3 |
| f. |  |
| g. |  |
(haga clic aquí para obtener soluciones)
Q4.3.1
¿Cómo afecta la presencia de un par solitario a la forma de la molécula?
Q4.3.2
¿Cuál es el ángulo de enlace “ideal” en una molécula tetraédrica (AB 4)? ¿Cómo cambia eso en piramidal trigonal (AB 3 E)? Doblada (AB 2 E 2)?
Q4.3.3
¿Cuál es el ángulo de unión ideal para las moléculas trigonales planas (AB 3)? ¿Cuál sería el ángulo de unión esperado para una molécula doblada (AB 2 E)?
Q4.3.4
Determinar la geometría electrónica para cada una de las siguientes moléculas.
| a. |  |
| b. |  |
| c. |  |
| d. |  |
| e. |  |
| f. |  |
(haga clic aquí para obtener soluciones)
Q4.4.1
Circular y etiquetar los grupos funcionales en cada molécula. Puede haber más de un grupo funcional en una molécula.
| a. |  |
| b. |  |
| c. |  |
| d. |  |
| e. |  |
| f. |  |
Q4.4.2
Dibuja una molécula que contenga un éster, un alcohol y un aldehído.
Q4.4.3
Etiquetar cada alcohol como primario, secundario o terciario.
| a. |  |
| b. |  |
| c. |  |
| d. |  |
Q4.4.4
Marcar cada amina como primaria, secundaria o terciaria.
| a. |  |
| b. |  |
| c. |  |
| d. |  |
| e. |  |
RESPUESTAS
4.1: Estructuras de punto de electrones de Lewis
Q4.1.1
Una estructura de Lewis muestra las conexiones entre los átomos (enlaces simples, dobles o triples) así como cualquier electrón no enlazante.
Q4.1.2
- 2
- 1
- 3
- 3
Q4.1.3
2 bonos en total; 2 enlaces simples o 1 doble enlace
Q4.1.4
4 bonos en total; 4 simples o 2 simples y 1 doble o 2 dobles o 1 simple y 1 triple
Q4.1.5
| a. |  |
| b. |  |
| c. |  |
| d. |  |
4.2: Representando estructuras
Q4.2.1
Dado un tipo de estructura (Lewis, condensada o esquelética), dibuje los otros dos.
| Estructura de Lewis | Estructura condensada | Estructura esquelética | |
| a. |  |
CH 3 CH 2 CH 3 |  |
| b. | 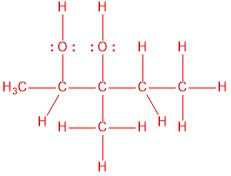 |
CH 3 CH (OH) C (CH 3) (OH) CH 2 CH 3 |  |
| c. |  |
CH 3 C (O) CH 3 |  |
| d. | 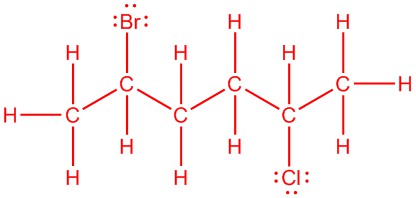 |
CH 3 CHBrCH 2 CH 2 CHClCH 3 |  |
| e. | 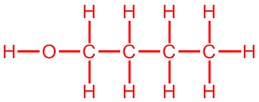 |
CH 2 (OH) CH 2 CH 2 CH 3 | 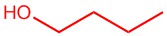 |
| f. |  |
CH 3 CH (CH 3) CH 2 CH 2 CH 3 |  |
| g. |  |
CH 3 CCCH 3 |  |
4.3: Formas Moleculares
Q4.3.1
Un par solitario provoca la compresión de otros ángulos de enlace en la molécula.
Q4.3.2
AB 4: 109.5°
AB 3 E: 107° (menos de AB 4)
AB 2 E 2: 104.5° (menos de AB 3 E)
Q4.3.3
AB 3: 120°
AB 2 E: menos de 120°
Q4.3.4
- plano trigonal
- lineal
- tetraédrico
- lineal
- plano trigonal
- tetraédrico
4.4: Grupos Funcionales
Q4.4.1
| a. |  |
| b. |  |
| c. | 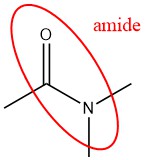 |
| d. | 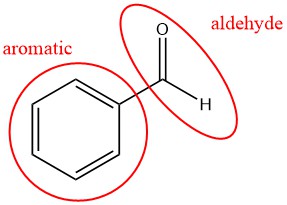 |
| e. |  |
| f. |  |
Q4.4.2
Las respuestas variarán. Se muestra un ejemplo.
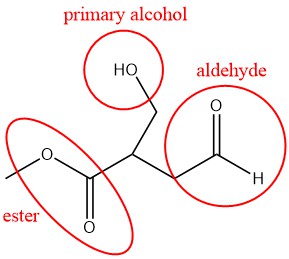
Q4.4.3
- secundaria
- primaria
- secundaria
- terciario
Q4.4.4
- primaria
- primaria
- secundaria
- terciario
- secundaria

