13.1: Aminoácidos
- Page ID
- 77398
Resultados de aprendizaje
- Identificar componentes estructurales de un aminoácido.
- Definir zwitterion y punto isoeléctrico.
- Determinar la carga en un aminoácido cuando no está en el punto isoeléctrico.
- Marcar los aminoácidos como polares y no polares y como ácidos, básicos o neutros.
El atletismo es muy competitivo en estos días en todos los niveles, desde los deportes escolares hasta los profesionales. Todo el mundo está buscando ese borde que los haga más rápidos, más fuertes, más en forma física. Un enfoque adoptado por muchos atletas es el uso de suplementos de aminoácidos. La teoría es que el aumento de aminoácidos en la dieta conducirá a un aumento de proteínas para los músculos. No obstante, el único beneficio real llega a las personas que fabrican y venden las pastillas. Los estudios no han mostrado ninguna ventaja obtenida por los propios atletas. Estás mucho mejor con solo mantener una dieta saludable.
Aminoácidos
Un aminoácido es un compuesto que contiene tanto un grupo\(\left( \ce{-NH_2} \right)\) amina como un grupo carboxilo\(\left( \ce{-COOH} \right)\) en la misma molécula. Si bien es posible imaginar cualquier cantidad de aminoácidos, los bioquímicos generalmente reservan el término para un grupo de 20 aminoácidos que son formados y utilizados por organismos vivos. La siguiente figura muestra la estructura general de un aminoácido. Cualquiera de las dos estructuras se considera correcta para un aminoácido.

Los grupos amina y carboxilo de un aminoácido están ambos unidos covalentemente a un átomo de carbono central. Ese átomo de carbono también está unido a un átomo de hidrógeno y a un\(\ce{R}\) grupo. Es este\(\ce{R}\) grupo el que varía de un aminoácido a otro y se llama la cadena lateral del aminoácido.

La naturaleza de las cadenas laterales explica la variabilidad en las propiedades físicas y químicas de los diferentes aminoácidos. Cada aminoácido se agrupa en función de las propiedades de la cadena lateral. Los grupos se designan como polares (hidroxílicos, que contienen azufre, amídicos), no polares (alifáticos y aromáticos), ácidos o básicos.
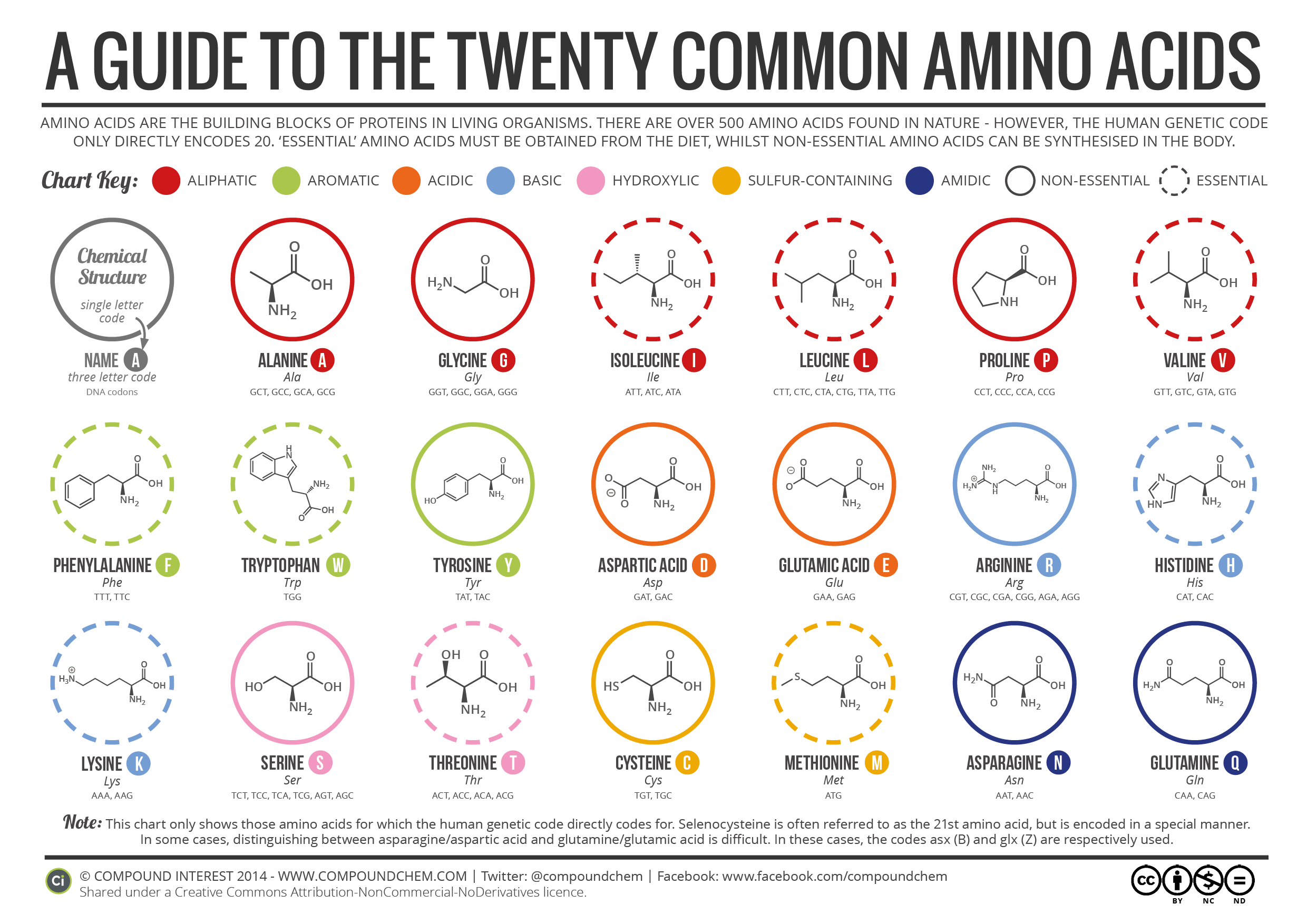
Además del nombre completo del aminoácido, también hay abreviaturas de una letra y tres letras para cada uno. Estas abreviaturas son especialmente útiles a la hora de enumerar los aminoácidos en una proteína (una cadena de muchos aminoácidos que se discutirán más adelante).
Reglas para clasificar aminoácidos
Las siguientes reglas (junto con dos excepciones) pueden ayudarte a clasificar los aminoácidos como no polares, ácidos polares (a veces llamados ácidos), polares básicos (a veces llamados básicos) o polares neutros. Analizaremos dos excepciones pero tenga en cuenta que la transición de neutro no polar a polar es una transición gradual (como los colores de un arco iris) por lo que es posible que veas variaciones en cómo se clasifican los aminoácidos si miras otras fuentes.
- Los aminoácidos no polares (hay 9) contienen cadenas alifáticas (hidrocarburos) o anillos aromáticos.
- Los aminoácidos ácidos polares (2) contienen un grupo ácido carboxílico (o carboxilato) en la cadena lateral (grupo R). Esto se suma al que se encuentra en la cadena principal del aminoácido.
- Los aminoácidos básicos polares (3) contienen un grupo amina (puede ser neutro o cargado) en la cadena lateral (grupo R). Esto se suma al que se encuentra en la cadena principal del aminoácido.
- Los aminoácidos neutros polares (6) contienen un hidroxilo (-OH), azufre o amida en el grupo R).
Existen dos excepciones importantes a las reglas anteriores.
- La tirosina tiene un grupo aromático y un grupo -OH y se considera polar neutra.
- La metionina contiene azufre pero como parte de la cadena de carbono. El azufre tiene la misma electronegatividad que el carbono, por lo que se considera no polar.
Zwitterion
Los aminoácidos se extraen típicamente sin cargas o con una carga positiva y negativa (ver figura 13.1.1). Cuando un aminoácido contiene tanto una carga positiva como una negativa en la “cadena principal”, se llama zwitterión y tiene una carga neutra general. El zwitterión de un aminoácido existe a un pH igual al punto isoeléctrico. Cada aminoácido tiene su propio valor de pI basado en las propiedades del aminoácido. A valores de pH por encima o por debajo del punto isoeléctrico, la molécula tendrá una carga neta que depende de su valor de pI así como del pH de la solución en la que se encuentre el aminoácido.
pH < pI
Cuando el pH es menor que el pI, hay una cantidad\(\ce{H^+}\) en exceso de solución. El exceso\(\ce{H^+}\) es atraído por el ion carboxilato cargado negativamente dando como resultado su protonación. El ion carbohidrato está protonado, haciéndolo neutro, dejando solo una carga positiva en el grupo amina. En general, el aminoácido tendrá una carga de\(+1\).

pH > pI
Cuando el pH es mayor que el pI, hay una cantidad\(\ce{OH^-}\) en exceso de solución. El exceso\(\ce{OH^-}\) es atraído por el grupo amina cargado positivamente dando como resultado la eliminación de un\(\ce{H^+}\) ion para formar (\ ce {H_2O}\). El grupo amina tiene una carga neutra dejando solo una carga negativa en el grupo carboxilato. En general, el aminoácido tendrá una carga de\(-1\).

Ejemplo\(\PageIndex{1}\)
- Identifique el aminoácido que se muestra a continuación.
- Encuentra el valor de pI para el aminoácido.
- Determinar cómo existirá el aminoácido a pH = 3.52
- Determinar cómo existirá el aminoácido a pH = 9.34
- Determinar cómo existirá el aminoácido a pH = 5.02

Solución:
a. Mirar la cadena lateral para identificar el aminoácido. La cadena lateral contiene la\(\ce{-CH_2SH}\) cual coincide con la estructura de la cisteína.
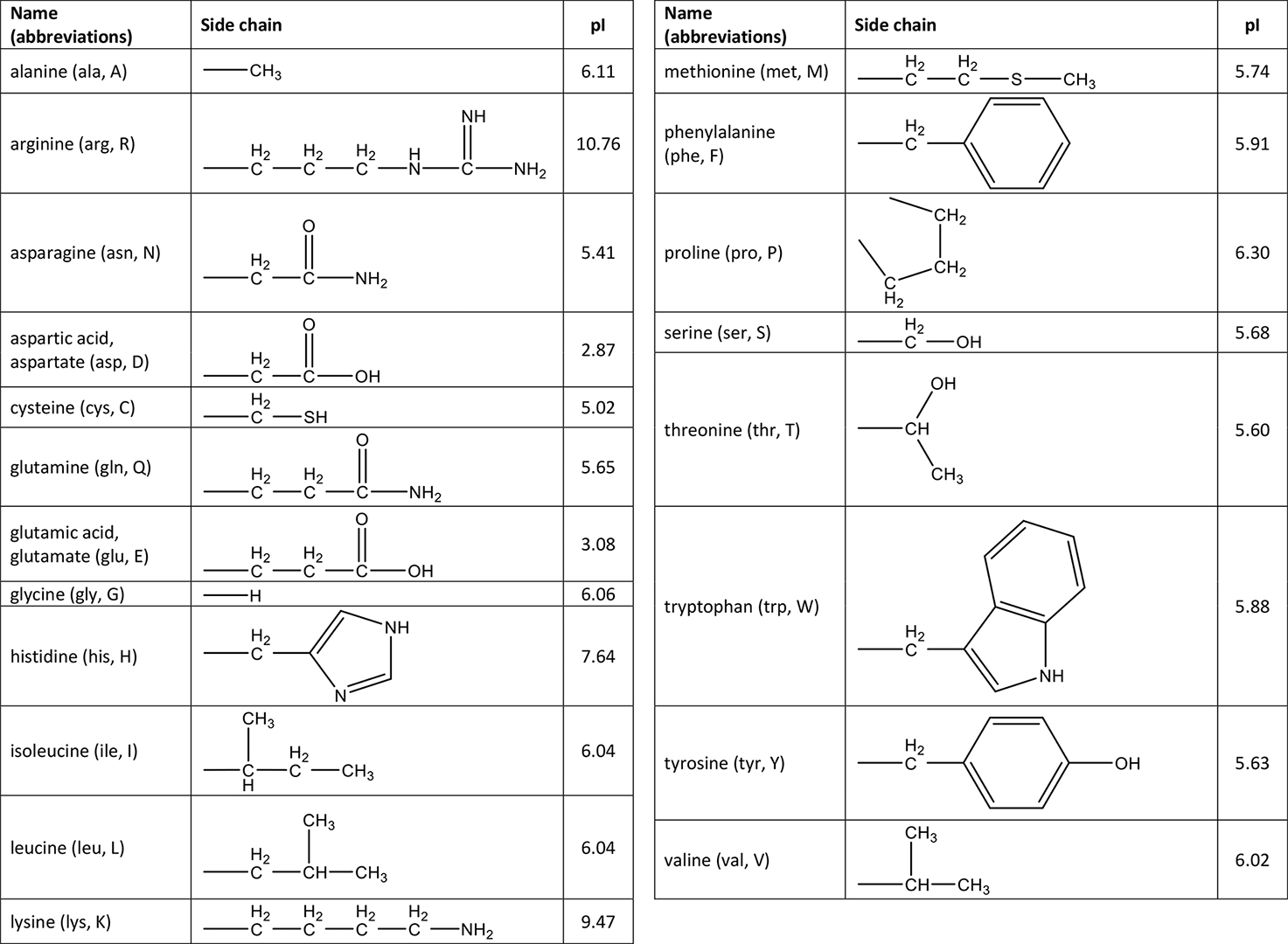
b. Los valores de pI para los aminoácidos se encuentran en la tabla de aminoácidos. Para cisteína, pI = 5.02.
c. A pH = 3.52, la\(\ce{H^+}\) concentración es alta (pH bajo = más ácido = más\(\ce{H^+}\)). Por lo tanto,\(\ce{H^+}\) se sumará al ion carboxilato y neutralizará la carga negativa. El aminoácido tendrá una carga positiva en el grupo amina restante y tendrá una carga general de\(+1\).

d. A pH = 9.34, la\(\ce{OH^-}\) concentración es alta (pH alto = más básico = menos\(\ce{H^+}\) = más\(\ce{OH^-}\)). Por lo tanto, el se\(\ce{OH^-}\) sentirá atraído por el grupo amina cargado positivamente y le “robará” una\(\ce{H^+}\). Como resultado, la única carga restante estará en el ion carboxilato por lo que el aminoácido tendrá una\(-1\) carga.

e. A pH = 5.02, el pH = pI por lo que el aminoácido existirá como el zwitterión con las cargas tanto positivas como negativas como se muestra anteriormente.
Colaboradores y Atribuciones
CK-12 Foundation by Sharon Bewick, Richard Parsons, Therese Forsythe, Shonna Robinson, and Jean Dupon.
Allison Soult, Ph.D. (Department of Chemistry, University of Kentucky)

