13.2: Péptidos
- Page ID
- 77384
Resultados de aprendizaje
- Definir polipéptido.
- Identificar enlace amida.
- Predecir producto de condensación de aminoácidos.
- Nombre polipéptidos dada la abreviatura de los aminoácidos.
Las células peptídicas en nuestros cuerpos tienen un mecanismo intrincado para la fabricación de proteínas. Los humanos tienen que utilizar otras técnicas para sintetizar las mismas proteínas en un laboratorio. La química de la síntesis de péptidos es complicada. Ambos grupos activos en un aminoácido pueden reaccionar y la secuencia de aminoácidos debe ser específica para que la proteína funcione. Robert Merrifield desarrolló el primer enfoque sintético para hacer proteínas en el laboratorio, un enfoque manual que fue largo y tedioso (y, ganó el Premio Nobel de Química en 1984 por su trabajo). Hoy en día, sin embargo, los sistemas automatizados pueden producir un péptido en un período de tiempo muy corto.
Péptidos
Un péptido es una combinación de aminoácidos en la que el grupo amina de un aminoácido ha sufrido una reacción con el grupo carboxilo de otro aminoácido. La reacción es una reacción de condensación, formando un grupo amida\(\left( \ce{CO-N} \right)\), que se muestra a continuación.
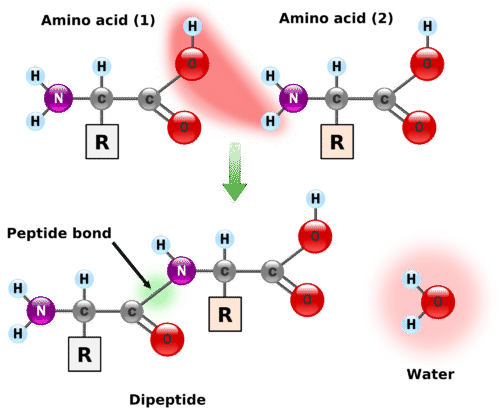
Un enlace peptídico es el enlace amida que se produce entre el nitrógeno amínico de un aminoácido y el carbono carboxilo de otro aminoácido. La molécula resultante se llama dipéptido. Observe que las cadenas laterales particulares de cada aminoácido son irrelevantes ya que los\(\ce{R}\) grupos no están involucrados en el enlace peptídico.
El dipéptido tiene un grupo amina libre en un extremo de la molécula (conocido como el\(\ce{N}\) extremo -terminal) y un grupo carboxilo libre en el otro extremo (conocido como el\(\ce{C}\) extremo -terminal). Cada uno es capaz de extender la cadena a través de la formación de otro enlace peptídico. La secuencia particular de aminoácidos en una cadena más larga se denomina secuencia de aminoácidos. Por convención, la secuencia de aminoácidos se enumera en el orden tal que el grupo amina libre está en el extremo izquierdo de la molécula y el grupo carboxilo libre está en el extremo derecho de la molécula. Por ejemplo, supongamos que se forma una secuencia de los aminoácidos glicina, triptófano y alanina con el grupo amina libre como parte de la glicina y el grupo carboxilo libre como parte de la alanina. La secuencia de aminoácidos se puede escribir fácilmente usando las abreviaturas como Gly-Trp-Ala. Esta es una secuencia diferente de Ala-Trp-Gly porque los grupos amina y carboxilo libres estarían en diferentes aminoácidos en ese caso.
Ejemplo\(\PageIndex{1}\)
Dibujar el polipéptido Asp-Val-Ser.
Solución
1. Identificar las estructuras de cada uno de los tres aminoácidos dados y dibujarlos en el mismo orden dado en el nombre.
2. Dejando el orden igual, conectar los aminoácidos entre sí formando enlaces peptídicos. Tenga en cuenta que el orden dado en el nombre es de la misma manera que los aminoácidos están conectados en la molécula. El primero en la lista es siempre el\(\ce{N}\) extremo terminal del polipéptido.
Ejemplo\(\PageIndex{2}\)
Enumere todos los posibles polipéptidos que se pueden formar a partir de cisteína (Cys), leucina (Leu) y arginina (Arg).
Solución
Aunque solo hay tres aminoácidos, el orden en el que están unidos cambia la identidad, las propiedades y la función del polipéptido resultante. Hay seis posibles polipéptidos formados a partir de estos tres aminoácidos.
Cys-Leu-Arg
Cys-Arg-Leu
Leu-Cys-Arg
Leu-Arg-Cys
Arg-Cys-Leu
Arg-Leu-Cys
Colaboradores y Atribuciones
CK-12 Foundation by Sharon Bewick, Richard Parsons, Therese Forsythe, Shonna Robinson, and Jean Dupon.
Allison Soult, Ph.D. (Department of Chemistry, University of Kentucky)




