15.5: Usos de isótopos radiactivos
- Page ID
- 74729
- Aprende algunas aplicaciones de la radiactividad.
Los isótopos radiactivos tienen una variedad de aplicaciones. Generalmente, sin embargo, son útiles porque o podemos detectar su radiactividad o podemos usar la energía que liberan.
Los isótopos radiactivos son trazadores efectivos porque su radiactividad es fácil de detectar. Un trazador es una sustancia que se puede utilizar para seguir el camino de esa sustancia a través de alguna estructura. Por ejemplo, las fugas en las tuberías de agua subterránea se pueden descubrir haciendo pasar algo de agua que contiene tritio a través de las tuberías y luego usando un contador Geiger para localizar cualquier tritio radiactivo presente posteriormente en el suelo alrededor de las tuberías. (Recordemos que el tritio es un isótopo radiactivo de hidrógeno.)
Los trazadores también se pueden utilizar para seguir los pasos de una reacción química compleja. Después de incorporar átomos radiactivos en moléculas de reactivos, los científicos pueden rastrear a dónde van los átomos siguiendo su radiactividad. Un excelente ejemplo de esto es el uso del carbono-14 para determinar los pasos involucrados en la fotosíntesis en plantas. Conocemos estos pasos porque los investigadores siguieron el avance del carbono-14 a lo largo del proceso.
Datación radiactiva
Los isótopos radiactivos son útiles para establecer las edades de diversos objetos. La vida media de los isótopos radiactivos no se ve afectada por ningún factor ambiental, por lo que el isótopo actúa como un reloj interno. Por ejemplo, si se analiza una roca y se encuentra que contiene cierta cantidad de uranio-235 y una cierta cantidad de su isótopo hijo, podemos concluir que cierta fracción del uranio-235 original se ha descompuesto radiactivamente. Si la mitad del uranio se ha descompuesto, entonces la roca tiene una edad de una vida media de uranio-235, o aproximadamente\(4.5\times 10^{9}y\). Muchos análisis como este, utilizando una amplia variedad de isótopos, han indicado que la edad de la tierra misma ha terminado\(4\times 10^{9}y\).
En otro interesante ejemplo de datación radiactiva, la datación por hidrógeno-3 se ha utilizado para verificar las añadas declaradas de algunos vinos finos viejos.
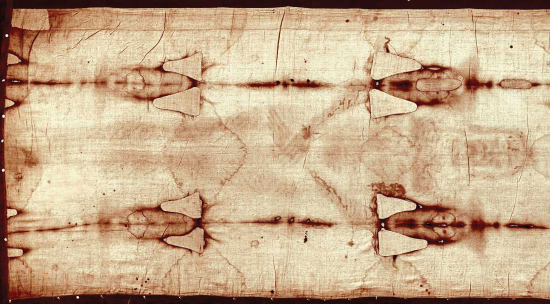
Un isótopo, el carbono-14, es particularmente útil para determinar la edad de los artefactos que alguna vez vivieron. Una pequeña cantidad de carbono-14 se produce naturalmente en los alcances superiores de la atmósfera, y los seres vivos incorporan parte de él en sus tejidos, acumulándose hasta un nivel constante, aunque muy bajo. Una vez que muere un ser vivo, ya no adquiere carbono-14; conforme pasa el tiempo el carbono-14 que estaba en los tejidos se descompone. (La vida media del carbono-14 es de 5,370 y.) Si un artefacto que alguna vez estuvo vivo es descubierto y analizado muchos años después de su muerte y el carbono-14 restante se compara con el nivel constante conocido, se puede determinar una edad aproximada del artefacto. Utilizando tales métodos, los científicos determinaron que la edad de la Sábana Santa de Turín (Figura que algunos\(\PageIndex{1}\) pretenden ser la tela funeraria de Jesucristo y compuesta por fibras de lino, un tipo de planta) es de aproximadamente 600—700 y, no 2,000 y como afirman algunos. Los científicos también pudieron utilizar la datación por radiocarbono para demostrar que la edad de un cuerpo momificado encontrado en el hielo de los Alpes era de 5,300 años.
Irradiación de Alimentos
La radiación emitida por algunas sustancias radiactivas puede ser utilizada para matar microorganismos en una variedad de alimentos, alargando la vida útil de estos productos. Los productos como tomates, hongos, brotes y bayas son irradiados con las emisiones de coba. Esta exposición mata a muchas de las bacterias que causan el deterioro, por lo que el producto se mantiene fresco por más tiempo. También se pueden irradiar huevos y algo de carne, como carne de res, cerdo y aves de corral. Contrario a la creencia de algunas personas, la irradiación de los alimentos no hace que el alimento en sí sea radioactivo.
Aplicaciones Médicas
Los isótopos radiactivos tienen numerosas aplicaciones médicas en el diagnóstico y tratamiento de enfermedades y enfermedades. Un ejemplo de aplicación diagnóstica es el uso de yodo-131 radioactivo para realizar pruebas de actividad tiroidea (Figura\(\PageIndex{1}\)). La glándula tiroides en el cuello es uno de los pocos lugares del cuerpo con una concentración significativa de yodo. Para evaluar la actividad tiroidea, se administra una dosis medida de 131 I a un paciente, y al día siguiente se utiliza un escáner para medir la cantidad de radiactividad en la glándula tiroides. La cantidad de yodo radiactivo que se acumula ahí está directamente relacionada con la actividad de la tiroides, lo que permite a médicos capacitados diagnosticar tanto el hipertiroidismo como el hipotiroidismo. El yodo-131 tiene una vida media de solo 8 d, por lo que el potencial de daño debido a la exposición es mínimo. El tecnecio-99 también se puede usar para probar la función tiroidea. Los huesos, el corazón, el cerebro, el hígado, los pulmones y muchos otros órganos se pueden obtener imágenes de manera similar usando el isótopo radiactivo apropiado.

Se necesita muy poco material radiactivo en estas técnicas de diagnóstico debido a que la radiación emitida es muy fácil de detectar. Sin embargo, las aplicaciones terapéuticas generalmente requieren dosis mucho mayores porque su propósito es matar preferentemente los tejidos enfermos. Por ejemplo, si se detectara un tumor tiroideo, una infusión mucho mayor (miles de rem, a diferencia de una dosis diagnóstica de menos de 40 rem) de yodo-131 podría ayudar a destruir las células tumorales. De igual manera, el estroncio radiactivo se utiliza no solo para detectar, sino también para aliviar el dolor de los cánceres óseos. En la\(\PageIndex{1}\) tabla se enumeran varios isótopos radiactivos y sus usos médicos.
| Isótopo | Uso |
|---|---|
| 32 P | detección y tratamiento del cáncer, especialmente en ojos y piel |
| 59 Fe | diagnóstico de anemia |
| 60 Co | irradiación con rayos gamma de tumores |
| 99 m Tc* | cerebro, tiroides, hígado, médula ósea, pulmón, corazón e intestinal; determinación del volumen sanguíneo |
| 131 I | diagnóstico y tratamiento de la función tiroidea |
| 133 Xe | imágenes pulmonares |
| 198 Au | diagnóstico de enfermedad hepática |
| *La “m” significa que es una forma metaestable de este isótopo de tecnecio. | |
Además de la aplicación directa de isótopos radiactivos al tejido enfermo, las emisiones de rayos gamma de algunos isótopos pueden dirigirse hacia el tejido a destruir. El cobalto-60 es un isótopo útil para este tipo de procedimientos.
Los amantes del vino pusieron algo de stock en añadas, o los años en los que las uvas de vino se cultivaban antes de que se convirtieran en vino. El vino puede diferir en calidad dependiendo de la añada. Algunos amantes del vino pagan voluntariamente mucho más por una botella de vino con cierta añada. Pero, ¿cómo se verifica que una botella de vino era de hecho parte de cierta añada? ¿La etiqueta es falsa? ¿Ese alijo de vino que se encuentra en el sótano de un castillo francés realmente de la década de 1940, o se hizo en 2009?

El cesio-137 es un isótopo radiactivo que tiene una vida media de 30.1 y, fue introducido en la atmósfera en las décadas de 1940 y 1950 por las pruebas atmosféricas de armas nucleares realizadas por varios países después de la Segunda Guerra Mundial. Una cantidad significativa de cesio-137 fue liberada durante el desastre nuclear de Chernobyl en 1986. Como resultado de esta contaminación atmosférica, los científicos cuentan con mediciones precisas de la cantidad de cesio-137 disponible en el medio ambiente desde 1950. Parte del isótopo del cesio es captado por plantas vivas, incluidas las vides de uva. Utilizando añadas conocidas, los enólogos (enólogos) pueden construir un análisis detallado del cesio-137 de diversos vinos a lo largo de los años.
La verificación de la añada de un vino requiere la medición de la actividad del cesio-137 en el vino. Al medir la actividad actual del cesio-137 en una muestra de vino (los rayos gamma de la desintegración radiactiva pasan fácilmente a través de botellas de vino de vidrio, por lo que no hay necesidad de abrir la botella), comparándola con la cantidad conocida de cesio-137 de la añada, y tomando en cuenta el paso del tiempo, los investigadores puede recopilar pruebas a favor o en contra de una añada de vino reclamada.
Antes aproximadamente de 1950, la cantidad de cesio-137 en el ambiente era insignificante, así que si un vino fechado antes de 1950 muestra alguna actividad medible de cesio-137, es casi seguro que es una falsificación, ¡así que no desembolses mucho dinero por ello! Puede ser un buen vino, pero casi definitivamente no tiene más de 60 años.
Resumen
La radiactividad tiene varias aplicaciones prácticas, incluyendo trazadores, aplicaciones médicas, fechar objetos que alguna vez vivieron y preservación de alimentos.


