11.5: Hidrogenación con Diimida
- Page ID
- 73648
Existen formas alternativas de agregar hidrógeno a un enlace múltiple además de los métodos catalíticos descritos en las secciones anteriores. Las más útiles de estas son las reacciones homogéneas que utilizan diimida\(\ce{HN=NH}\),, y diborano,\(\ce{B_2H_6}\).
El comportamiento y reactividad de la diimida se puede entender mejor considerando la termoquímica de hidrogenación de nitrógeno:

El primer paso es fuertemente endotérmico y es el principal obstáculo a superar en la hidrogenación del nitrógeno a amoníaco. Por el contrario, la reacción inversa, que es la deshidrogenación de la diimida, es fuertemente exotérmica. Por lo tanto, podemos esperar que la diimida tenga una pronunciada tendencia a revertir al nitrógeno molecular. Esto de hecho es así y, a temperaturas normales, la diimida existe sólo como un intermedio transitorio que no se puede aislar. Es extremadamente reactivo y transfiere fácilmente hidrógeno a enlaces múltiples carbono-carbono:

En la práctica, la diimida se genera ya que es necesaria en presencia del compuesto a hidrogenar. Existen varias formas de hacerlo, pero uno de los métodos más simples es la deshidrogenación de hidrazina con agentes oxidantes como el oxígeno atmosférico o el peróxido de hidrógeno:
\[\ce{H_2N-N_2} \underset{\text{or} \: \ce{O_2}}{\overset{\ce{H_2O_2}}{\longrightarrow}} \ce{HN=NH} + 2 \ce{H}^\oplus + 2 \ce{e}^\ominus\]
La hidrazina en realidad se ha utilizado como agente hidrogenante por más de sesenta años, pero no fue hasta la década de 1960 cuando se reconoció el intermedio de diimida en tales reacciones.
La etapa de hidrogenación es estereoespecífica y transfiere hidrógeno de manera suprafacial. Por ejemplo, los alquinos se convierten en cis-alquenos:
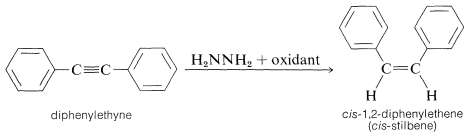
No hay etapas intermedias detectables ni reordenamientos en la hidrogenación de diimida. La reacción se visualiza como un proceso de seis centros (pericíclico) en el que los vínculos se rompen y se hacen de manera concertada:

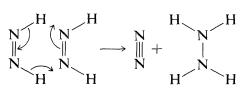
Una diferencia importante entre la hidrogenación de diimida y la hidrogenación catalítica es que la diimida reaccionará solo con enlaces simétricos o no polares\(\left( \ce{C=C}, \: \ce{C \equiv C}, \: \ce{N=N} \right)\), mientras que el hidrógeno puede agregar, aunque a regañadientes, a enlaces polares\(\left( \ce{C=O}, \: \ce{C=N} \right)\). La diimida no ataca los enlaces polares más fuertes probablemente porque no sobrevive el tiempo suficiente para hacerlo. Se autodestruye en ausencia de un sustrato reactivo para dar nitrógeno e hidrazina:
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


