14.5: Haluros de Alquenilo y Alquinilo
- Page ID
- 73311
El haluro de alquenil más fácilmente disponible es el cloroeteno (cloruro de vinilo), que se puede preparar por varias vías:

La preparación comercial más económica es la cloración de eteno a alta temperatura. Una modificación útil de este proceso utiliza cloruro de hidrógeno en lugar de cloro. Se requiere un agente oxidante para elevar el estado de oxidación del cloro\(\ce{HCl}\) al de\(\ce{Cl_2}\); para este propósito se usa oxígeno molecular junto con sales cúpricas como catalizadores.
Los métodos generales de preparación de haluros de alquinilo y alquinilo se enumeran en el Cuadro 14-5. Por haluros de alquinilo nos referimos a 1-halo-alquinos. Un método interesante por el cual se pueden preparar emplea 1-alquinos con hipohalitos:

Este tipo de reacción no procede ni con alcanos ni alquenos.
Usos del haluro de alquenil
El cloroeteno se produce en grandes cantidades para la producción de polímeros (cloruro de polivinilo) y copolímeros:

Estos polímeros comúnmente se describen como plásticos de PVC o menos específicamente como “vinilo”. Son materiales que pueden ser flexibles o rígidos de acuerdo con lo que se mezclen, y se utilizan en la fabricación de muchos artículos familiares como cortinas de plástico, ropa impermeable, baldosas de piso, artículos de cuero sintético, tapicería, tapetes de mesa, discos fonográficos, aislamiento, tuberías de plástico, tubos, y materiales de empaque.
Recientemente, se ha encontrado que las personas que trabajan en plantas que fabrican y utilizan cloroeteno tienen una incidencia inusualmente alta de un tipo inusual de cáncer de hígado. Como resultado, se han establecido estrictas regulaciones de seguridad y estándares de contaminación para las plantas donde se elabora o usa cloroeteno. Se ha reducido el uso generalizado del cloroeteno como propulsor para latas de aerosol. El cloruro de polivinilo en sí parece ser bastante seguro, pero existen posibles problemas con su incorporación a los materiales de construcción interiores, ropa y tapicería porque el calor, como el fuego, hace que el cloruro de polivinilo se descomponga, produciendo así cloruro de hidrógeno como un solo producto de descomposición. En áreas cerradas la toxicidad del gas cloruro de hidrógeno puede ser un peligro tan grave como el propio incendio. Otros polímeros pueden desprender productos igualmente tóxicos con un fuerte calentamiento.
Propiedades Químicas
La característica química sobresaliente de los haluros de alquenil es su inercia general en\(S_\text{N}1\) y\(S_\text{N}2\) reacciones. Así, el cloroeteno no reacciona con nitrato de plata en etanol (es decir, baja\(S_\text{N}1\) reactividad), no reacciona con yoduro de potasio en acetona (es decir, baja\(S_\text{N}2\) reactividad), y solo reacciona lentamente con hidróxido de sodio para dar etino (baja\(E2\) reactividad). Los haloalquinos, tales como\(\ce{RC \equiv C-Cl}\), son igualmente no reactivos.
No es de extrañar que\(\ce{=C-X}\) y\(\ce{\equiv C-X}\) los enlaces sean difíciles de romper heterolíticamente. En general,\(\ce{C-X}\) los enlaces son fuertes en haluros de alquenil (ver Cuadro 4-6) y esta propiedad tiende a hacerlos menos reactivos que los haluros de alquilo. Además, los carbonos de doble y triple enlace son más fuertemente atrayentes de electrones que los saturados\(sp^3\), razón por la cual los 1-alquinos y alquenos son ácidos más fuertes (Sección 11-8) que los alcanos. En consecuencia es más fácil romper un\(\ce{\equiv C-H}\) vínculo en el sentido\(\ce{C}^\ominus \ce{H}^\oplus\) que como\(\ce{\equiv C}^\oplus \ce{H}^\ominus\). También será más difícil ionizar un enlace carbono-halógeno\(\ce{C}^\oplus \ce{X}^\ominus\) si el carbono está insaturado. Por lo tanto, los cationes etenilo y etinilo, tales como\(\ce{CH_2=CH}^\oplus\) y\(\ce{HC \equiv C}^\oplus\), son difíciles de generar a partir de los haluros correspondientes. Se requieren grupos salientes superiores, tales como trifluorometanosulfonato,\(\ce{-OSO_3CF_3}\) (Sección 8-7C):

La razón de la falta de\(S_\text{N}2\) reactividad en haluros de etenilo o etinilo puede ser que el nucleófilo atacante es incapaz de reaccionar por el mecanismo de inversión concertado que invariablemente se observa con haluros de alquilo:
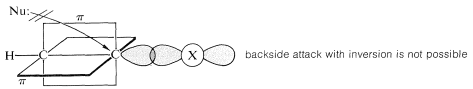
Sin embargo, la sustitución del halógeno ocurre en algunas circunstancias. En tales casos, el nucleófilo primero se agrega al enlace múltiple, y en una etapa posterior el halógeno sale como ion haluro. Se trata de un mecanismo de “adición-eliminación”, del cual tendremos más ejemplos más adelante:

Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


