23.8: Aminas como ácidos
- Page ID
- 72564
Las aminas primarias y secundarias son ácidos muy débiles. Las sales de litio de tales aminas se pueden preparar en solución de éter por tratamiento de la amina con fenillitio:
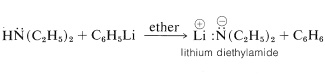
La sal de litio de\(\ce{N}\) -etiletanamina (dietilamina) se llama dietilamida de litio,\(^4\) pero esta nomenclatura puede generar confusión con compuestos del tipo\(\ce{RCO_2NH_2}\), que se derivan de ácidos carboxílicos y también se llaman amidas. Elegimos evitar usar el nombre “amida alcalina” para\(\ce{RN} \overset{\ominus}{\ce{H}} \overset{\oplus}{\ce{Li}}\) y en consecuencia nos referiremos a ellas como sales metálicas de la amina madre.
Las alcanaminas tienen fuerzas ácidas correspondientes a\(K_a\) valores de aproximadamente\(10^{-33}\), lo que significa que sus bases conjugadas son reactivos poderosamente básicos. Por lo tanto, son muy eficaces para provocar reacciones de eliminación por el\(E2\) mecanismo (Sección 8-8) y sustitución aromática por el mecanismo de arino (Sección 14-6C). El siguiente ejemplo ilustra esta propiedad en una síntesis útil de una bencenamina a partir de bromobenceno:
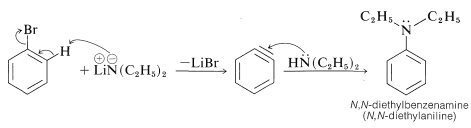
Las sales de alcanaminas también son útiles para generar sales enolatos de compuestos carbonílicos (Secciones 17-4A y\ (\ alfa\) Carbones de Derivados de Acidos Carboxílicos” href=” /Librerías/Química orgánica/libro:_básico_principios_de_químicaorgánica _ (Roberts_and_Caserio) /18:_carboxilic_ácidos_and_ Sus derivativos/18.09:_reacciones_en/ (/alpha/) _carbons_of_carboxilic_acid_derivados #18 -8c_alquilación_de_éster_aniones">18-8C).
\(^4\)El sistema utilizado aquí nombra a estas sales como productos de sustitución de\(\ce{NH_2^-}\). Claramente, dar\(\ce{LiN(C_2H_5)_2}\) el nombre “\(\ce{N}\)litio-etiletanamida” sería totalmente incorrecto porque\(\ce{N}\) -etiletanamida es\(\ce{CH_3CONHC_2H_5}\). Quizás un nombre mejor sería dietilazanida de litio o\(\ce{N}\),\(\ce{N}\) -dietilaminolitio.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


