27.6: Espectroscopia fotoelectrónica
- Page ID
- 73292
La excitación de electrones a estados de mayor energía a través de la absorción de luz visible y ultravioleta (generalmente cubriendo el rango de longitudes de onda de\(200 \: \text{nm}\) a\(780 \: \text{nm}\)) se discute en las Secciones 9-9 y 28-1. Ahora consideraremos lo que sucede en la absorción de fotones de longitud de onda mucho más corta, más energéticos.
Cuando la radiación de longitudes de onda del orden de\(120 \: \text{nm}\) es absorbida por una molécula de eteno, el estado excitado tiene apenas la energía suficiente (aproximadamente\(250 \: \text{kcal mol}^{-1}\)) para hacer que el electrón más flojamente unido sea expulsado. Con radiación de longitud de onda aún más corta, como la\(58.4 \: \text{nm}\)\(\left( 490 \: \text{kcal mol}^{-1} \right)\) proporcionada por un tubo de descarga de helio, estos electrones tendrán, por la ley de Einstein, una energía cinética de\(\left( 490 - 250 \right) = 240 \: \text{kcal mol}^{-1}\). Los electrones más estrechamente unidos también pueden ser expulsados por la\(58.4 \: \text{nm}\) radiación, y tendrán energías cinéticas\(E = h \nu - I\), en las que\(h \nu\) está la energía de la radiación absorbida\(\left( 490 \: \text{kcal mol}^{-1} \right)\) y\(I\) es la energía de ionización. Si conocemos\(h \nu\) y medimos el número de electrones expulsados en función de sus energías cinéticas, podemos derivar un espectro que muestre cómo la probabilidad de excitación se correlaciona con la energía de ionización. Dichos espectros, llamados espectros fotoelectrónicos, se muestran en la Figura 27-10 para eteno gaseoso, etino y benceno y son bastante individualistas. Se observa una estructura fina considerable como consecuencia de una considerable dispersión en los niveles vibracionales del estado excitado.
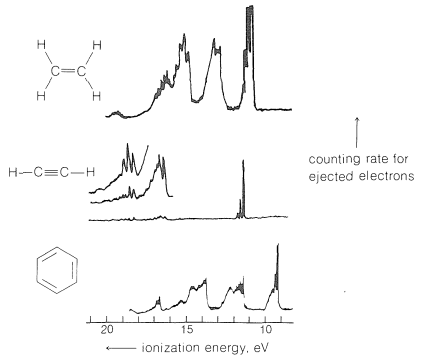
La sustitución y conjugación tienen efectos sustanciales sobre las energías de ionización. Hemos mencionado cómo los grupos metilo son capaces por su poder donador de electrones para estabilizar los cationes de carbono más que los hidrógenos (Sección 8-7B). El mismo efecto es muy prominente en la ionización de alquenos, siendo la energía más baja requerida para expulsar un electrón del 1-buteno aproximadamente\(11 \: \text{kcal mol}^{-1}\) mayor que la del cis - o trans -2-buteno. Las diferencias correspondientes para 1-hexeno y 2,3-dimetil-2-buteno son aproximadamente\(27 \: \text{kcal mol}^{-1}\). La conjugación produce efectos similares. La energía más baja requerida para expulsar un electrón de 1,4-pentadieno con dobles enlaces aislados es\(21 \: \text{kcal mol}^{-1}\) mayor que para el 1,3-pentadieno isomérico con dobles enlaces conjugados.
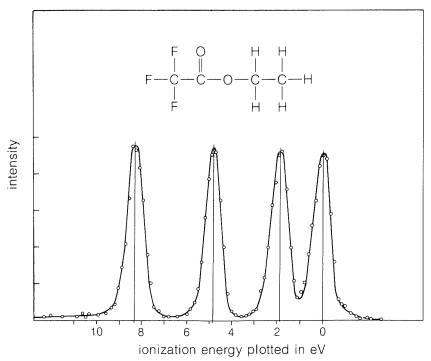
La espectroscopia fotoelectrónica también se puede llevar a cabo con rayos x como fuente de excitación y en esta forma a menudo se llama “ESCA” (Electron Spectroscopy for Chemical Analysis). Los rayos x utilizados tienen longitudes de onda del orden de\(0.9 \: \text{nm}\)\(\left( 32,000 \: \text{kcal mol}^{-1} \right)\) y las energías involucradas son más que amplias para causar la expulsión de electrones tanto de conchas internas como de conchas de valencia. En la Figura 27-11 se muestra un espectro fotoelectrónico de rayos X de\(1s\) los electrones de carbono del trifluoroetanoato de etilo. Este espectro es extremadamente significativo ya que muestra cuatro picos diferentes, uno por cada carbono químicamente diferente presente. Lo que esto significa es que la energía requerida para expulsar un\(1s\) electrón de carbono depende del estado químico del carbono. El rango de energía para este compuesto es completamente\(185 \: \text{kcal mol}^{-1}\) del aproximadamente\(6700 \: \text{kcal mol}^{-1}\) requerido para expulsar un\(1s\) electrón. Esta forma de espectroscopia es especialmente adecuada para el estudio de superficies sólidas y se está utilizando ampliamente para la caracterización de catalizadores sólidos.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


