27.10: Espectroscopia de Resonancia Electrón-Espín (ESR) de Radicales Orgánicos
- Page ID
- 73315
Un método importante para estudiar los radicales es la espectroscopia de resonancia electrón-espín (ESR). Los principios de esta forma de espectroscopia son muy parecidos a los de la espectroscopia de RMN, pero el lenguaje utilizado por los practicantes de estas dos formas de espectroscopia de resonancia magnética es diferente.
Primero, hablemos de las similitudes. El punto importante es que un electrón desapareado, como un protón, tiene un giro y un momento magnético tal que tiene dos posibles orientaciones en un campo magnético. Las dos orientaciones corresponden a números cuánticos magnéticos\(+\frac{1}{2}\) y\(-\frac{1}{2}\) que definen dos estados de energía. Estos estados difieren en energía por\(\Delta E = \left( h \gamma \right) H\), en la que\(\gamma\) se encuentra la relación giromagnética del electrón. (Véase la Sección 9-10A para una discusión de la situación análoga para los protones.) Las transiciones entre estos estados ocurren con absorción de radiación de frecuencia\(\nu = \gamma H\). Debido a que\(\gamma\) para los electrones libres es aproximadamente 1000 veces mayor que\(\gamma\) para los protones, la frecuencia\(nu\) de absorción de electrones es aproximadamente 1000 veces la de los protones en el mismo campo magnético. En campos magnéticos de 3600 gauss la frecuencia de absorción de electrones libres es aproximadamente\(10,000 \: \text{MHz}\), que cae en el microondas, más que en la región de ondas de radio.
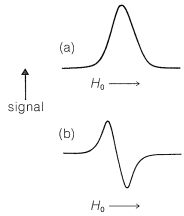
El aparato básico para espectroscopía ESR es similar al que se muestra en la Figura 9-22 para espectroscopía de RMN, excepto que la muestra se irradia con un generador de microondas. Los espectros producidos por las absorciones ESR de electrones desapareados son similares a los mostrados en la Figura 9-25, excepto que los espectrómetros ESR normalmente están dispuestos de manera que produzcan una gráfica de la primera derivada de la curva de absorción contra el campo magnético en lugar de la propia curva de absorción, como se muestra en la Figura 27-17. Esta disposición se utiliza porque da una mejor relación señal-ruido que una simple gráfica de absorción contra campo magnético.
La sensibilidad de la espectroscopia ESR para la detección de radicales es muy alta. En condiciones favorables, una concentración de radicales tan baja como se\(10^{-12} \: \text{M}\) puede detectar fácilmente. La identificación de radicales hidrocarburo simples a menudo es posible mediante el análisis de la estructura fina en sus espectros, que surge de las divisiones espín-espín que involucran a aquellos protones que están razonablemente cerca de los centros sobre los que se distribuye el electrón desapareado. Los radicales metilo,\(\ce{CH_3} \cdot\), generados por bombardeo de rayos X de yoduro de metilo\(-196^\text{o}\) muestran cuatro líneas de resonancia de intensidad 1:3:3:1, como se esperaba para la interacción del electrón con\(n + 1\) protones (ver Sección 9-10G).
El desplazamiento químico generalmente es mucho menos importante en la espectroscopia ESR que en la RMN. Una razón es que los tiempos de vida de los electrones en los\(-\frac{1}{2}\) estados\(+\frac{1}{2}\) y generalmente son muy cortos (\(10^{-6} \: \text{sec}\)o menos) por lo que las líneas ESR son bastante amplias en comparación con las líneas de RMN (Sección 27-1). Los desplazamientos químicos de ESR generalmente se miden en términos de "\(g\)factores”, que, al igual que\(\delta\) los valores de RMN, son independientes del campo. La frecuencia de resonancia viene dada por\(\nu = g \mu_0 H_0/h\), en la que\(\mu_0\) se encuentra el momento magnético del electrón.
Las divisiones de espín-espín que surgen de las interacciones protón-electrón son muy grandes en los espectros de ESR y generalmente se reportan en gauss, bajo el título interacciones hiperfinas. La división protón-electrón en el radical metilo es de 23 gauss\(\left( 64.4 \: \text{MHz} \right)\), que es mucho mayor que la división\(7\) -\(\text{Hz}\) protón-protón en etanol (Figura 9-23). Las grandes divisiones (y líneas anchas) típicas de la ESR permiten ejecutar espectros de ESR en sólidos o materiales altamente viscosos, para lo cual la estructura fina típica de los espectros de RMN de alta resolución sería completamente lavada (Sección 27-1).
Los espectros de ESR están sujetos a efectos de intercambio de la misma manera que los espectros de RMN. Un ejemplo específico es proporcionado por el intercambio electrónico entre naftalenuro de sodio y naftaleno. La naftalina tiene un conjunto\(\pi\) de diez orbitales moleculares, similares a los seis orbitales\(\pi\) moleculares del benceno (Figura 21-5). Los diez\(\pi\) electrones de naftaleno llenan los cinco inferiores de estos orbitales. En un disolvente tal como 1,2-dimetoxietano, que solvata bien iones metálicos pequeños, el naftaleno acepta un electrón de un átomo de sodio y forma naftalenuro de sodio, un anión radical:
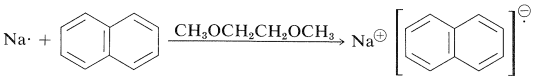
El electrón adicional entra en el orbital molecular desocupado más bajo del naftaleno, lo que significa que el electrón circula por todos los carbonos. La resonancia electrónica se divide en un total de 25 líneas por interacciones magnéticas electrón-protón. El motivo de la compleja división se puede entender si observamos que hay ocho protones en dos series de cuatro. Un conjunto escupe la señal electrónica en cinco líneas\(\left( n + 1 \right)\) de intensidad 1:4:6:4:1 con un espaciado de 5.0 gauss, mientras que el segundo conjunto divide cada una de las cinco líneas en otro quinteto 1:4:6:4:1 con un espaciado de 1.9 gauss. Entonces, en total, hay veinticinco líneas, cinco conjuntos de cinco.
Si se agrega un exceso de naftaleno a una solución de naftalenuro de sodio, se produce un intercambio intermolecular de electrones:
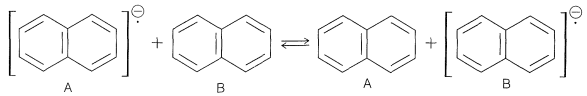
Esto significa que el electrón va de naftaleno A con un conjunto particular de núcleos de\(+\frac{1}{2}, -\frac{1}{2}\) protones a naftaleno B con un conjunto diferente. El resultado es que las líneas se amplían y, si el intercambio es muy rápido, la división se desvanece. Debido a que el área de divisiones combate 5 gauss\(\left( 14 \: \text{MHz} \right)\), la vida media antes del intercambio tiene que ser aproximadamente\(10^{-8} \: \text{sec}\) o menos para oscurecer la división (ver Secciones 27-1 y 27-2).
Las aplicaciones más emocionantes de la ESR están en el estudio de intermedios radicales en reacciones orgánicas. Se ha hecho un uso considerable de la técnica en reacciones bioquímicas y se ha demostrado que se generan radicales y se descomponen en las oxidaciones provocadas por las enzimas. También se han detectado radicales mediante mediciones de ESR en algas que “fijan” el dióxido de carbono en la fotosíntesis. Se ha encontrado que el carácter de los radicales formados depende de la longitud de onda de la luz suministrada para la fotosíntesis.
Colaboradores y Atribuciones
- John D. Robert and Marjorie C. Caserio (1977) Basic Principles of Organic Chemistry, second edition. W. A. Benjamin, Inc. , Menlo Park, CA. ISBN 0-8053-8329-8. This content is copyrighted under the following conditions, "You are granted permission for individual, educational, research and non-commercial reproduction, distribution, display and performance of this work in any format."


