1.2: Carboxiloides cíclicos
- Page ID
- 71916
El desarrollo de nylon de Carrothers en Du Pont condujo indirectamente a un polímero muy similar que se hizo de una manera muy diferente. Al otro lado del Océano Atlántico, Paul Schlack en IG Farben en Alemania buscaba una manera de hacer un material similar que no estaría sujeto a la patente de Du Pont. Sus esfuerzos llevaron a un material llamado perlon, a veces referido como nylon 6.
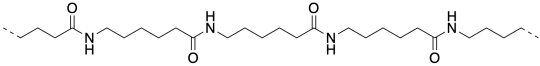
El Nylon 6 no es un copolímero alterno como el nylon 66. Es sólo un polímero. Y no está hecho de un monómero difuncional como el nylon 66 o proteínas. En cambio, está hecho de una amida cíclica, a veces llamada lactama. Para polimerizar, la lactama tiene que abrirse en una forma lineal, y los monómeros de lactama terminan encadenados cabeza a cola. Este proceso se llama polimerización por apertura de anillo.
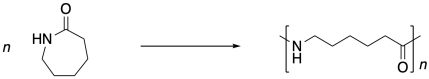
Hay una serie de cosas que son diferentes en estas dos formas de hacer nylon. Una de ellas enciende todo el concepto de síntesis. La síntesis es el acto de hacer las cosas. Es un poco como cocinar. Reúne los ingredientes. Toma la cantidad correcta de esto y la cantidad correcta de eso. Los mezclas y obtienes algo maravilloso. Pero esa es la diferencia aquí: al hacer el nylon 66, Carrothers mezcló dos compuestos diferentes juntos. Vertió un compuesto de una botella y otro compuesto de otra botella. Los mezcló y consiguió un polímero.
En contraste, Schlack no mezcló nada, al menos por lo que hemos visto hasta ahora. Todo salió de una botella. Entonces, ¿por qué no estaba ya nylon 6 en la botella? Si los monómeros solo reaccionan consigo mismos, ¿no podrían haber seguido adelante y hecho eso en la botella?
La polimerización por apertura de anillo, al menos en este contexto, es un ejemplo de una reacción en cadena. Las reacciones en cadena no solo ocurren por sí mismas; necesitan un arranque rápido.
Para entender por qué, hay que apreciar que estos dos materiales provienen a través de dos clases muy diferentes de reacciones de polimerización. El Nylon 66 es el producto de una reacción de condensación. Se mezcla una amina con un ácido carboxílico, se libera agua y se forma un enlace amida. Incluso si el par de reactivos se elige para que sea más eficiente sintéticamente —digamos, una amina y un cloruro de ácido en lugar de un ácido carboxílico— todavía resulta una reacción de condensación, en este caso liberando cloruro de hidrógeno.
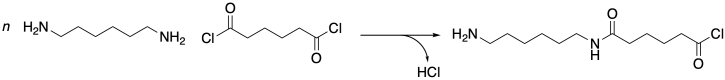
El Nylon 6, por otro lado, no es producto de una reacción de condensación — al menos a primera vista. Observe cuidadosamente el monómero y el polímero. Contar los átomos. No falta nada. No se liberó ninguna molécula de agua ni cloruro de hidrógeno ni nada más. El nitrógeno en un extremo de la cadena simplemente se une al carbonilo del siguiente.
Pero si caminas hasta el final de esa cadena, hasta llegar al último carbonilo, ¿qué encuentras ahí? No hay nitrógeno unido. Ese nitrógeno era el nucleófilo que se unía al carbonilo en el siguiente monómero. Tiene que haber algo, sin embargo, porque el carbono no puede estar ahí sentado con sólo tres lazos. Entonces debió haber habido algún nucleófilo que se sumó a ese carbonilo, soltando la amina que se añadió al siguiente carbonilo, brotando la siguiente amina, y así sucesivamente. Tenía que haber un nucleófilo original.
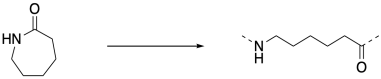
Este es el salto inicial que necesitaba la reacción en cadena. Se tuvo que agregar un nucleófilo para poner las cosas en marcha. Una vez que reaccionó con el primer monómero, la amina se convirtió en el nucleófilo para el siguiente monómero, y esa apertura de anillo produjo otro nucleófilo de amina, y así sucesivamente. Debido a que siempre se produce un nuevo nucleófilo cuando se abre el siguiente anillo, la reacción simplemente sigue adelante. Ese primer nucleófilo, el que empezó todo, se llama iniciador. La necesidad de un iniciador es un sello distintivo de las reacciones en cadena.
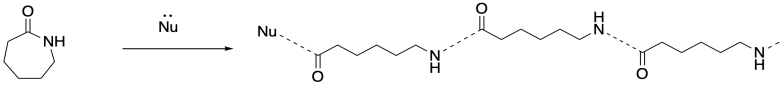
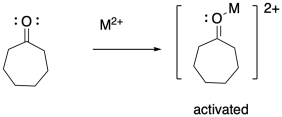
Además del iniciador, las polimerizaciones por apertura de anillo emplean frecuentemente catalizadores para acelerar la reacción, al igual que en algunas polimerizaciones por condensación. El catalizador puede ser un ácido de Lewis que activa el carbonilo o un “organocatalizador” que hace lo mismo a través de enlaces de hidrógeno. Ambos enfoques catalíticos también pueden hacer uso de catálisis nucleofílica. En ese caso, la nucleofilia del nucleófilo puede mejorarse, o bien un nucleófilo temporal puede agregarse al carbonilo hasta que sea reemplazado por el grupo nucleófilo dando como resultado el encadenamiento.
También se pueden preparar otras poliamidas mediante amidas cíclicas de apertura de anillo. El mismo enfoque también se utiliza para preparar poliésteres a partir de ésteres cíclicos, también llamados lactonas. En ese caso, la reacción a veces se denomina polimerización de transesterificación por apertura de anillo, o ROTEP para abreviar.

