4.4: Conformaciones de Butano
- Page ID
- 76393
Objetivo de aprendizaje
- interpretar y dibujar la rotación alrededor de un enlace sencillo carbono-carbono usando proyecciones Newman y estructuras de caballete
- correlacionar energías de conformaciones con diagramas de energía rotacional y predecir las conformaciones más estables para butano
Conformaciones de butano
Ahora consideremos el butano, con su cadena de cuatro carbonos. Ahora hay tres enlaces giratorios carbono-carbono a considerar, pero nos centraremos en el enlace medio entre C 2 y C 3. A continuación se presentan dos representaciones de butano en una conformación que pone a los dos grupos CH 3 (C1 y C 4) en la posición eclipsada, con los dos enlaces C-C en un ángulo diedro de 0 o.
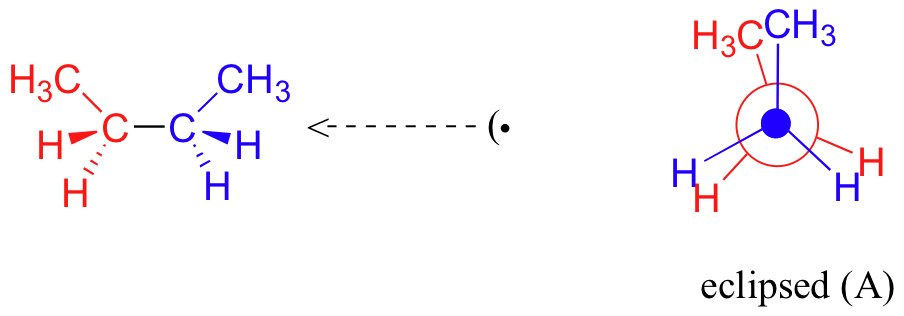
Si giramos el carbono frontal, (azul) 60° en el sentido de las agujas del reloj, la molécula de butano se encuentra ahora en una conformación escalonada.
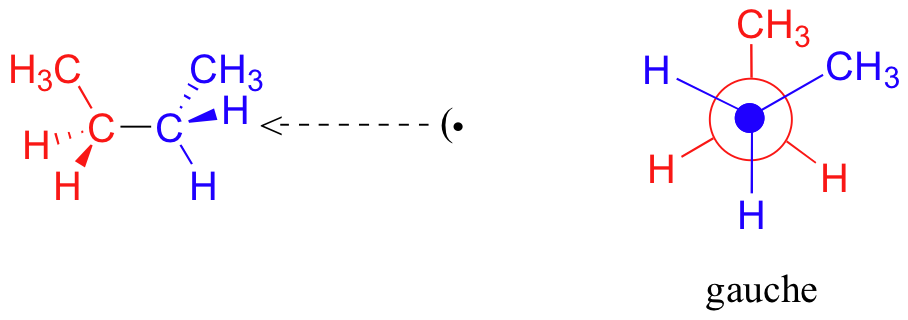
Esto se conoce más específicamente como la conformación gauche del butano. Observe que aunque están escalonados, los dos grupos metilo no están tan separados como podrían estar.
Una rotación adicional de 60° nos da una segunda conformación eclipsada (B) en la que ambos grupos metilo se alinean con átomos de hidrógeno.
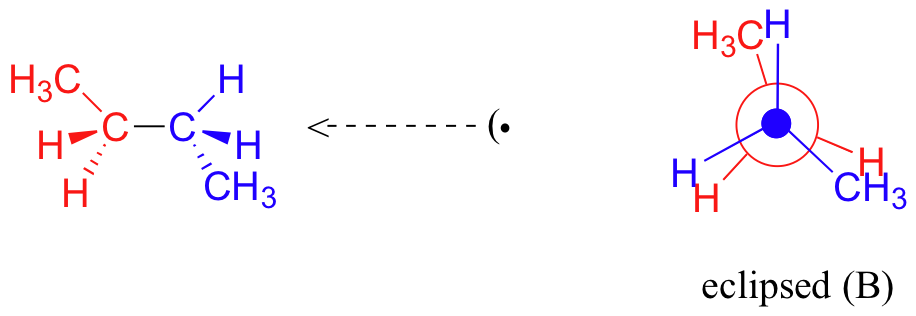
Una rotación más de 60 produce otra conformación escalonada llamada anti conformación, donde los dos grupos metilo se posicionan uno frente al otro (un ángulo diedro de 180 o).
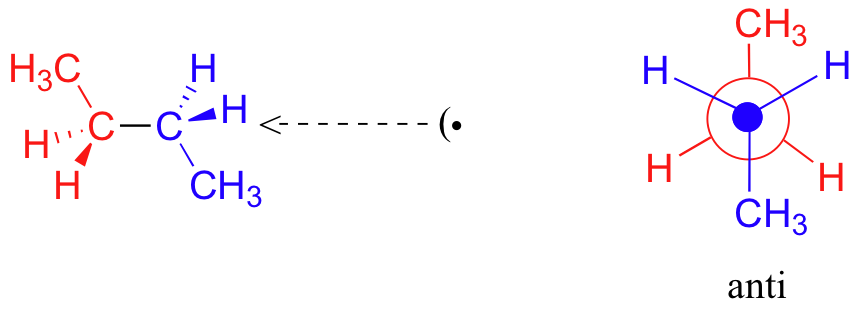
Al igual que con el etano, las conformaciones escalonadas del butano son “valles” energéticos, y las conformaciones eclipsadas son “picos” energéticos. Sin embargo, en el caso del butano hay dos valles diferentes, y dos picos diferentes. La conformación gauche es un valle de energía mayor que la anti conformación debido a la deformación estérica, que es la interacción repulsiva causada por los dos grupos metilo voluminosos que se ven forzados demasiado cerca entre sí. Claramente, la deformación estérica es menor en la anti conformación. De la misma manera, la cepa estérica provoca que la conformación A eclipsada -donde los dos grupos metilo están lo más cercanos que pueden estar- sea mayor en energía que las dos conformaciones B eclipsadas.
El siguiente diagrama resume las energías relativas para las diversas conformaciones eclipsadas, escalonadas y gauches.
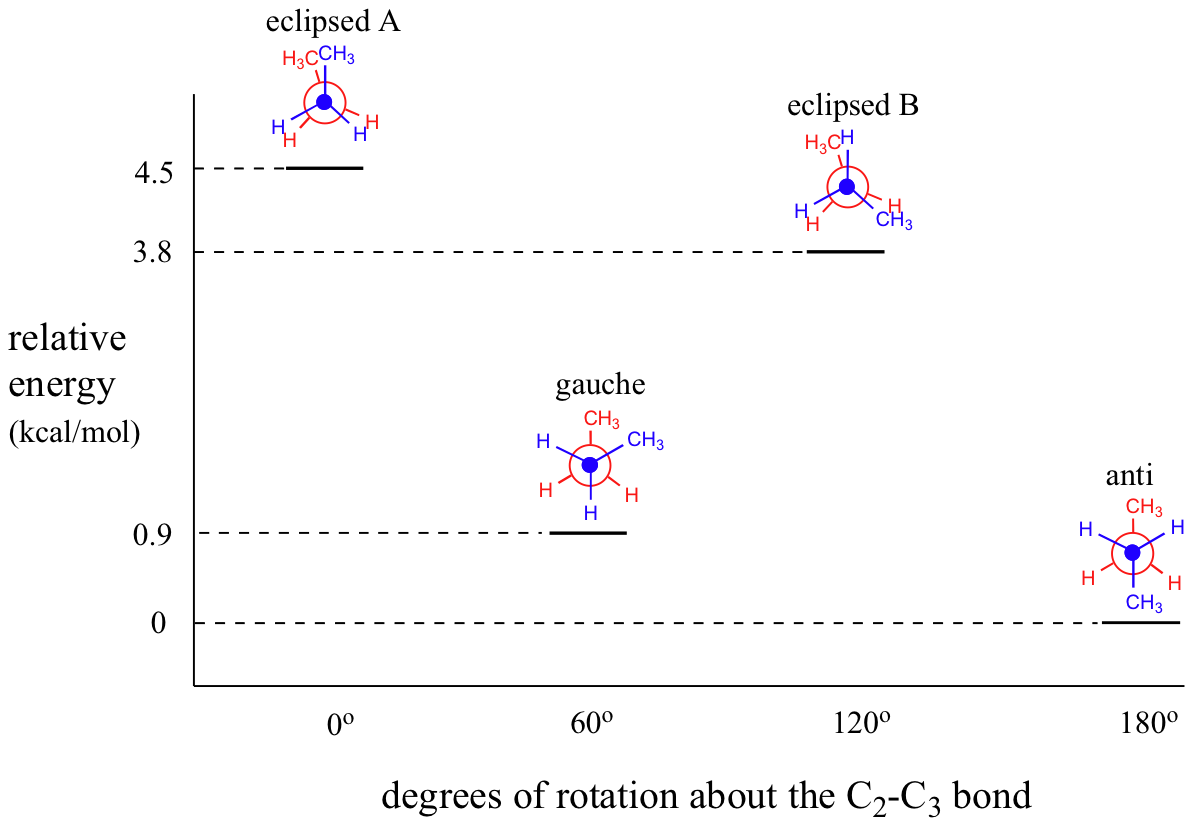
El siguiente diagrama ilustra el cambio en la energía potencial que ocurre con la rotación alrededor del enlace C2-C3 en incrementos rotacionales más pequeños.
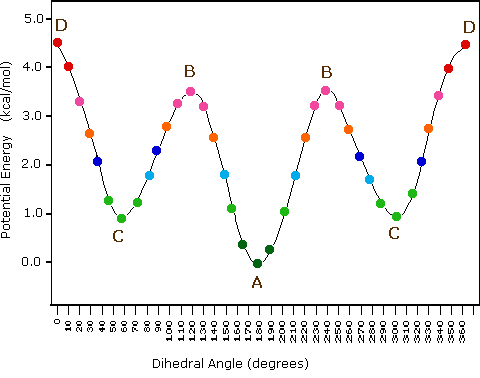
Curva de potencial vs ángulo diedro del enlace C 2 -C 3 de butano.
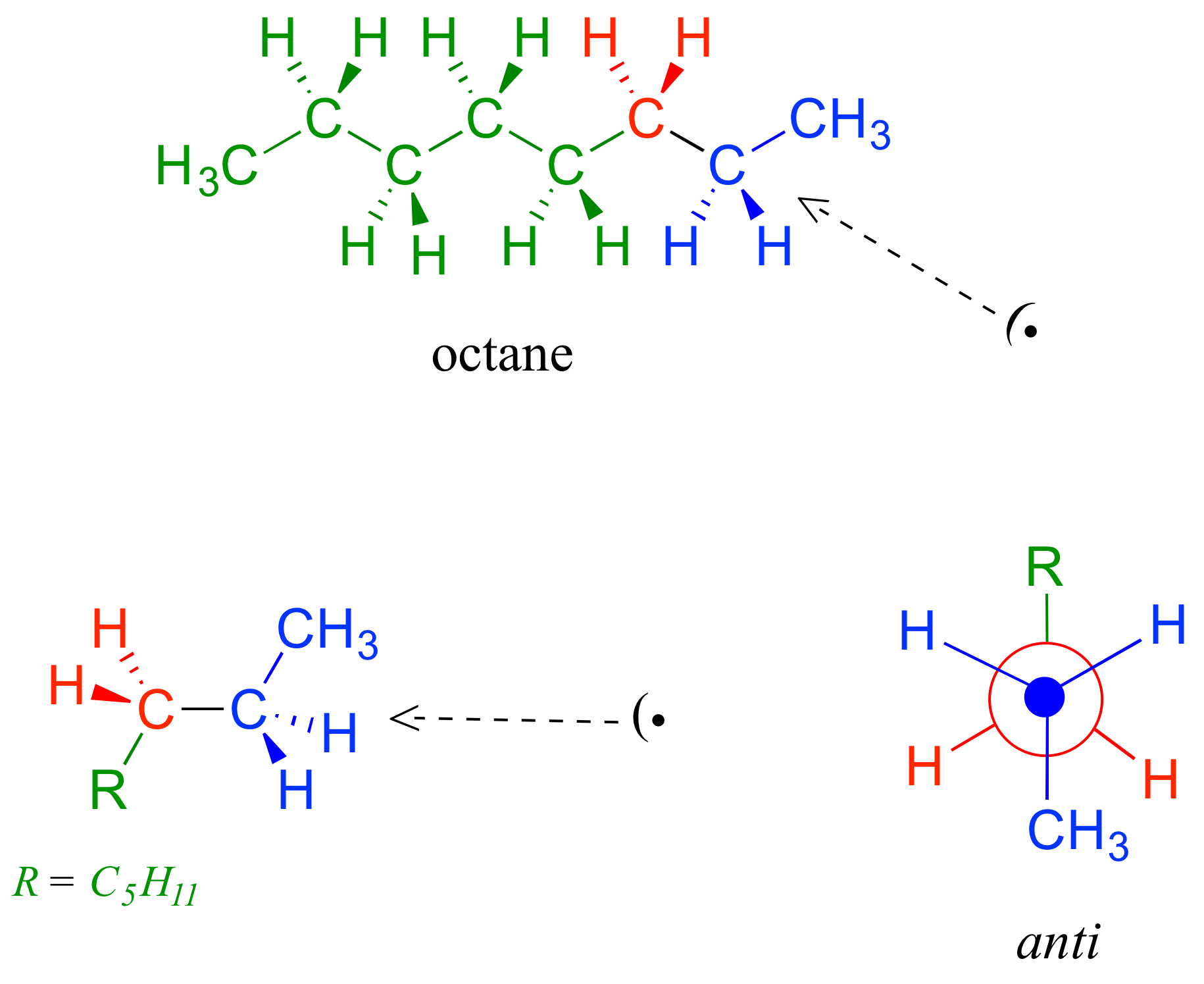
Debido a que la anti conformación (escalonada) es la más baja en energía (y también simplemente para facilitar el estirado), es convencional dibujar alcanos de cadena abierta en forma de 'zigzag', lo que implica anti conformación en todos los enlaces carbono-carbono. La siguiente figura muestra, como ejemplo, una proyección de Newman mirando hacia abajo el enlace C2-C3 de octano.