7.3: Preparación de haluros de alquilo
- Page ID
- 76207
Objetivo de aprendizaje
- especificar los reactivos para la síntesis más eficiente de haluros de alquilo mediante halogenación por radicales libres de alcanos (Capítulo 5) o halogenación alínica de alquenos con NBS
Halogenación por radicales libres de alcanos
La halogenación por radicales libres de alcanos es la sustitución de un solo hidrógeno en el alcano por un solo halógeno para formar un haloalcano. Se requiere luz para iniciar la formación de radicales y es un buen ejemplo de una reacción fotoquímica. El ejemplo más simple se muestra a continuación para el metano que reacciona con cloro en presencia de luz para formar clorometano y cloruro de hidrógeno gaseoso.
\[\ce{CH4 + Cl2 + energy → CH3Cl + HCl}\]
La halogenación por radicales libres de alcanos se ha explicado a fondo en el capítulo 5. Se evalúa la estructura del alcano para elegir entre la alta reactividad del cloro (Cl 2) y la alta selectividad del bromo (Br 2).

Bromación alílica
Cuando los halógenos están en presencia de moléculas insaturadas como los alquenos, la reacción esperada es la adición a los carbonos de doble enlace dando como resultado un dihaluro vecinal (halógenos en carbonos adyacentes). La reacción se estudia en un capítulo posterior. Para evitar reacciones halógenas en el alqueno, la concentración de halógeno se mantiene lo suficientemente baja como para que se produzca una reacción de sustitución en la posición alínica en lugar de la adición en el doble enlace. El producto es un haluro alílico (halógeno sobre carbono junto a los carbonos de doble enlace), que se adquiere a través de un mecanismo de cadena radical.
![]()
¿Por qué Sustitución de Hidrógenos Alílicos?
Como muestra la siguiente tabla, la energía de disociación para el enlace alílico C-H es menor que las energías de disociación para los enlaces C-H en las posiciones vinílica y alquílica. Esto se debe a que el radical formado cuando se elimina el hidrógeno alílico se estabiliza por resonancia. Por lo tanto, dado que la concentración de halógeno es baja, la sustitución en la posición alílica se ve favorecida sobre las reacciones competidoras. Sin embargo, cuando la concentración de halógeno es alta, se favorece la adición en el doble enlace porque una reacción polar compite con la reacción en cadena del radical.
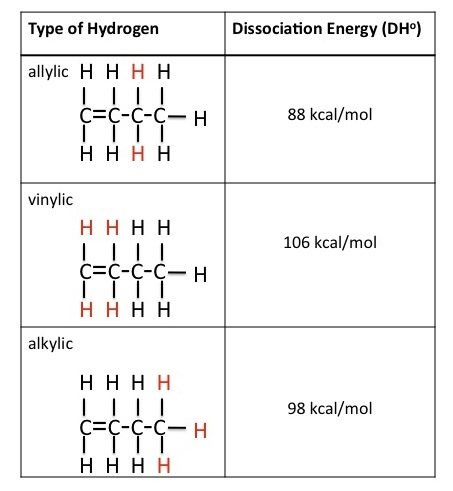
Bromación Alílica Radical usando NBS y luz
Preparación de Bromo (baja concentración)
La NBS (N-bromosuccinimida) es el reactivo más utilizado para producir bajas concentraciones de bromo. Cuando se suspende en tetracloruro (CCl 4), el NBS reacciona con trazas de HBr para producir una concentración suficientemente baja de bromo para facilitar la reacción de bromación alílica.
.jpg)
Mecanismo de bromación alílico
Paso 1: Iniciación
Una vez que la etapa de preiniciación que involucra NBS produce pequeñas cantidades de Br 2, las moléculas de bromo se escinden homolíticamente por la luz para producir radicales de bromo.
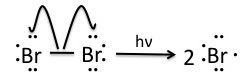
Paso 2: Propagación
Un radical bromo producido por escisión homolítica en la etapa de inicio elimina un hidrógeno alílico de la molécula de alqueno. Se genera un intermedio radical, el cual se estabiliza por resonancia. La estabilidad proporcionada por la deslocalización del radical en el intermedio alqueno es la razón por la que la sustitución en la posición alílica se ve favorecida sobre las reacciones competitivas como la adición en el doble enlace.
.jpg)
El radical intermedio reacciona entonces con una molécula de Br 2 para generar el producto bromuro alílico y regenerar el radical bromo, lo que continúa con el mecanismo de la cadena radical. Si el reactivo alqueno es asimétrico, se forman dos isómeros de producto distintos.
.jpg)
Paso 3: Terminación
El mecanismo de cadena radical de la bromación alílica puede ser terminado por cualquiera de los posibles pasos que se muestran a continuación.
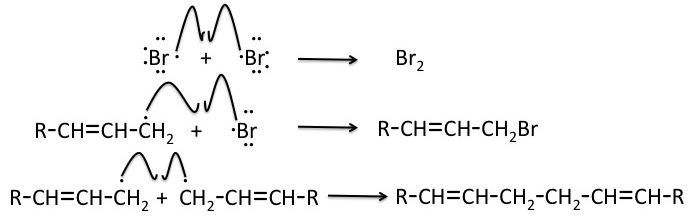
Cloración Alílica Radical
Al igual que la bromación, la cloración en la posición alínica de un alqueno se logra cuando se presentan bajas concentraciones de Cl 2. La reacción se lleva a cabo a altas temperaturas para lograr los resultados deseados.
Usos Industriales
La cloración alílica tiene importantes aplicaciones prácticas en la industria. Dado que el cloro es económico, las cloraciones alílicas de alquenos se han utilizado en la producción industrial de productos valiosos. Por ejemplo, el 3-cloropropeno, que es necesario para la síntesis de productos como la resina epoxi, se adquiere a través de la cloración alílica radical (se muestra a continuación).
![]()
Ejercicios
Ejercicios
- Predecir los dos productos de la reacción de cloración alílico del 1-hepteno.
- ¿Qué condiciones se requieren para que ocurra la halogenación alílica? ¿Por qué esta reacción supera a otras posibles reacciones como la adición cuando se cumplen estas condiciones?
- Predecir el producto de la reacción de bromación alílica del 2-fenilheptano. (Pista: ¿Cómo son los hidrógenos bencílicos similares a los hidrógenos alílicos?)
- El reactivo 5-metil-1-hexeno genera los productos 3-bromo-5-metil-1-hexeno y 1-bromo-5-metil-2-hexeno. ¿Qué reactivos se utilizaron en esta reacción?

- Predecir los productos de las siguientes reacciones:

- Soluciones
-
1. 3-cloro-1-hepteno y 1-cloro-2-hepteno
2. Una baja concentración de radical haluro es suficiente para la reacción en el carbono alílico sin crear un ambiente de reactividad para el enlace pi del alqueno.
3. 2-bromo-2-fenilheptano
4. NBS con luz
5. El producto (A) es un halógeno 1° el cual es un producto más estable aunque el (B) tuviera un mejor estado de transición con un radical 2°.

6.
.png)
Referencias
- Djerassi, Carl. “Bromaciones con N-Bromosuccinimida y Compuestos Relacionados - La Reacción Wohl-Ziegler”. Química Orgánica y Biomolecular (2003). RSC Publishing. 9 de junio de 2003. Real Sociedad de Química. 25 feb. 2009.
- Kent, Doug. Bromación Alílica. Taller Chem 118B. Centro de Habilidades de Aprendizaje. 3 feb. 2009.
- Li, Chao-Jun y Tak-Hang Chan. Química Orgánica: Estructura y Función. 5ta ed. Nueva York: W.H. Freeman and Company, 2007.
Colaboradores y Atribuciones
- Sharon Wei (UCD), Liza Chu (UCD)
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)

