7.7: Estereoquímica de la reacción SN2
- Page ID
- 76266
Objetivo de aprendizaje
- predecir los productos y especificar los reactivos para reacciones de S N 2 con estereoquímica
- proponer mecanismos para reacciones de S N 2
- dibujar e interpretar Diagramas de Energía de Reacción para S N 2reactions
Las reacciones de S N 2 son estereoespecíficas
La reacción de S N 2 es estereoespecífica como otras reacciones concertadas. Una reacción estereoespecífica es aquella en la que reaccionan diferentes estereoisómeros para dar diferentes estereoisómeros del producto. El nuclefilo y el electrófilo deben estar correctamente orientados para que se produzca el solapamiento orbital y desencadene la reactividad química. Las observaciones experimentales muestran que todas las reacciones de S N 2 proceden con inversión de configuración; es decir, el nucleófilo siempre penetrará desde la parte posterior en reacciones de S N 2. Para pensar por qué esto podría ser cierto, recuerde que el nucleófilo tiene un par solitario de electrones para ser compartidos con el centro de carbono electrófilo y el grupo de salida va a llevar consigo un par solitario de electrones al salir. Porque como cargas se repelen entre sí, el nucleófilo siempre procederá por un mecanismo de desplazamiento trasero.
- Orientación Frontal: En una orientación de frente, el nucleófilo se acerca al centro electrófilo en el mismo lado que el grupo de salida. Con orientación de frente, la estereoquímica del producto sigue siendo la misma; es decir, tenemos retención de configuración.
- Orientación posterior: En una orientación posterior, el nucleófilo se acerca al centro electrófilo en el lado opuesto al grupo de salida. Con orientación trasera, la estereoquímica del producto no permanece igual. Hay inversión de configuración.
Por ejemplo, si el sustrato es un enantiómero R, una orientación nucleofílica de frente da como resultado la retención de la configuración y la formación del enantiómero R. Una orientación nucleofílica posterior da como resultado la inversión de la configuración y la formación del enantiómero S.
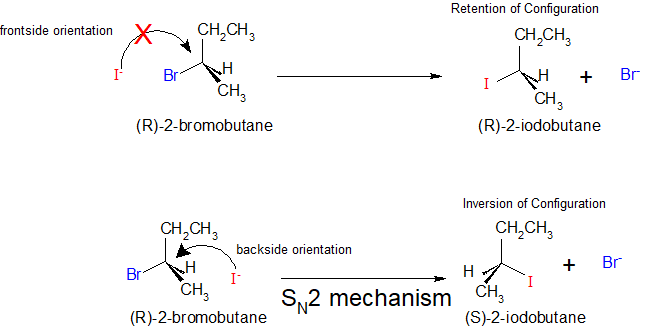
Por el contrario, si el sustrato es un enantiómero S, una orientación nucleofílica del frente da como resultado la retención de la configuración y la formación del enantiómero S. Una orientación nucleofílica posterior da como resultado la inversión de la configuración y la formación del enantiómero R.

Empíricamente, las reacciones de S N 2 que comienzan con el enantiómero R como sustrato formarán el enantiómero S como producto. Aquellos que comiencen con el enantiómero S como sustrato formarán el enantiómero R como producto. Este concepto de retención e inversión de configuración también se puede aplicar a sustratos que pueden existir como isómeros geométricos (cis y trans). Si la configuración cis es el sustrato, el producto resultante será trans. Por el contrario, si la configuración trans es el sustrato, el producto resultante será cis.
Ejercicio
1. Predecir el producto de una sustitución nucleofílica de (S) -2-bromopentano reaccionando con CH 3 CO 2 -, Mostrar estereoquímica.
Responder
-
1.

Colaboradores y Atribuciones
- Curtis raqueal (UCD)

