7.19: Comparación de reacciones de sustitución y eliminación
- Page ID
- 76256
Objetivo de aprendizaje
- predecir los productos y especificar los reactivos para las reacciones S N 1, S N 2, E1 y E2 con estereoquímica
- proponer mecanismos para reacciones S N 1, S N 2, E1 y E2
- dibujar, interpretar y aplicar Diagramas de Energía de Reacción para reacciones S N 1, S N 2, E1 y E2
Resumen de Reaction Patterns
Habiendo discutido los muchos factores que influyen en las reacciones de sustitución nucleofílica y eliminación de haluros de alquilo, ahora debemos considerar el problema práctico de predecir el resultado más probable cuando un haluro de alquilo dado reacciona con un nucleófilo dado. Como señalamos anteriormente, se deben considerar varias variables, siendo la más importante la estructura del grupo alquilo y la naturaleza del reactivo nucleófilo.En general, para que se produzca una reacción de S N 1 o E1, el intermedio carbocatiónico relevante debe ser relativamente estable. Los nucleófilos fuertes favorecen la sustitución, y las bases fuertes, especialmente las bases impedidas fuertes (como el terc-butóxido) favorecen la eliminación.
La naturaleza del sustituyente halógeno en el haluro de alquilo no suele ser muy significativa si es Cl, Br o I. En los casos en que compiten ambas reacciones de S N 2 y E2, los cloruros generalmente dan más eliminación que los yoduros, ya que la mayor electronegatividad del cloro aumenta la acidez del beta- hidrógenos. En efecto, aunque los fluoruros de alquilo son relativamente poco reactivos, cuando las reacciones con nucleófilos básicos son forzadas, se produce la eliminación (nótese la alta electronegatividad del flúor).
En la siguiente tabla se resume el resultado esperado de las reacciones de haluro de alquilo con nucleófilos. Se supone que los haluros de alquilo tienen uno o más beta-hidrógenos, haciendo posible la eliminación; y que se utilizan disolventes dieléctricos bajos (por ejemplo, acetona, etanol, tetrahidrofurano y acetato de etilo). Cuando un disolvente dieléctrico alto influiría significativamente en la reacción esto se nota en rojo. Tenga en cuenta que los halógenos unidos a átomos de carbono hibridados sp 2 o sp normalmente no experimentan reacciones de sustitución o eliminación con reactivos nucleofílicos.
|
Nucleófilo |
Nucleófilos aniónicos |
Nucleófilos aniónicos |
Nucleófilos Neutros |
|---|---|---|---|
| Grupo alquilo | |||
RCH primario 2 — |
Sustitución rápida S N 2. La tasa puede ser reducida por sustitución de β-carbonos, como en el caso del neopentilo. | Sustitución rápida S N 2. También puede ocurrir la eliminación de E2. ej., ClCH 2 CH 2 Cl + KOH —— > CH 2 =CHCl |
S N 2 sustitución. (N ≈ S >>O) |
| Secundaria R 2 CH— |
S N 2 sustitución y/o eliminación E2 (dependiendo de la basicidad del nucleófilo). Las bases más débiles que el acetato (pK a = 4.8) dan menos eliminación. La tasa de sustitución se puede reducir por ramificación en los β-carbonos, y esto incrementará la eliminación. | Dominará la eliminación E2. | S N 2 sustitución. (N ≈ S >>O) En disolventes ionizantes de alto dieléctrico, como agua, dimetilsulfóxido y acetonitrilo, los productos S N 1 y E1 pueden formarse lentamente. |
| Terciario R 3 C— |
La eliminación de E2 dominará con la mayoría de los nucleófilos (aunque sean bases débiles). No hay sustitución de S N 2 por impedimento estérico. En solventes ionizantes de alto dieléctrico, como agua, dimetilsulfóxido y acetonitrilo, se pueden esperar productos S N 1 y E1. | Dominará la eliminación E2. No se producirá ninguna sustitución de S N 2. En disolventes ionizantes de alto dieléctrico se pueden formar productos S N 1 y E1. | Eliminación E2 con nucleófilos nitrogenados (son bases). Sin sustitución S N 2. En disolventes ionizantes de alto dieléctrico se pueden formar productos S N 1 y E1. |
| Alilo H 2 C=CHCH 2 — |
Sustitución rápida S N 2 por los halogenuros 1º y 2º-. Para los haluros 3º-una sustitución S N 2 muy lenta o, si el nucleófilo es moderadamente básico, eliminación de E2. En disolventes ionizantes de alto dieléctrico, como agua, dimetilsulfóxido y acetonitrilo, se pueden observar productos S N 1 y E1. | Sustitución rápida S N 2 por 1º halogenuros. La eliminación E2 competirá con la sustitución en haluros 2º-, y dominará en el caso de los haluros 3º-. En disolventes ionizantes de alto dieléctrico se pueden formar productos S N 1 y E1. | Los nucleófilos de nitrógeno y azufre darán sustitución S N 2 en el caso de los haluros 1º y 2º. los haluros 3º-probablemente darán eliminación E2 con nucleófilos de nitrógeno (son bases). En disolventes ionizantes de alto dieléctrico se pueden formar productos S N 1 y E1. La hidrólisis del agua será favorable para los halogenuros de 2º y 3º. |
| Bencilo C 6 H 5 CH 2 — |
Sustitución rápida S N 2 por los halogenuros 1º y 2º-. Para los haluros 3º-una sustitución S N 2 muy lenta o, si el nucleófilo es moderadamente básico, eliminación de E2. En disolventes ionizantes de alto dieléctrico, como agua, dimetilsulfóxido y acetonitrilo, se pueden observar productos S N 1 y E1. | Sustitución rápida de S N 2 por 1º haluros (tenga en cuenta que no hay β hidrógenos). La eliminación E2 competirá con la sustitución en haluros 2º-, y dominará en el caso de los haluros 3º-. En disolventes ionizantes de alto dieléctrico se pueden formar productos S N 1 y E1. | Los nucleófilos de nitrógeno y azufre darán sustitución S N 2 en el caso de los haluros 1º y 2º. los haluros 3º-probablemente darán eliminación E2 con nucleófilos de nitrógeno (son bases). En disolventes ionizantes de alto dieléctrico se pueden formar productos S N 1 y E1. La hidrólisis del agua será favorable para los halogenuros de 2º y 3º. |
Observaciones Experimentales
Se reportan observaciones experimentales para las siguientes reacciones. Estas reacciones incluyen una gama de estructuras de haluro de alquilo en una variedad de condiciones de reacción para ilustrar los patrones de reacción resumidos anteriormente. Al describirlos, es útil designar el carbono portador de halógeno como alfa y el átomo o átomos de carbono adyacentes a éste como beta, como se señala en las cuatro primeras ecuaciones que se muestran a continuación. La sustitución o sustitución del halógeno en el α-carbono (color granate) por un reactivo nucleofílico es una reacción comúnmente observada, como se muestra en las ecuaciones 1, 2, 5, 6 y 7 siguientes. Además, dado que el carácter electrófilo introducido por el halógeno se extiende a los β-carbonos, y dado que los nucleófilos también son bases, también se debe considerar la posibilidad de eliminación H-X inducida por bases, como lo ilustra la ecuación 3. Finalmente, existen algunas combinaciones de haluros de alquilo y nucleófilos que no logran mostrar ninguna reacción en un periodo de 24 horas, como el ejemplo en la ecuación 4. Por consistencia, en estos ejemplos se han utilizado bromuros de alquilo. Reacciones similares ocurren cuando se utilizan cloruros o yoduros de alquilo, pero la velocidad de las reacciones y la distribución exacta de los productos cambiarán.
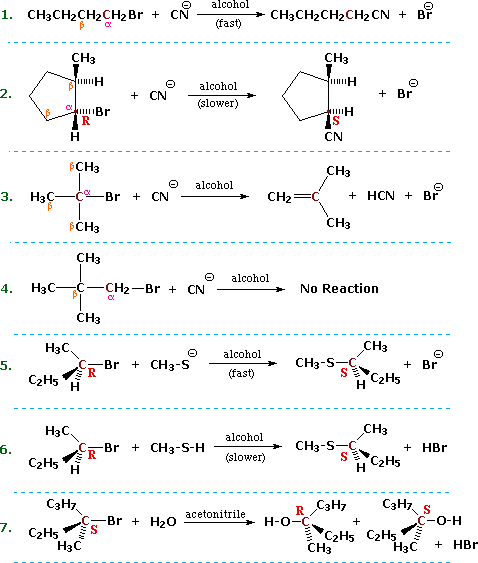
Para entender por qué algunas combinaciones de haluros de alquilo y nucleófilos dan una reacción de sustitución, mientras que otras combinaciones dan eliminación, y otras no dan reacción observable, debemos investigar sistemáticamente la forma en que los cambios en la reacción las variables perturban el curso de la reacción. La siguiente ecuación general resume los factores que serán importantes en dicha investigación.

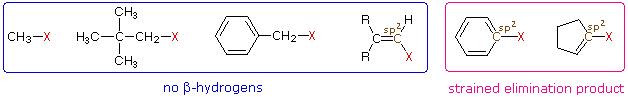
Recordatorio amistoso: Una conclusión, relacionar la estructura del grupo R con posibles productos, debería ser inmediatamente obvia. Si R- no tiene beta-hidrógenos no es posible una reacción de eliminación, a menos que se produzca primero un reordenamiento estructural. Los primeros cuatro haluros que se muestran a la izquierda de abajo no dan reacciones de eliminación en el tratamiento con base, debido a que no tienen β-hidrógenos. Los dos haluros de la derecha normalmente no experimentan tales reacciones debido a que los productos de eliminación potenciales tienen dobles o triples enlaces altamente tensos. También vale la pena señalar que los compuestos C-X hibridados con sp 2, como los tres de la derecha, normalmente no experimentan reacciones de sustitución nucleofílica, a menos que otros grupos funcionales perturbar el (los) doble enlace (s).
Ejercicio
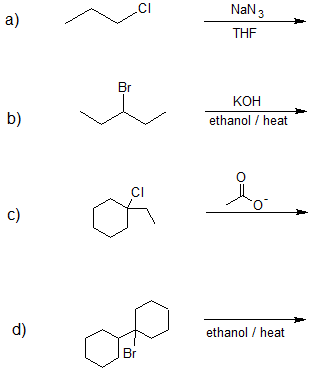
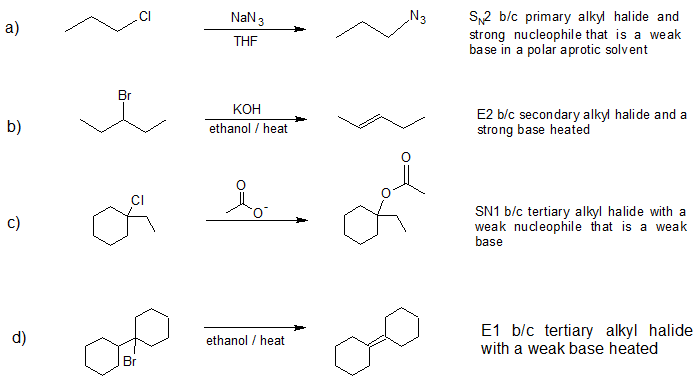
1. Identificar el mecanismo de reacción dominante (S N 1, S N 2, E1 o E2) y predecir el producto principal para las siguientes reacciones.
- Contestar
-
1.
Colaboradores
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

