10.4: Hidratación de Alquinos para Productos Markovnikov
- Page ID
- 75987
Objetivo de aprendizaje
- predecir los productos y especificar los reactivos para los productos Markovnikov de hidratación alquino
Reacción: Hidratación de alquinos (Regla de Markovnikov)
La hidratación de los alquinos comienza de manera similar a la hidratación de los alquenos mediante la adición de la primera molécula de agua. Sin embargo, esta primera reacción de hidratación forma un enol, un alcohol unido a un carbono vinílico. Los enoles se someten inmediatamente a un tipo especial de reacción de isomerización llamada tautomerización para formar grupos carbonilo - aldehídos o cetonas. Para que las cosas sean simples, esta reacción se llama tautomerización “enol-keto” con el entendimiento de que los aldehídos se forman en los carbonos alquinos terminales. Al igual que con los alquenos, la hidratación (adición de agua) a los alquinos requiere un ácido fuerte, generalmente ácido sulfúrico con un catalizador de sulfato mercúrico como se muestra a continuación.
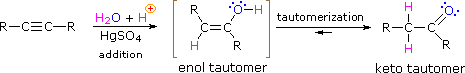
Tautomeros Enol-Keto
Los tautómeros se definen como isómeros constitucionales rápidamente interconvertidos, generalmente distinguidos por una ubicación de enlace diferente para un átomo de hidrógeno lábil (aquí coloreado de rojo) y un doble enlace ubicado de manera diferente. El equilibrio entre los tautómeros no solo es rápido en condiciones normales, sino que a menudo favorece fuertemente a uno de los isómeros (la acetona, por ejemplo, es 99.999% keto tautómeros). Incluso en esos equilibrios unilaterales, la evidencia de la presencia del tautomero menor proviene del comportamiento químico del compuesto. Los equilibrios tautoméricos son catalizados por trazas de ácidos o bases que generalmente están presentes en la mayoría de las muestras químicas. Los tres ejemplos que se muestran a continuación ilustran estas reacciones para diferentes sustituciones del triple enlace. El paso de tautomerización se indica con una flecha roja. Para los alquinos terminales la adición de agua sigue la regla de Markovnikov, como en el segundo ejemplo a continuación, y el producto final es una metil cetona (a excepción del acetileno, mostrado en el primer ejemplo). Para los alquinos internos (el triple enlace está dentro de una cadena más larga) la adición de agua no es regioselectiva. Si el triple enlace no está localizado simétricamente (es decir, si R & R' en la tercera ecuación no son iguales) se formarán dos cetonas isoméricas.
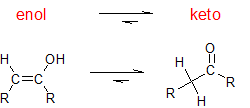
Con la adición de agua, los alquinos pueden hidratarse para formar enoles que tautomerizan espontáneamente a cetonas. La reacción es catalizada por iones de mercurio y sigue la Regla de Markovnikov. Una conversión útil de grupos funcionales para síntesis de múltiples etapas es hidratar alquinos terminales para producir metilcetonas.
Mecanismo de Hidratación de Alquino
El primer paso es una reacción ácido/base donde los electrones π del triple enlace actúan como una base de Lewis y reaccionan con el protón por lo tanto protonando el carbono con la mayor cantidad de sustituyentes de hidrógeno como se esperaba por la Regla de Markovnikov. En la segunda etapa, la molécula nucleofílica de agua reacciona con el carbocatión electrófilo para producir un ion oxonio. El ion oxonio es desprotonado por una base para producir un enol que inmediatamente se tautomeriza en una cetona. La reacción de hidratación para propino se muestra a continuación con su mecanismo para ilustrar el flujo de electrones del mecanismo.
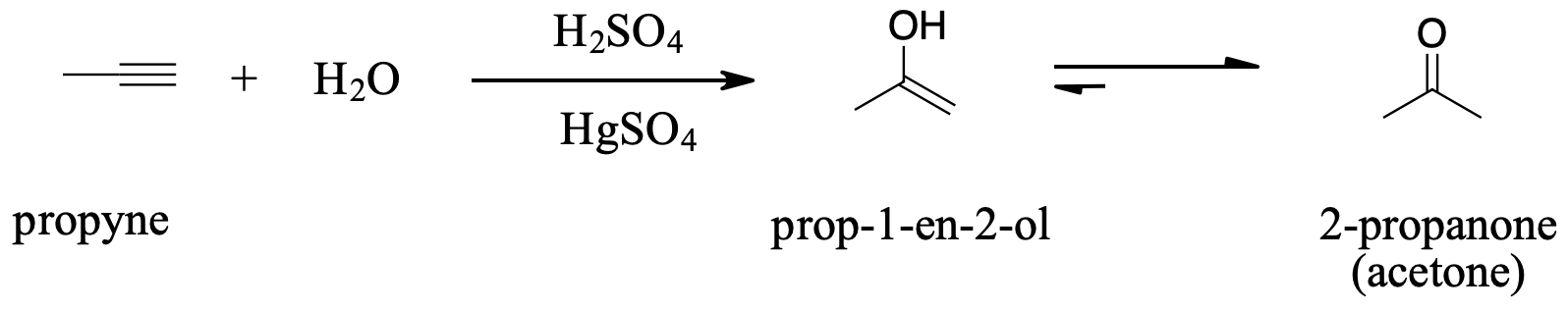
Ejercicio
- Dibujar la estructura del producto formado cuando cada una de las sustancias siguientes es tratada con H 2 O/H 2 SO 4 en presencia de HGSO 4.
- CH 3 CHCCH
-
- Dibuja la estructura de la forma keto del compuesto que se muestra a continuación. ¿Cuál forma esperarías que fuera la más estable?
- ¿Con qué alquino comenzarías para obtener los siguientes productos, en una reacción de oxidación? Tenga en cuenta la resonancia.
4. Proponer un esquema de reacción para el siguiente compuesto partiendo del alquino y mostrando los reactivos e intermedios requeridos.

- Responder
- 1.
-
2.
; La forma keto debe ser la más estable.
3.
4.

Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

