10.9: Síntesis de alquinos más grandes a partir de acetiluros
- Page ID
- 75997
Objetivo de aprendizaje
- predecir los productos y especificar los reactivos para sintetizar alquinos más grandes con iones acetilide
Reacciones de Sustitución Nucleofílica de Acetilidas 
Los aniones acetiluro son bases fuertes y nucleófilos fuertes. Por lo tanto, son capaces de desplazar haluros y otros grupos salientes en reacciones de sustitución. El producto es un alquino sustituido con una cadena carbonada continua más larga.
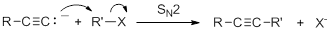
Debido a que el ion es una base muy fuerte, la reacción de sustitución sigue el mecanismo S N 2 y es más eficiente con metilo o haluros primarios sin sustitución cerca del centro de reacción.

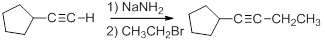
Los sustratos primarios secundarios, terciarios o incluso voluminosos darán eliminación por el mecanismo E2.

Adición nucleofílica de acetilidos a carbonilos
Los aniones acetiluros se agregarán a aldehídos y cetonas para formar alcóxidos que posteriormente se protonan para formar alcoholes propargílicos.
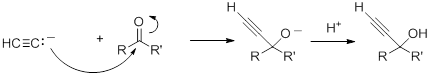
Con aldehídos y cetonas no simétricas, en ausencia de catalizador quiral, el producto será una mezcla racémica de los dos enantiómeros.
Ejercicio
1. El pK a de amoníaco es 35. Estimar la constante de equilibrio para la desprotonación de pent-1-ino por amida, como se muestra arriba.
2. Dar los posibles reactivos para las siguientes formaciones:

3. Proponer una ruta sintética para producir 2-penteno a partir de propino y un haluro de alquilo.
- Contestar
-
1. Suponiendo que el pK a de pent-1-ino es de aproximadamente 25, entonces la diferencia en pK a s es 10. Dado que el pentino es más ácido, la formación del acetiluro se verá favorecida en equilibrio, por lo que la constante de equilibrio para la reacción es de aproximadamente 10 10.
2.

3.
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

