16.6: La reacción de cicloadición de Diels-Alder (4 + 2)
- Page ID
- 76055
La reacción de cicloadición de Diels-Alder (4+2)
Una reacción de cicloadición es el enlace concertado entre sí de dos sistemas independientes de electrones pi para formar un nuevo anillo de átomos. Cuando esto ocurre, dos enlaces pi se convierten en dos enlaces sigma, siendo el ejemplo más simple la hipotética combinación de dos moléculas de eteno para dar ciclobutano. Esto no ocurre en condiciones normales, pero la cicloadición de 1,3-butadieno a cianoeteno (acrilonitrilo) sí, y este es un ejemplo de la reacción de Diels-Alder. El siguiente diagrama ilustra dos cicloadiciones e introduce varios términos que son útiles para discutir reacciones de este tipo.
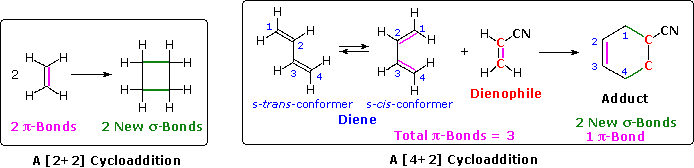
En la hipotética dimerización de etileno de la izquierda, cada molécula reaccionante tiene un enlace pi (color naranja) ocupado por dos electrones. La cicloadición convierte estos enlaces pi en nuevos enlaces sigma (de color verde), y esta transformación se denomina cicloadición [2+2], para enumerar los electrones pi reactivos que cambian su ubicación de unión.
La reacción de Diels-Alder es un método importante y ampliamente utilizado para hacer anillos de seis miembros, como se muestra a la derecha. Los reactivos utilizados en tales reacciones son un dieno conjugado, simplemente denominado dieno, y un correactante de doble o triple enlace llamado dienófilo, porque se combina con (tiene afinidad por) el dieno. La cicloadición de Diels-Alder se clasifica como un proceso [4+2] porque el dieno tiene cuatro electrones pi que cambian de posición en la reacción y el dienófilo tiene dos.
Mecanismo Diels-Aliso
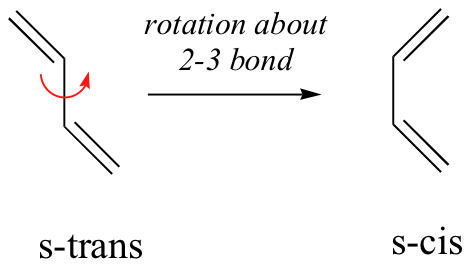
La reacción de Diels-Alder es un proceso de una sola etapa, por lo que el componente diénico debe adoptar una s-cisconformación para que los átomos de carbono finales (#1 y #4) se unan simultáneamente al dienófilo. Para muchos dienos acíclicos, el conformador s-trans es más estable que el conformador s-cis (debido al hacinamiento estérico de los grupos terminales), pero los dos están generalmente en rápido equilibrio, permitiendo el uso de todos menos los dienos más obstaculizados como reactivos en las reacciones de Diels-Alder. Para que ocurra una reacción de Diels-Alder, la molécula de dieno debe adoptar lo que se denomina conformación s-cis:
En su forma habitual, el componente diénico es rico en electrones, y los mejores dienófilos son pobres en electrones debido a sustituyentes aceptores de electrones como CN, C=O y NO 2. La interacción de enlace inicial refleja este desequilibrio electrónico, con los dos nuevos enlaces sigma que se forman simultáneamente, pero no necesariamente a tasas iguales. Esencialmente, este proceso implica la superposición de los orbitales 2p en los carbonos 1 y 4 del dieno con los dos orbitales 2p en los carbonos hibridados sp 2 del dienófilo. Ambos nuevos solapamientos forman nuevos enlaces sigma, y se forma un nuevo enlace pi entre el carbono 2 y 3 del dieno.
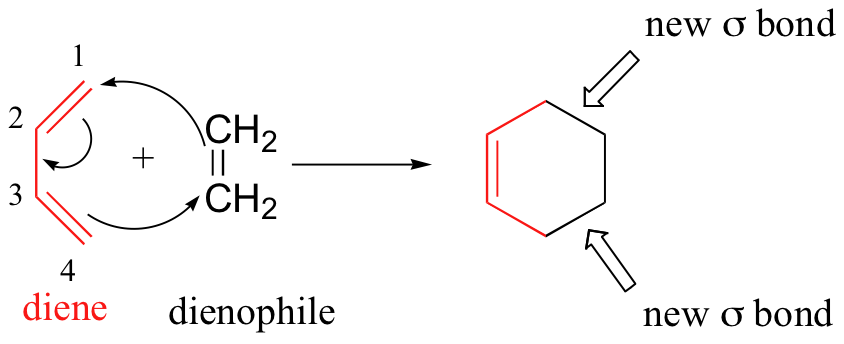
Una de las cosas más importantes a entender sobre este proceso es que está concertado —todo el reordenamiento de electrones tiene lugar a la vez, sin intermediarios de carbocatión.
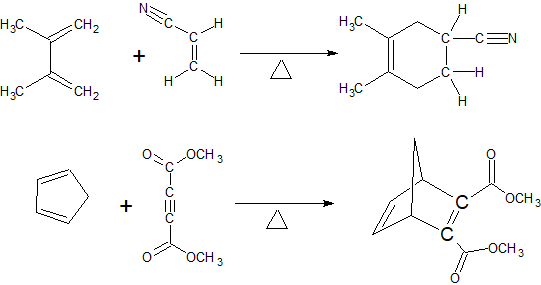
Dado que el dieno toma el papel del nucleófilo, el grupo donador de electrones aumenta la reactividad del dieno. Mientras que el dienófilo toma el papel del electrófilo, los grupos aceptores de electrones aumentan la reactividad del dienófilo. Las reacciones a continuación son ejemplos de la reacción de Diels-Alder.
Ejercicio
7. Dibuje las estructuras de la línea de unión para las reacciones a continuación.
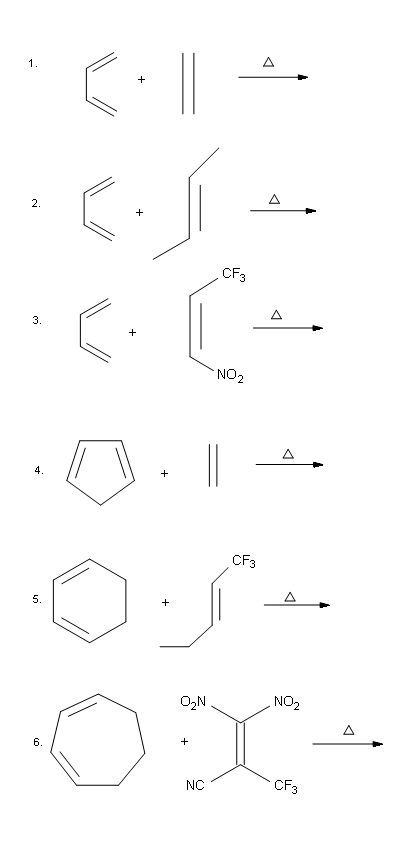
- Responder
-
7.
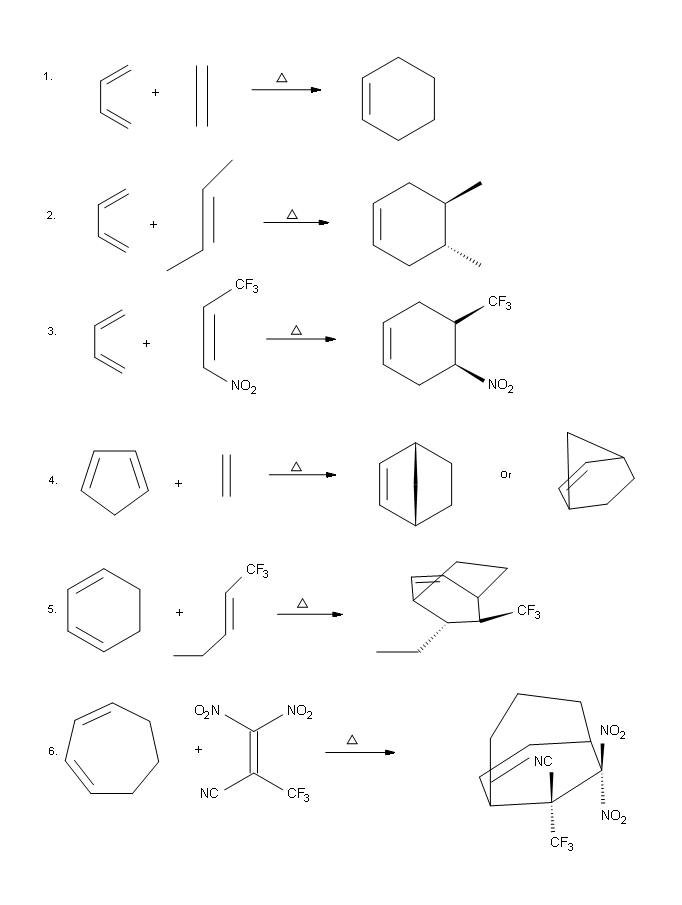.png)
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry
Organic Chemistry With a Biological Emphasis by Tim Soderberg (University of Minnesota, Morris)
- Amar Patel (UCD)

