21.4: Síntesis de Ácidos Carboxílicos
- Page ID
- 76899
Síntesis de Acidos Carboxílicos - Revisión
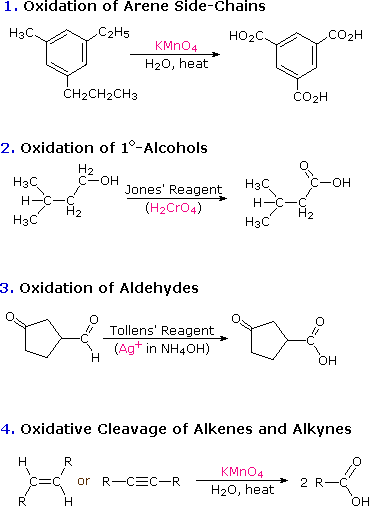
El átomo de carbono de un grupo carboxilo tiene un alto estado de oxidación. No es sorprendente, por lo tanto, que muchas de las reacciones químicas utilizadas para su preparación sean oxidaciones. Tales reacciones han sido discutidas en secciones anteriores de este texto, y el siguiente diagrama resume la mayoría de ellas. Para revisar la discusión previa de cualquiera de estas clases de reacción simplemente haga clic en el número (1 a 4) o encabezado descriptivo para el grupo.
Síntesis de Acidos Carboxílicos - Nuevo
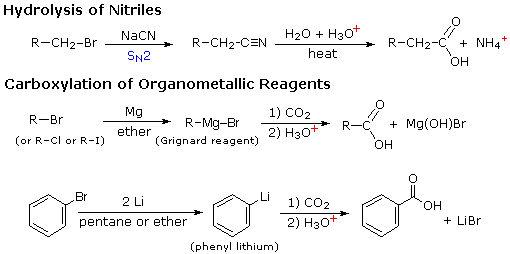
Otros dos procedimientos útiles para preparar ácidos carboxílicos implican la hidrólisis de nitrilos y la carboxilación de intermedios organometálicos. Como se muestra en el siguiente diagrama, ambos métodos comienzan con un compuesto orgánico halógeno y el grupo carboxilo eventualmente reemplaza al halógeno. Ambos métodos requieren dos etapas, pero son complementarios ya que el intermedio nitrilo en el primer procedimiento es generado por una reacción de S N 2, en la que el anión cianuro es un precursor nucleófilo del grupo carboxilo. La hidrólisis puede ser catalizada por ácido o base, pero esta última da una sal carboxilato como producto inicial.
En el segundo procedimiento el haluro electrófilo se transforma primero en un derivado metálico fuertemente nucleófilo, y esto se suma al dióxido de carbono (un electrófilo). El producto inicial es una sal del ácido carboxílico, que luego debe liberarse por tratamiento con ácido acuoso fuerte.
Un ácido carboxílico existente puede ser alargado por un grupo metileno, usando un procedimiento de homologación llamado reacción de Arddt-Eistert. Para conocer este útil método Haga clic aquí.
Hidrólisis de derivados de ácido carboxílico y nitrilos
En este capítulo aprendemos que todos los derivados de ácido carboxílico pueden sintetizarse a partir de ácidos carboxílicos. Estas reacciones tienden a ser más útiles para las síntesis de múltiples etapas para construir moléculas grandes y complejas. Los derivados de ácido carboxílico pueden hidrolizarse para producir ácidos carboxílicos. Estas reacciones de hidrólisis tienen un uso limitado en la síntesis de múltiples etapas debido a que el protón ácido puede ser problemático para muchas reacciones orgánicas. Bioquímicamente, las reacciones de hidrólisis son muy importantes en el metabolismo de alimentos, drogas y otros nutrientes. La hidrólisis puede ocurrir en condiciones ácidas o básicas que determinan la ionización del ácido carboxílico. Las reacciones en condiciones básicas requerirán una etapa final de neutralización con H + diluido para recuperar el ácido carboxílico. Para reforzar nuestra conciencia de la sensibilidad al pH de los ácidos carboxílicos, a continuación se muestran ambos mapas de reacción.
- Hidrólisis ácida de los derivados de ácido carboxílico
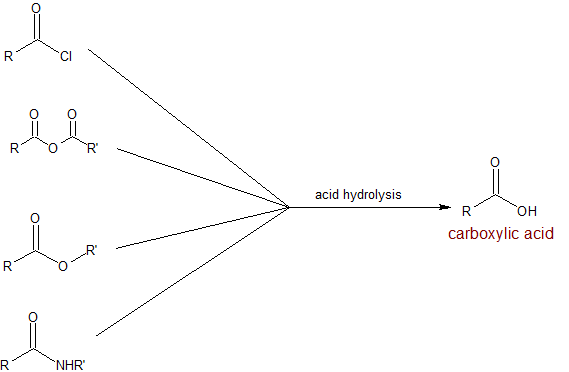
Pista útil: Diferentes profesores tienden a usar diferentes fuentes de protones. Es útil reconocer a los reactivos por su papel en una reacción. Por ejemplo, H 2 SO 4, HCl, H 3 PO 4, CH 3 CO 2 H y p-TSA son todas fuentes de H +. No importa cuál se utilice para catálisis o neutralización. El ácido nítrico es oxidante, por lo que normalmente solo se usa en reacciones de oxidación. A medida que continuamos aprendiendo más reacciones/reactivos, puede ayudar a agruparlos por su reactividad: ácidos, bases, neutros, oxidantes, reductores, próticos, apróticos, etc. Por ejemplo, los peróxidos son oxidantes, ya sea H 2 O 2 o MCPBA (ácido m-cloroperoxibenzoico).
- Hidrólisis Básica de los Derivados de
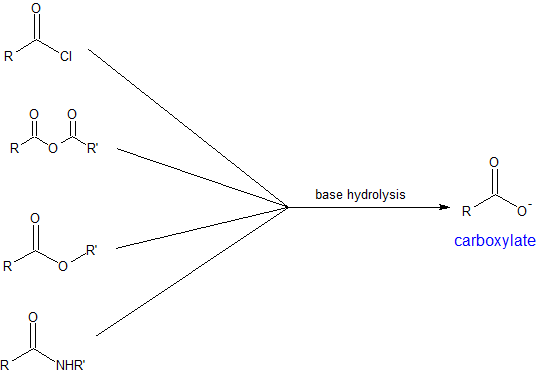
Ejercicio
4. Completa las reacciones a continuación.
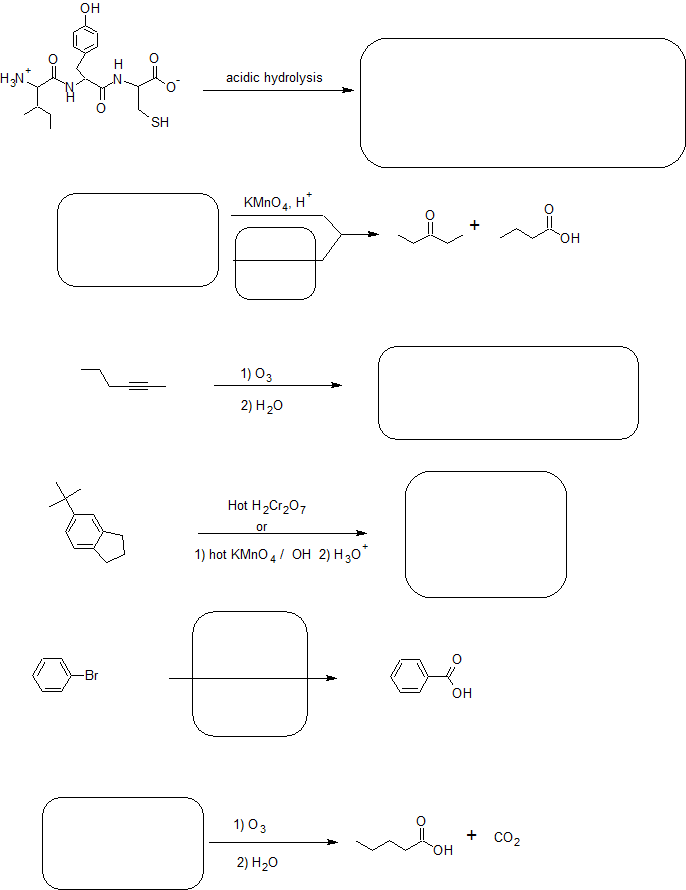
- Contestar
-
4.
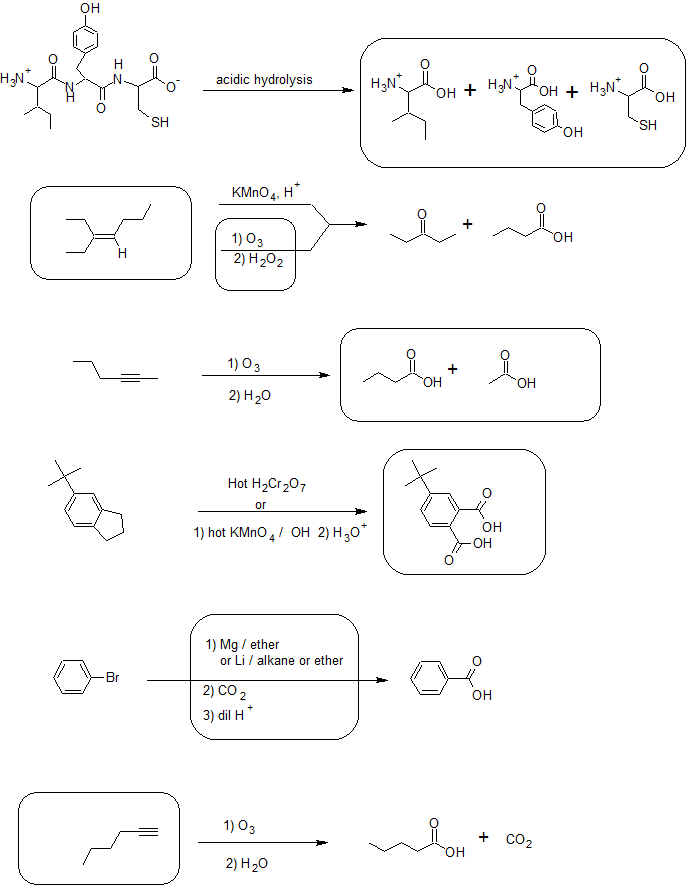
Colaboradores y Atribuciones
Dr. Dietmar Kennepohl FCIC (Professor of Chemistry, Athabasca University)
Prof. Steven Farmer (Sonoma State University)
- William Reusch, Professor Emeritus (Michigan State U.), Virtual Textbook of Organic Chemistry

