10.5: Enlaces N-glicosídicos
- Page ID
- 72356
Acabamos de ver que cuando un segundo alcohol ataca a un hemiacetal o hemicetal, el resultado es un acetal o cetal, con los enlaces glicosídicos en carbohidratos proporcionando un ejemplo bioquímico. Pero si un hemiacetal es atacado no por un segundo alcohol sino por una amina, lo que resulta es una especie de 'acetal mixto' en el que el carbono anomérico está unido a un oxígeno y un nitrógeno.
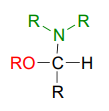
Este arreglo es referido por los bioquímicos como un enlace N-glicosídico. Puede reconocerlos como los enlaces en nucleósidos y nucleótidos que enlazan la base G, C, A, T o U con el azúcar.
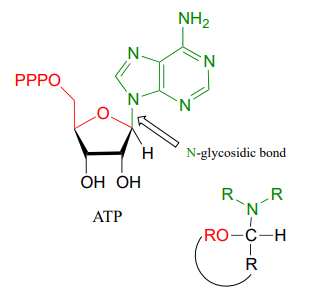
La formación de enlaces\(N\) glicosídicos en ribonucleótidos es muy análoga a la formación de enlaces glicosídicos en carbohidratos; nuevamente, es un proceso\(S_N1\) similar con un grupo saliente de agua activado. Típicamente, el hemiacetal se activa por difosforilación, como se ilustra en la etapa A del mecanismo general a continuación.
Mecanismo para la formación\(N\) de un enlace glicosídico:
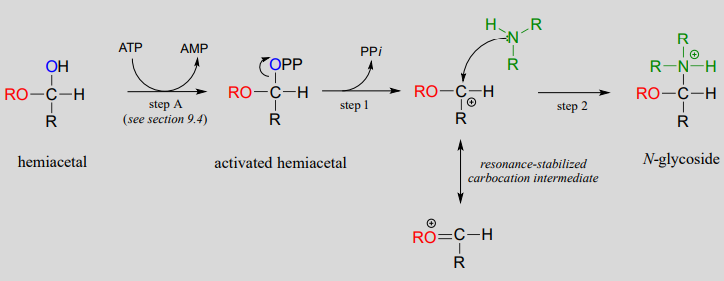
El punto de partida para la biosíntesis de ribonucleótidos de purina (G y A) es un azúcar de cinco carbonos llamado ribosa-5-fosfato, que en solución toma la forma de un hemiacetal cíclico. El enlace\(N\) crítico-glicosídico se establece a través de la sustitución de\(NH_3\) por\(OH\) en el carbono anomérico de la ribosa. El\(OH\) grupo anomérico se activa primero (paso A a continuación) para formar un intermedio activado llamado fosforibosilpirofosfato (PRPP). Luego, el pirofosfato inorgánico sale para generar un carbocatión estabilizado por resonancia (etapa 1) el cual es atacado por un amoníaco nucleófilo en la etapa 2 para establecer el enlace\(N\) glicosídico.
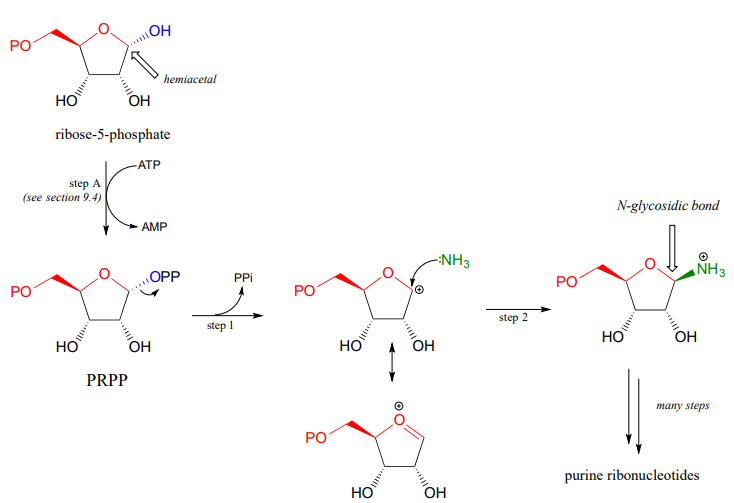
Con el enlace\(N\) -glicosídico en su lugar, el resto de la base de purina se ensambla pieza por pieza por otras enzimas biosintéticas.
(El mecanismo anterior debería parecer familiar - vimos el paso A en el capítulo 9 como un ejemplo de difosforilación de alcohol, y los pasos 1 y 2 en el capítulo 8 como un ejemplo de una\(S_N1\) reacción bioquímica).
El establecimiento del enlace\(N\) -glicosídico en la biosíntesis de los ribonucleótidos de pirimidina y (U, C y T) también comienza con PRPP, pero aquí la estructura anular de la parte base nucleotídica de la biomolécula ya ha sido 'prefabricada' en forma de orotato:
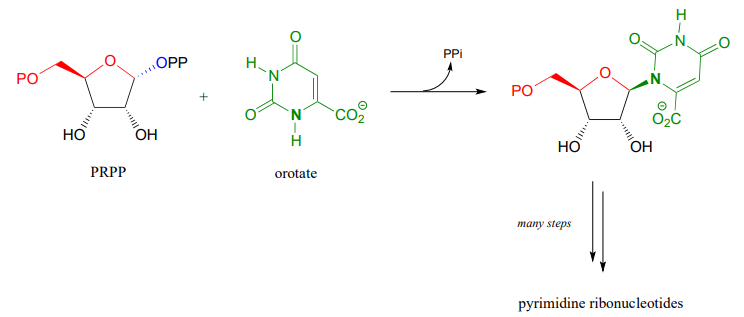
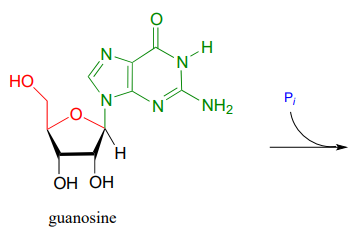
Acabamos de ver una ilustración de la formación de un enlace N-glicosídico en una vía biosintética. En la dirección catabólica (degradativa), se debe romper un enlace N-glicosídico, en un proceso que es análogo a la hidrólisis de un enlace glicosídico (ilustrado anteriormente). En el catabolismo del nucleósido de guanosina, el enlace N-glicosídico se rompe con fosfato inorgánico (¡no agua!) aparentemente en una reacción de desplazamiento concertada (similar a SN2) (Biochemistry 2011, 50, 9158). Predecir los productos de esta reacción, y dibujar un mecanismo probable.
Las glicoproteínas son proteínas que están unidas, por enlaces glicosídicos o N-glicosídicos, a azúcares o carbohidratos a través de una cadena lateral de asparagina, serina o treonina en la proteína. Como en otras reacciones de glicosilación y N-glicosilación, el hemiacetal del azúcar debe activarse antes de la formación del enlace glicosídico. A continuación se muestra la estructura del sustrato hemiacetal de azúcar activado en una reacción de glicosilación de asparagina.
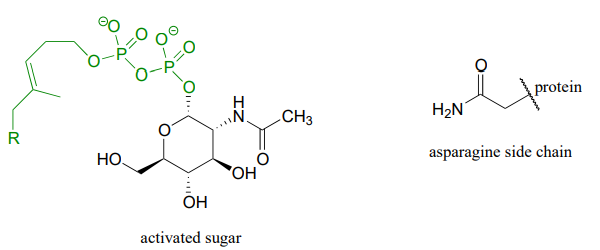
Dibujar el producto de la reacción de glicosilación de asparagina, asumiendo inversión de configuración del carbono anomérico.


