11.6: Acil-fosfatos
- Page ID
- 72122
Formación de tioéster
Los tioésteres, que en sí mismos son bastante reactivos en las reacciones de sustitución de acilo (pero menos que los fosfatos de acilo), juegan un papel crucial en el metabolismo de los ácidos grasos El 'grupo acilo X' en un tioéster es un tiol.
La coenzima A es una coenzima que contiene tiol que juega un papel clave en el metabolismo. La coenzima A a menudo se abrevía 'HSCoA' con el fin de enfatizar la importancia de la funcionalidad tiol.
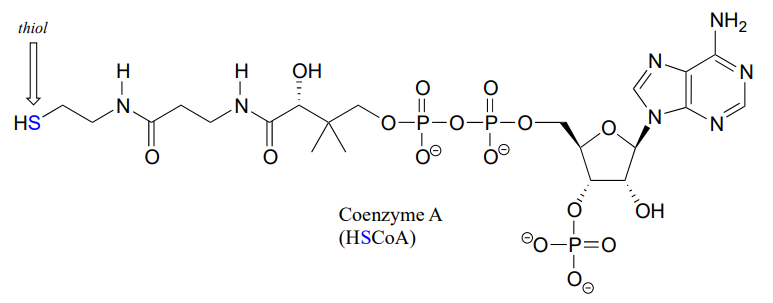
La coenzima A sirve como un grupo 'portador' en la biosíntesis de lípidos, y se une mediante un enlace tioéster a las cadenas de ácidos grasos en crecimiento. El palmitilo se muestra a continuación como un ejemplo de un tioéster de acil-CoA graso típico.
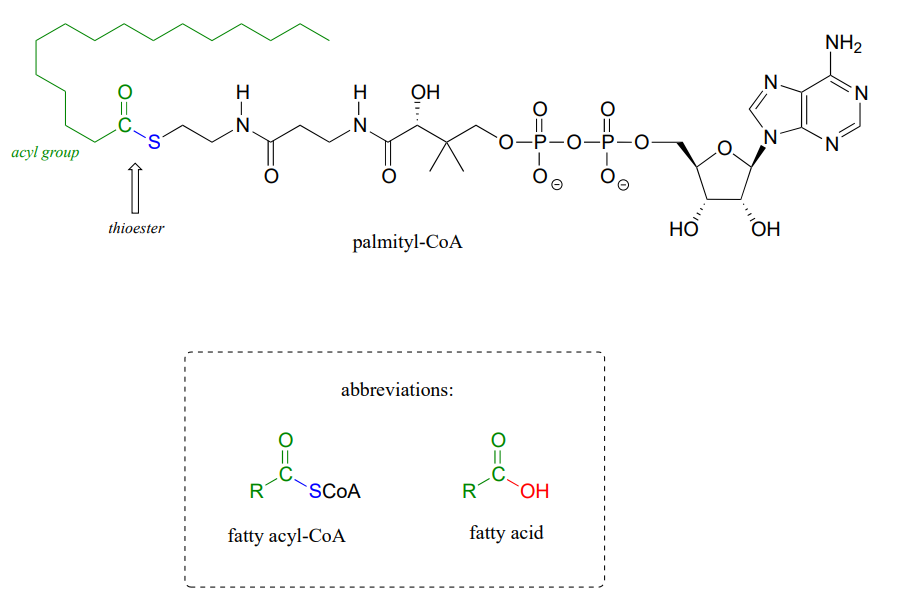
Al observar las reacciones que involucran tioésteres en esta y futuras secciones, frecuentemente veremos que la Coenzima A juega un papel clave. También veremos la formación y ruptura de enlaces tioéster entre un grupo acilo y otras especies que contienen tiol, como un residuo de cisteína en la enzima:
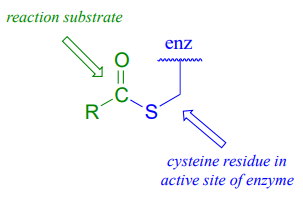
El término 'tioesterificación' se refiere a la formación de un grupo funcional tioéster. En una reacción de tioesterificación bioquímica típica, un carboxilato se convierte primero en un fosfato de acilo (es decir, se activa), luego el fosfato de acilo se somete a una reacción de sustitución de acilo con un nucleófilo de tiol.
Reacción de tioesterificación:

Mecanismo:
1. fase de activación:
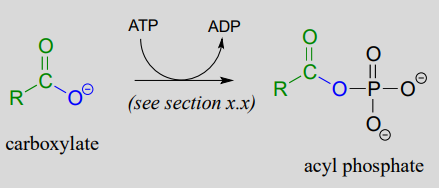
2. fase de sustitución de acilo:
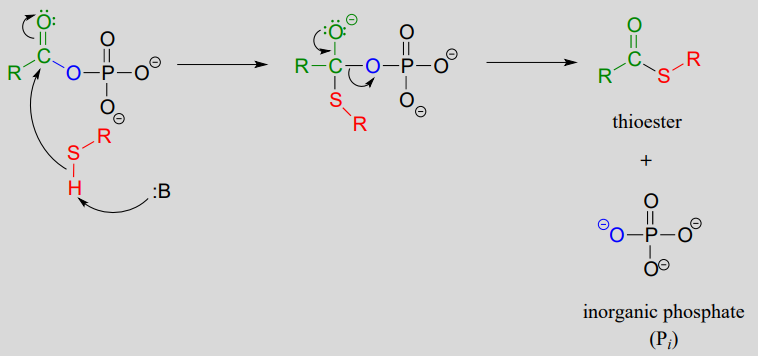
Los ácidos grasos como el palmitato, de las grasas y aceites de tu comida, se convierten en un tioéster de coenzima A antes de ser desintegrados por la vía de degradación de los ácidos grasos.
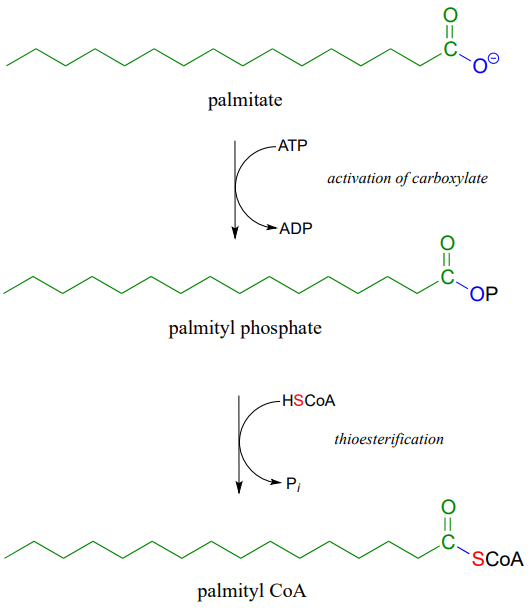
Una reacción de transtioesterificación es una conversión de tioéster a tioéster; en otras palabras, un grupo acilo se transfiere de un tiol a otro.
Transtioesterificación:
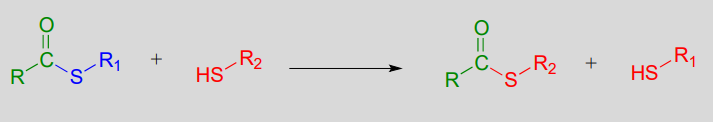
Mecanismo:
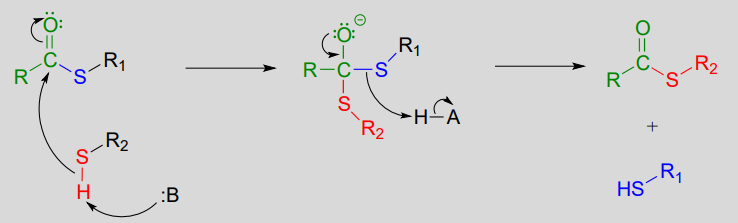
Por ejemplo, cuando tu cuerpo sintetiza ácidos grasos, el ácido graso de dos carbonos, acetil CoA, se convierte primero en acetil ACP (EC 2.3.1.38). ACP es una abreviatura de 'Acil Carrier Protein', una proteína modificada con un grupo protésico que contiene tiol unido a una de sus cadenas laterales de serina. A lo largo del proceso de elongación de la cadena de ácidos grasos, la cadena hidrocarbonada en crecimiento permanece unida
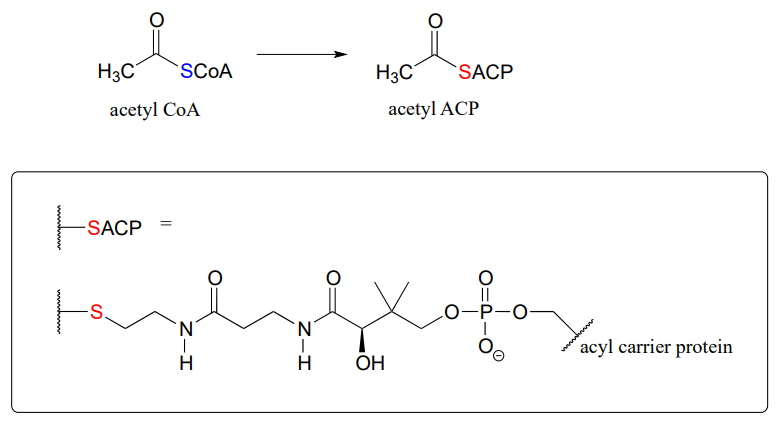
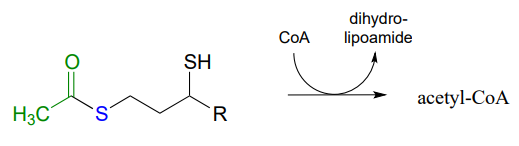
El complejo piruvato deshidrogenasa (EC 1.2.4.1) cataliza una de las reacciones metabólicas centrales más centrales, la conversión de piruvato a acetil-CoA, que une la vía gicolítica con el ciclo del ácido cítrico (Krebs). La reacción es bastante compleja, y aún no estamos equipados para seguirla de principio a fin (finalmente estaremos listos para hacerlo en la sección 17.3). El paso final, sin embargo, podemos entender: es una transtioesterificación, involucrando una coenzima ditiol llamada dihidrolipoamida y coenzima A. Dada la siguiente información, extraer un mecanismo razonable para la reacción.
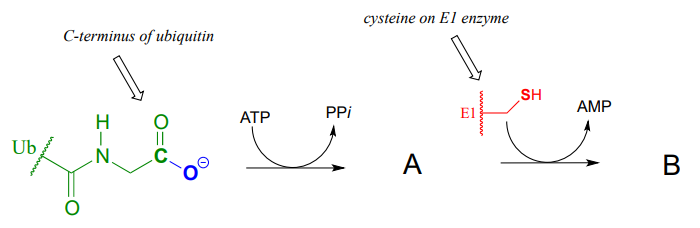
La ubiquitina es una proteína que juega un papel clave en muchos procesos celulares al unirse reversiblemente a otras proteínas, alterando o regulando así su función. Recientemente, un equipo de investigadores descubrió detalles del mecanismo por el cual la ubiquitina (abreviada Ub) es transferida por la enzima activadora de ubiquitina (abreviada E1) a proteínas diana. En la primera parte de este proceso, el extremo carboxi de la ubiquitina se une a una cadena lateral de cisteína en E1, como se muestra en la secuencia de reacción incompleta a continuación. Completar la figura dibujando las estructuras de las especies A y B.
Formación de ésteres
La esterificación se refiere a la formación de un nuevo grupo funcional éster.
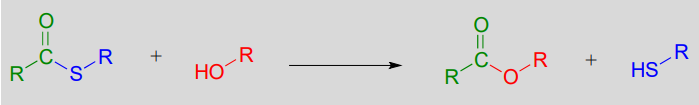
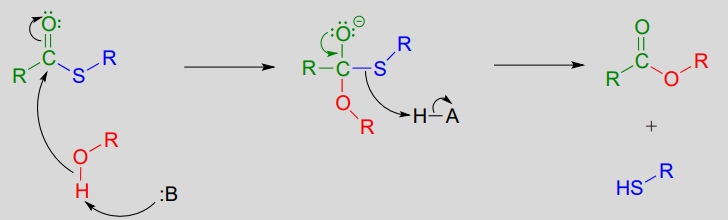
En una esterificación bioquímica típica, un tioéster es sometido a ataque nucleofílico de un alcohol, lo que lleva a la formación de un éster y un tiol.
Reacción de esterificación (a partir de tioéster):
Mecanismo:
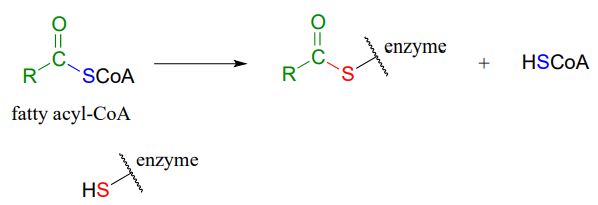
La reacción a continuación es de la síntesis del triacilglicerol, la forma en la que se almacena la grasa en nuestros cuerpos.
Fase 1 (transtioesterificación):
Fase 2 (esterificación):
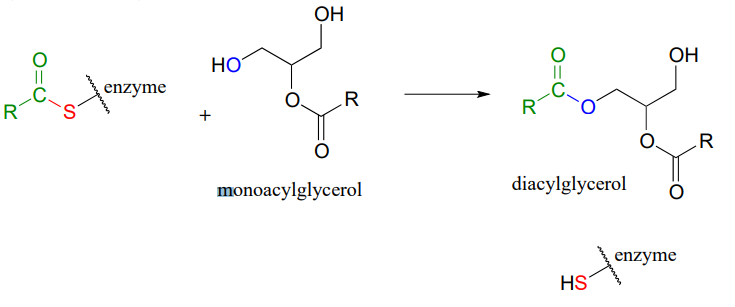
La reacción, catalizada por monoacilglicerol aciltransferasa (EC 2.3.1.22), comienza (fase 1 anterior) con una etapa preliminar de transtioesterificación en la que el grupo acilo graso se transfiere de la coenzima A a un residuo de cisteína en el sitio activo de la enzima. Recordemos que es una estrategia común que las enzimas formen primero un enlace covalente a un sustrato antes de catalizar la reacción química “principal”.
En la fase 2 de la reacción, el grupo acilo graso ya está listo para ser transferido a glicerol, intercambiando su enlace tioéster a la cisteína por un nuevo enlace éster a uno de los grupos alcohol en glicerol.
Una reacción de esterificación tiene una tremenda importancia en la historia del desarrollo de fármacos, historia que escuchamos en la introducción a este capítulo. El descubrimiento de la penicilina fue posiblemente uno de los eventos más importantes en la historia de la medicina moderna. El grupo funcional clave en la penicilina es la lactama de cuatro miembros (recordemos que una lactama es una amida cíclica).
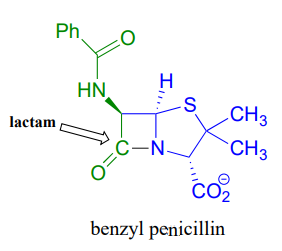
La penicilina, y posteriormente g eneraciones de antibióticos, han salvado innumerables vidas de infecciones bacterianas que alguna vez fueron mortales. La elucidación del mecanismo químico de la acción de la penicilina también fue un hito en nuestro desarrollo de la comprensión de cómo funcionan los fármacos a nivel molecular. Ahora sabemos que la penicilina, y medicamentos estrechamente relacionados como la ampicilina y la amoxicilina, funcionan inhibiendo una enzima que está involucrada en la construcción del componente peptídico de las paredes celulares bacterianas. Los detalles de la reacción de construcción de muros en sí están fuera del alcance de esta discusión, pero es suficiente saber que el proceso implica la participación de un residuo de serina nucleofílica en el sitio activo de la enzima. La molécula de penicilina es capaz de ingresar al sitio activo, y una vez dentro, el grupo lactama sirve como un 'cebo' electrófilo para la serina nucleofílica:
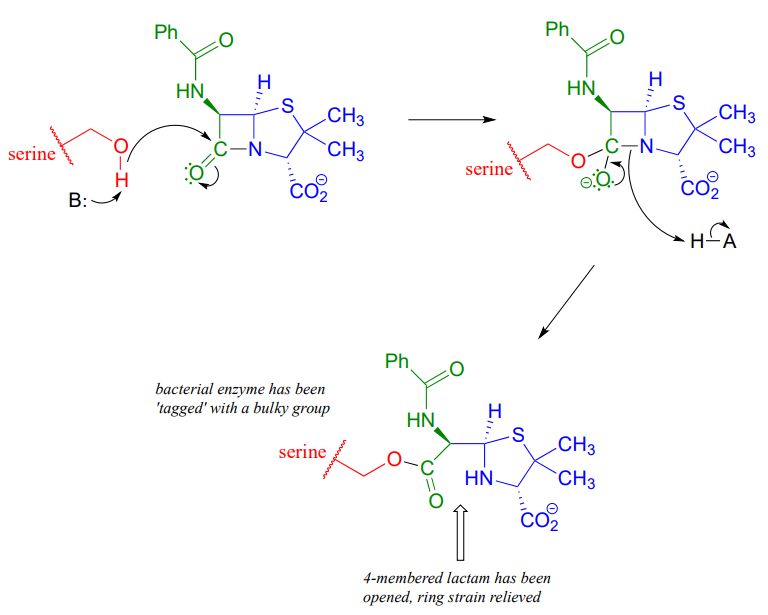
Aunque podría esperarse que una conversión de amida a éster como la que se muestra anteriormente sería energéticamente desfavorable en función de las tendencias de reactividad que hemos aprendido, esta lactama es de hecho mucho más reactiva que un grupo amida ordinario debido al efecto de la cepa del anillo: recuerde de la sección 3.2 que cuatro- los anillos de miembros están muy tensos y se libera una energía considerable cuando se abren.
La cepa de anillo también explica por qué la penicilina tiene tendencia a degradarse: cuando entra en contacto con el agua, la lactama se hidrolizará espontáneamente con el tiempo, lo que abre el anillo y forma un grupo carboxilato.
Desafortunadamente, muchas cepas de bacterias han adquirido una enzima llamada\(\beta \)-lactamase (EC 3.5.2.6), that catalyzes rapid hydrolysis of the lactam ring in penicillin-based drugs, rendering them inactive. These bacteria are consequently resistant to penicillin and related antibiotics. As you are probably aware, the evolution of drug resistance in bacteria is a major, world-wide health problem, and scientists are engaged in a constant battle to develop new antibiotics as the older ones become less and less effective.
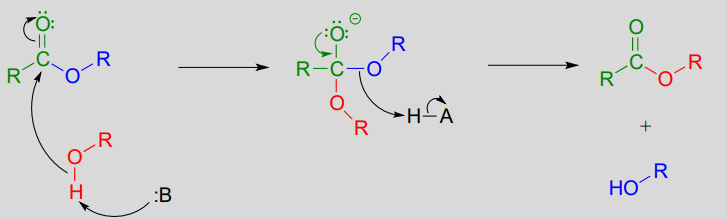
In a transesterification reaction, one ester is converted into another by an acyl substitution reaction.
Mechanism for a transesterification reaction:
If studying organic chemistry sometimes gives you a headache, you might want to turn to a transesterification reaction for help. Prostaglandins are a family of molecules that promote a wide range of biological processes, including inflammation. Acetylsalicylic acid, commonly known as aspirin, acts by transferring - through a transesterification reaction - an acetyl group to a serine residue on the enzyme responsible for the biosynthesis of prostaglandin H2 (one member of the prostaglandin family).
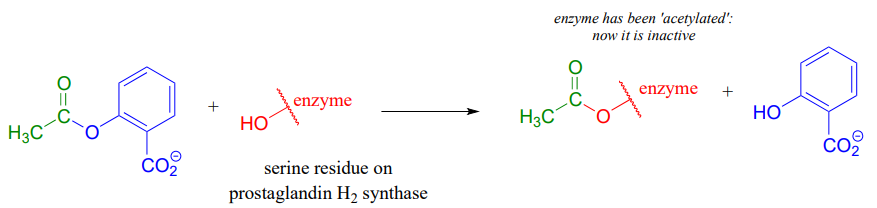
Acetylation of this serine blocks a channel leading to the active site, effectively shutting down the enzyme, impeding prostaglandin production, and inhibiting the inflammation process that causes headaches.
In section 11.8, we will see two laboratory acyl substitution reactions that lead to the formation of aspirin and ibuprofen.
Discuss the key structural feature of aspirin that makes it so effective at transferring its acetyl group - in other words, why is the ester group in aspirin more reactive than a typical ester?
Amide formation
An activated carboxylate group (in other words, acyl phosphate or acyl-AMP) can be converted to an amide through nucleophilic attack by an amine.
Mechanism for amide formation:
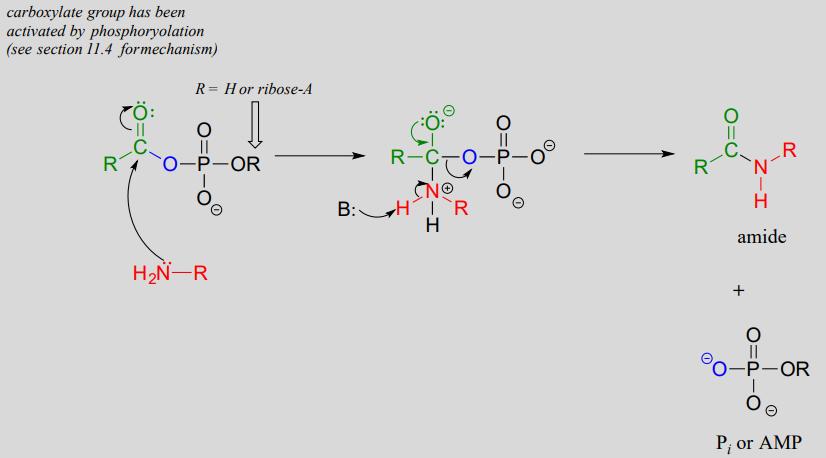
The amino acid biosynthesis pathways provide examples of amide formation in biology. The amino acid glutamine is synthesized in most species by converting the carboxylate side chain of glutamate (another amino acid) to an amide, after first activating the carboxylate by monophosphorylation: (EC 6.3.1.2)
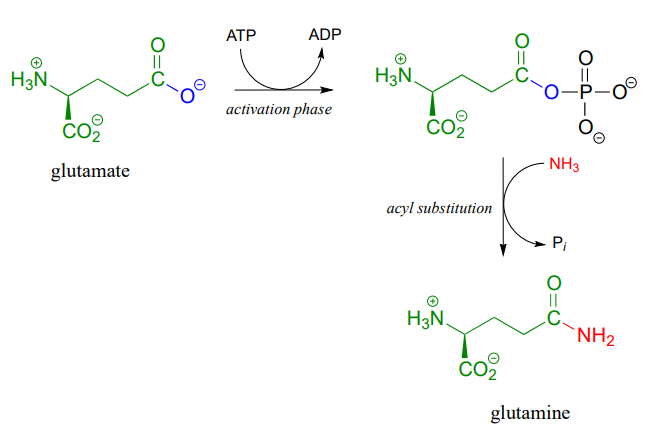
A similar process takes place in the synthesis of asparagine from aspartate, except that the activated carboxylate in this case is an acyl-AMP:
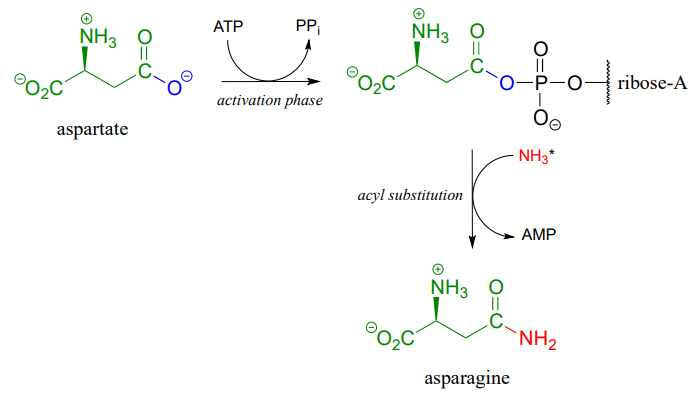
*En la reacción de síntesis de asparagina, el nucleófilo de amoníaco en realidad proviene de la hidrólisis de una molécula de glutamina.
Se cree que una enzima en bacterias es responsable de la resistencia a una clase de antibióticos que incluyen apramicina, ribostamicina y paromomicina. La enzima cataliza la acetilación del compuesto antibiótico con acetil-CoA como sustrato adicional. A continuación se muestra la estructura de la apramicina acetilada.
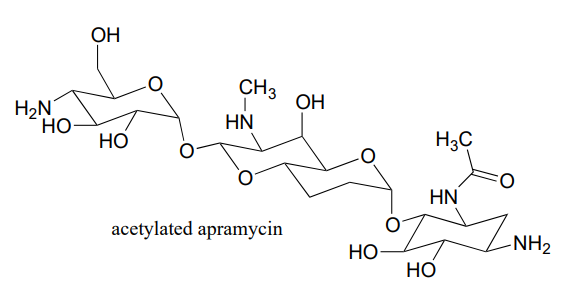
- a) Identificar el grupo acetilo que ha sido transferido a la apramicina, (y así inactivarlo).
- b) ¿Qué grupo funcional actúa como donante de grupos acetilo? ¿Qué grupo funcional actúa como grupo acetilo?
- c) ¿Cuál es el coproducto de la reacción?


