15.6: Monitoreo de reacciones de hidrogenación y deshidrogenación mediante espectroscopía UV
- Page ID
- 72216
Para estudiar cualquier reacción catalizada por enzimas, un investigador debe tener disponible algún tipo de prueba, o ensayo, para observar y medir el progreso de la reacción y medir su velocidad. En muchos casos, un ensayo simplemente implica ejecutar la reacción durante un período de tiempo especificado, luego aislar y cuantificar el producto usando una técnica de separación como la cromatografía líquida de alta resolución (HPLC) o la cromatografía de gases (GC). Este tipo de ensayo puede llevar mucho tiempo, sin embargo, por lo que es de gran ventaja para el investigador si se puede encontrar un ensayo más conveniente.
Las reacciones redox en las que participa una coenzima nicotinamida como donante o aceptor de hidruro son generalmente bastante convenientes para ensayar. De hecho, el avance de estas reacciones suele observarse en tiempo real, lo que significa que el investigador no necesita detener la reacción para ver hasta dónde ha progresado. \(NADPH\)y\(NADH\) tienen bandas distintivas\(n-\pi\) * de absorbancia UV centradas a 340 nm, con una absortividad molar de 6290 M-1 cm-1 (sección 4.4). Las coenzimas oxidadas\(NADP^+\) y\(NAD^+\) no absorben a esta longitud de onda.
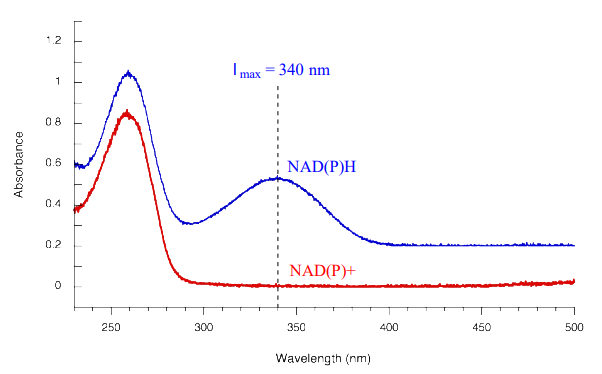
Por lo tanto, el curso de una reacción de hidrogenación, en la que\(NAD(P)H\) is converted to \(NAD(P)^+\), can be observed in real time if it is run in a quartz cuvette in a UV spectrometer. By observing the decrease in absorbance at 340 nm, the researcher can calculate how much \(NAD(P)H\) has been oxidized to \(NAD(P)^+\) at any given time point, and this number is the molar equivalent of the amount of organic substrate that has been reduced:
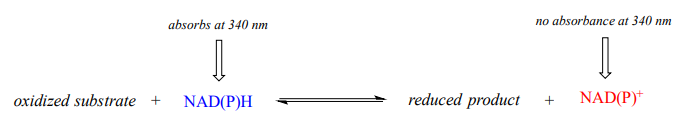
Asimismo, se puede seguir una reacción de deshidrogenasa\(NAD^+\) dependiente en tiempo real monitoreando el aumento de absorbancia a 340 nm a medida que\(NAD^+\) se convierte en\(NADH\).
Está observando el progreso de la reacción de (R) -glicerol fosfato deshidrogenasa que se muestra en la siguiente figura.
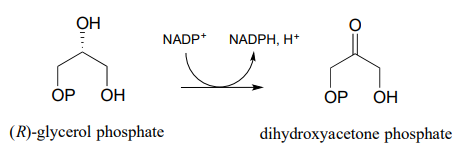
Se ejecuta la reacción en una cubeta de cuarzo (longitud de trayectoria 1 cm) en un volumen total de solución de 1 ml. se inicia con sustrato 200 mM y 100 mM\(NADP^+\) en solución, se pone a cero el espectrofotómetro UV, luego se agrega la enzima para iniciar la reacción. Después de 5 minutos, la lectura del A340 ha subido de 0.000 a 0.096. En este momento:
- ¿Cuántos moles de sustrato se han oxidado?
- ¿Cuál es la concentración de la solución\(NADP^+\)?
- La enzima tiene una masa de 25 kilodaltons (25,000 g/mol) .Agregaste 5 mL de una solución 2 ng/mL de enzima pura para iniciar la reacción. ¿Cuántas reacciones cataliza cada molécula enzimática, en promedio, por segundo? (Este número es referido por los bioquímicos como el 'número de rotación').


