17.5: Folato
- Page ID
- 72288
El folato, o vitamina\(B_9\), es esencial para una variedad de reacciones importantes en el metabolismo de nucleótidos y aminoácidos. La parte reactiva del folato es el sistema de anillos de pterina, que se muestra en rojo a continuación. También se indica el sistema convencional de numeración de átomos para folato.
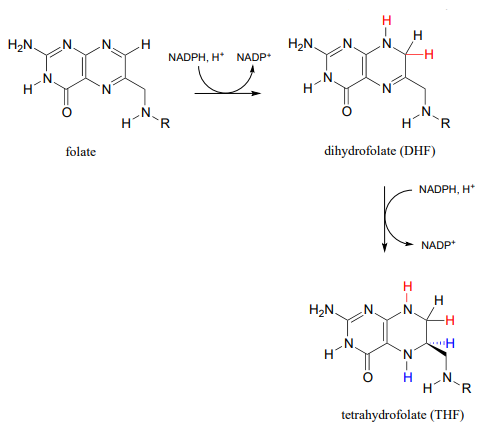
Formas activas de folato
El folato es activo como coenzima en sus formas reducidas, dihidrofolato y tetrahidrofolato, que están formados por\(NADPH-\)dependent imine hydrogenation steps (section 15.3).

El papel metabólico del folato es servir como donante o aceptor en reacciones de transferencia de carbono único. ¿En qué se diferencia el folato de la\(S\) -adenosilmetionina (\(SAM\), sección 8.8) que también sirve como donante de carbono único? Recordemos que\(SAM\) dona un solo carbono en forma de un grupo metilo: esencialmente, el carbono único de\(SAM\) está en el estado de oxidación metanol (\(CH_3OH\)), porque tiene solo un enlace a un heteroátomo (específicamente, al azufre). (Consulte la sección 15.1 para una revisión de los estados de oxidación).
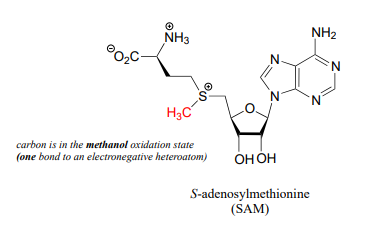
Las coenzimas de folato, por otro lado, pueden portar un solo carbono en los estados de oxidación de formaldehído y formiato, además del estado de oxidación del metanol. Por estado de oxidación 'formaldehído' y 'formiato', queremos decir que el carbono tiene dos y tres enlaces a heteroátomos, respectivamente.
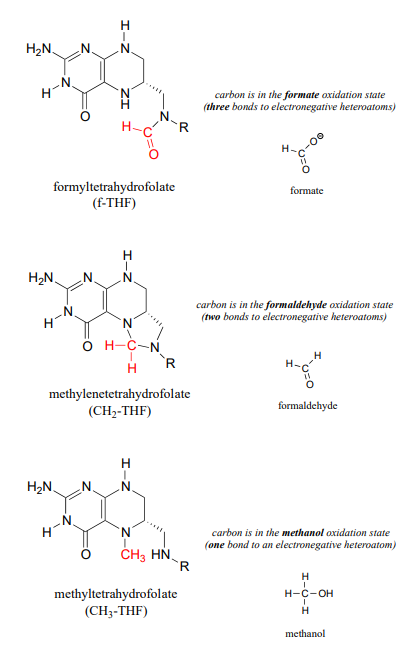
Algunas reacciones clave en las vías metabólicas de ácidos nucleicos y aminoácidos implican la transferencia de un solo carbono en los estados formaldehido o formiato. Sin embargo, esto podría presentar problemas. El formaldehído por sí mismo es muy tóxico: en particular, tiende a formar espontáneamente entrecruzamientos no deseados entre los grupos amina (por ejemplo, cadenas laterales de lisina) en las proteínas.
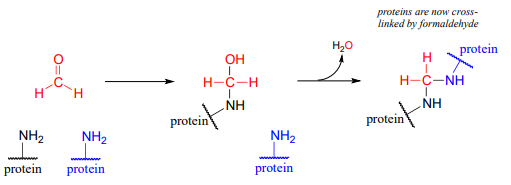
fig 53
El formaldehído libre es demasiado reactivo y causaría daños a una célula. El\(CH_2-THF\) coenzyme is stable in solution, but in the active site of certain enzymes it is reactive enough to serve as a formaldehyde donor, as we will see shortly.
Free formate, on the other hand, is a carboxylate, and we know from chapter 11 that carboxylates are not reactive in acyl substitution steps. Formate could be activated by phosphorylation, of course, but the resulting formyl phosphate would be too reactive in many enzyme active sites. A 'happy medium' has been found in which carbons in the formate oxidation state are carried by folate in the form of \(f-THF\): once again, the carbon donor is stable in solution, but sufficiently reactive in certain enzyme active sites to accomplish controlled transfer of a formate group.
Formation of formyl-\(THF\) and methylene-\(THF\)
Formyltetrahydrofolate (\(f-THF\)) is formed from \(THF\) and a formate molecule which has been activated by phosphorylation (formyl phosphate, as stated in the paragraph above, is a high reactive intermediate, but is held inside the enzyme's active site for immediate reaction with the incoming amine group of \(THF\)).

Hay dos rutas metabólicas principales para\(CH_2-THF\). Una ruta es solo el último paso de la reacción de serina hidroximetiltransferasa que ya hemos visto en la sección 17.1: el formaldehído formado en la fase dependiente de PLP de la reacción permanece en el sitio activo, y el oxígeno es desplazado por ataques sucesivos de los nucleófilos de amina en las posiciones 5 y 10 de\(THF\). (Observe la similitud con la reacción de reticulación formaldehído-proteína mostrada anteriormente en esta sección.)

En la segunda ruta,\(f-THF\) is dehydrated, then the resulting methenyl-\(THF\) intermediate is reduced by \(NADPH\).
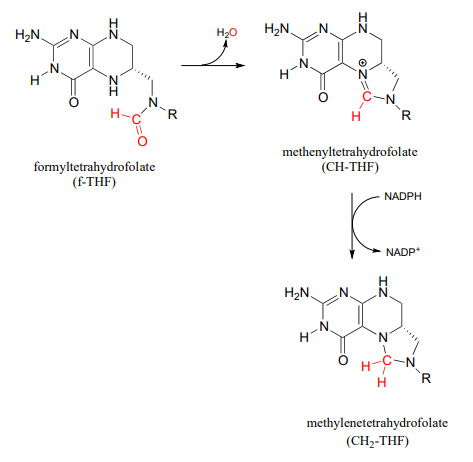
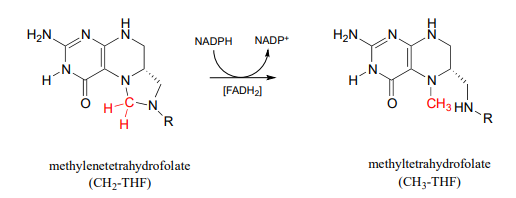
El metileno-\(THF\) (\(CH_2-THF\)) se reduce a metil-\(THF\) (\(CH_3-THF\)) en una reacción dependiente de flavina. Bioquímica 2001, 40, 6216
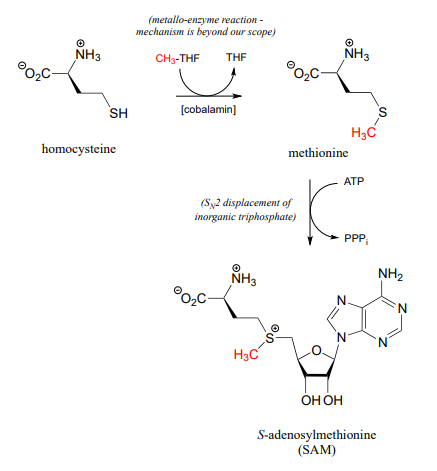
Recordemos de la introducción a este capítulo que los bebés que estuvieron en el útero durante el invierno del hambre holandesa enfrentaron un mayor riesgo, cuando llegaron a la edad adulta, de padecimientos como obesidad y esquizofrenia, muy probablemente causados por interrupciones en el\(S\)-adenosylmethionine-dependent methylation of their DNA, which was in turn caused by their mothers not getting enough folate. \(CH_3-THF\) is the source of the methyl group in methionine, which ultimately becomes the methyl group in \(SAM\). The methylation of homocysteine to methionine (below) involves a cobalt-containing coenzyme called cobalamin, but the mechanism for this reaction is beyond the scope of our discussion. The second reaction below (formation of \(SAM\)) is simply an \(SN_2\) displacement of the inorganic triphosphate leaving group on ATP by the nucleophilic sulfur in methionine.
Transferencia de carbono único con formyl-\(THF\)
Hay dos etapas importantes de formilación\(f-THF\) dependientes en las vías biosintéticas para nucleófilos de purina. Ambas son simplemente reacciones de transamidación: es decir, la conversión por el mecanismo de sustitución de acilo nucleofílico (capítulo 11) de una amida a otra.
Reacción de glicinamida ribonucleótido transformilasa:

Reacción de aminoimidazol carboxamida transformilasa:

¿Cuál de las dos reacciones de transformilasa anteriores esperaría que fuera más favorable cinéticamente? Explica tu razonamiento.
Predecir la estructura del 'producto X' en la reacción siguiente, a partir de la ruta de degradación de histidina.

Transferencia de un solo carbono con metileno\(THF\)
\(CH_2-THF\)sirve como donador de carbono único en una reacción algo complicada en la biosíntesis del monómero de ADN monofosfato de doexitimidina (\(dTMP\)).
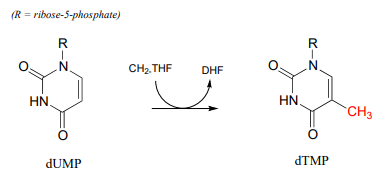
Las reacciones comienzan con el anillo de cinco miembros de\(CH_2-THF\) breaking apart to create an imine intermediate (step 1 below). The imine becomes an electrophile in a conjugate addition step (section 13.4, steps 2-3 below). Note that after step 1, the second ring in the pterin system of the coenzyme is abbreviated for clarity.

A continuación, se elimina el tetrahidrofolato en un mecanismo de\(E1cb\) eliminación (etapas 4 y 5). Observe que aquí es donde el carbono único se transfiere de metil-\(THF\) a dUMP.

El paso final en el mecanismo es donde se vuelve realmente interesante: un ion hidruro se transfiere de la coenzima tetrahidrofolato al metileno (\(CH_2\)) group on the deoxynucleotide substrate. Essentially, this is a conjugated \(SN_2\) step with hydride as the nucleophile and the active site cysteine as the leaving group.



