III. Formación de cationes radicales a partir de nucleótidos
- Page ID
- 80425
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
La adición del radical feniltiilo al nucleótido insaturado 30 produce el radical 31 centrado en carbono (Esquema 9). 2 Este radical (31) o bien abstrae un átomo de hidrógeno para dar una mezcla epimérica de nucleótidos reducidos o fragmenta el enlace C-O en C-3' heterolíticamente para dar un anión fosfato y un catión radical. 19 La fragmentación es asistida por disolventes polares. 20 Dado que la fragmentación heterolítica de 31 también depende de la capacidad del sustituyente en C-3' para estabilizar una carga negativa a medida que se rompe el enlace C-O, formar un anión altamente estabilizado es crítico; por lo tanto, la fragmentación es competitiva con la abstracción de átomos de hidrógeno cuando el anión producido es un fosfato (Esquema 9) pero no un benzoato (eq 8). 2

.png)
En el Esquema 10 se dan detalles adicionales sobre la formación de pares iónicos a partir del nucleótido insaturado 30. 21—24 Un par de iones de contacto (CIP), un par de iones separados por disolvente (SSIP) e iones libres de difusión están incluidos en este Esquema. Los experimentos de marcaje muestran cómo los diversos pares de iones participan en la reacción. Dado que no se produce ninguna aleatulación del marcador de oxígeno en el grupo fosfato en el sustrato 30 después de la reacción parcial, el CIP no puede regresar al radical 31 o si lo hace, no se produce ninguna reorganización dentro de este par iónico. 23 Dado que la mezcla de oxígeno puede tener lugar en el SSIP, los experimentos de marcaje muestran que una vez que se alcanza este intermedio, no hay retorno al radical 31.
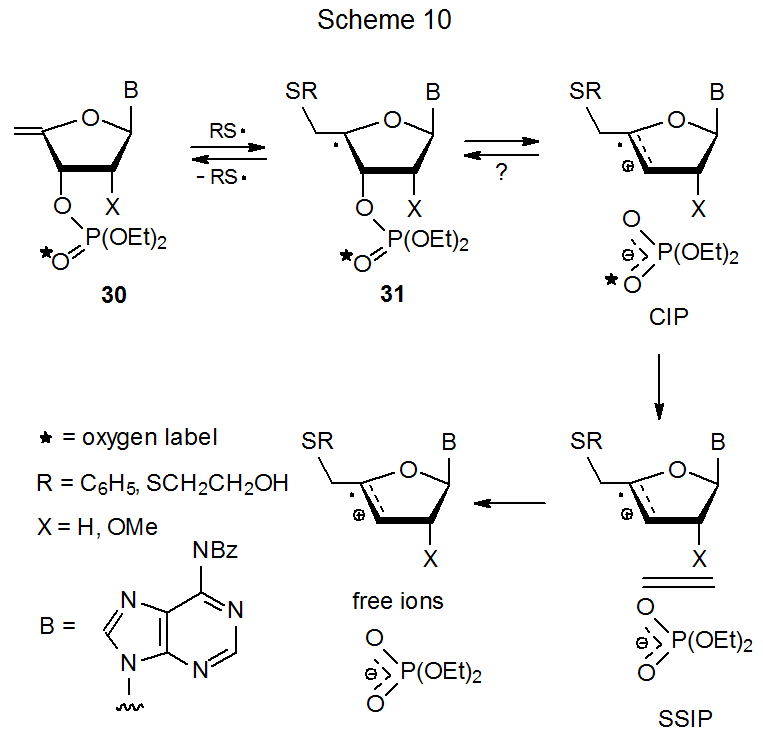
Estudios mecanicistas utilizando tanto alquil- como ariltioles muestran que el equilibrio entre el nucleótido 30 y el radical aducto 31 depende de la identidad del grupo R en el radical tiilo (Esquema 10). En este equilibrio, los radicales alquiltiilo favorecen la formación de aductos en mayor medida que los radicales ariltiilo. Cuando el método de formación produce una baja concentración de radicales, pueden existir condiciones en las que los radicales alquiltiilo formarán una concentración suficiente de radicales aductos (31) para que la reacción proceda a una velocidad observable, pero los radicales ariltiilo no producen el radical necesario concentración. 22
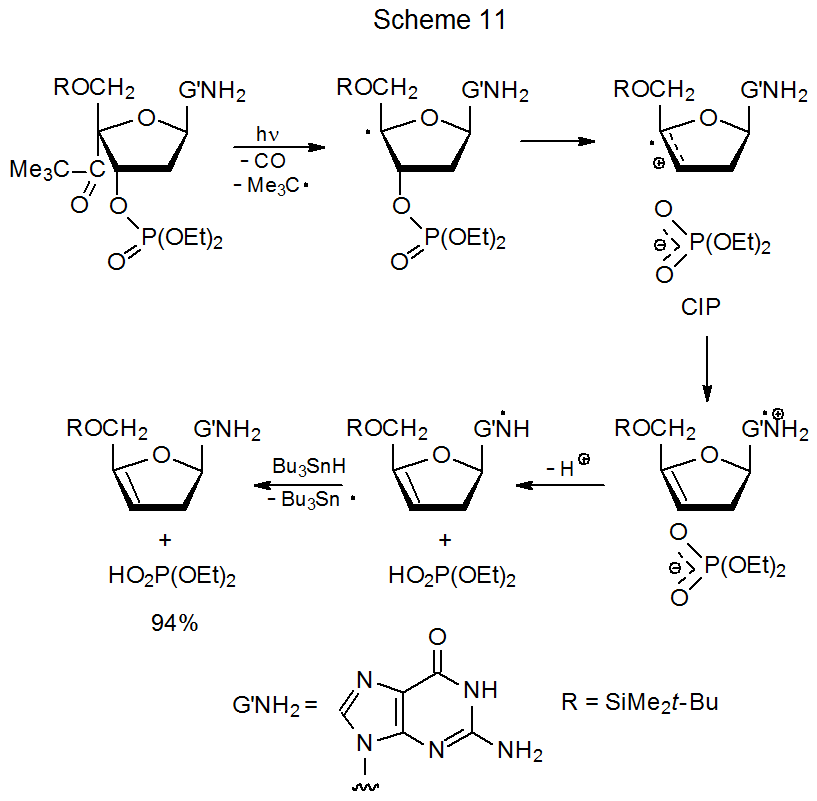
El estudio de las tasas de reacción radical de los derivados de timidina, citidina, adenosina y guanosina muestra que las guanosinas son, con mucho, las más reactivas. 23 (La velocidad de reacción de los derivados de guanosina es demasiado rápida para ser medida.) Esta reactividad mejorada se atribuye a la rápida transferencia interna de electrones desde el radical guanina a la porción catiónica radical de la molécula (Esquema 11). 23,25—27 La transferencia de electrones de este tipo puede ser lo suficientemente rápida (k > 1 x 10 9 s -1) para realizarse dentro del CIP. 23 Una estimación de la constante de velocidad para este tipo de transferencia de electrones es 1.4 x 10 8 s -1. 27