2.3D: Teoría de la Separación
- Page ID
- 74037
Teoría General
TLC es una excelente herramienta analítica para separar mezclas en una muestra. En esta sección se discuten los detalles de la separación, y ampliar la discusión general de la Sección 2.1.B.
En todas las formas de cromatografía, las muestras se equilibran entre las fases estacionaria y móvil. En casi todas las aplicaciones de TLC, la fase estacionaria es un adsorbente de sílice o alúmina y la fase móvil es un disolvente orgánico o mezcla de disolventes (el "eluyente “) que sube por la placa (ecuación 3).
\[\ce{X}_\text{(silica/alumina)} \rightleftharpoons \ce{X}_\text{(solvent)} \label{3}\]
El gel de sílice (mostrado en la Figura 2.16) está compuesto por una red de enlaces silicio-oxígeno, con\(\ce{O-H}\) enlaces en su superficie, así como una capa de moléculas de agua. \(\left( \ce{SiO_2} \cdot x \ce{H_2O} \right)\)El gel de sílice se utiliza en esta discusión, pero es estructuralmente análogo a la alúmina\(\left( \ce{Al_2O_3} \cdot x \ce{H_2O} \right)\). Esta fase estacionaria muy polar se empareja con una fase móvil relativamente no polar (un disolvente o solución orgánica), en lo que se denomina TLC de “fase normal”. Si bien esta es la forma más común de TLC (y en lo que se enfocará en esta sección), a veces se usa TLC de “fase inversa” (con una fase estacionaria no polar y una fase móvil polar).
La Figura 2.16 muestra cómo la acetofenona se adheriría a la superficie del gel de sílice a través de fuerzas intermoleculares (IMF). En este caso, la acetofenona puede formar enlaces de hidrógeno (el IMF indicado en la Figura 2.16a) a la superficie de la sílice a través de su átomo de oxígeno. A medida que el eluyente fluye sobre la muestra (Figura 2.16b), se establece un equilibrio entre la muestra que se adsorbe en la fase estacionaria y se disuelve en la fase móvil. Cuando está en la fase móvil, el compuesto sube por la placa con el flujo de líquido (Figura 2.16c) para posteriormente readsorber en la fase estacionaria más arriba de la placa. El resultado\(R_f\) del compuesto depende de la cantidad de tiempo empleado en las fases estacionaria y móvil.
.png)
La distribución de equilibrio entre las dos fases depende de varios factores:
- Depende de la fuerza de las fuerzas intermoleculares entre la muestra y la fase estacionaria.
Un compuesto que forme fuertes IMF con la sílice o alúmina a menudo favorecerá la fase estacionaria y pasará gran parte del tiempo de elución adherido a la placa. Esto significa que pasará menos tiempo en la fase móvil (que es el único medio para que viaje por el plato), haciendo que termine bajo en la placa TLC, y tenga un bajo\(R_f\).
Los compuestos que tienen átomos de oxígeno o nitrógeno deben ser capaces de formar enlaces de hidrógeno con la fase estacionaria (tener fuertes IMF con la fase estacionaria), y así tendrán\(R_f\) valores más bajos que los compuestos de tamaño similar que solo pueden interactuar a través de la dispersión de Londres fuerzas (LDF). - Depende de la fuerza de interacción entre la muestra y la fase móvil.
Como la fase móvil es siempre menos polar que la fase estacionaria en TLC de fase normal, los compuestos polares tenderán a tener una menor afinidad por la fase móvil que los compuestos no polares (basado en el principio de “como se disuelve como”). Por lo tanto, los compuestos polares tienden a pasar menos del tiempo de elución móvil que un compuesto no polar, por lo que viajarán “más lento” por la placa, y tendrán un bajo\(R_f\).
El grado de atracción de un compuesto a las fases estacionaria y móvil lleva a la misma conclusión:
- Cuanto más fuerte sea posible el FMI con la fase estacionaria (a menudo los grupos funcionales más polares en un compuesto), más tiempo el compuesto estará estacionario\(\rightarrow\) menor\(R_f\).
- Cuantos más grupos funcionales polares estén presentes en un compuesto, menos tiende a ser atraído por el eluyente menos polar, y menor será el tiempo que el compuesto será móvil\(\rightarrow\) menor\(R_f\).
Así, un compuesto con un menor\(R_f\) tiende a tener grupos funcionales más polares que un compuesto con un mayor\(R_f\) (resumido en la Figura 2.17).
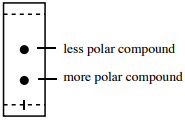
Consideraciones estructurales
Para demostrar el efecto de las características estructurales\(R_f\), en la Figura 2.18 se muestra una placa TLC eluida de alcohol bencílico, benzaldehído y etilbenceno. El orden relativo de\(R_f\) refleja la tendencia de polaridad en la serie.
.png)
El alcohol bencílico y el benzaldehído tienen grupos funcionales polares por lo que tuvieron\(R_f\) valores más bajos que el etilbenceno, que es completamente no polar. Ambos compuestos son capaces de unirse por hidrógeno a la fase estacionaria polar (Figura 2.19a+b), por lo que son atraídos más fuertemente a la fase estacionaria que el etilbenceno, que interactúa sólo a través de débiles fuerzas de dispersión de Londres (Figura 2.19c). Como el menos “polar” de la serie, el etilbenceno es también el mejor disuelto por el eluyente débilmente polar. Por estas razones, el etilbenceno pasó el menor tiempo en la fase estacionaria y el mayor tiempo en la fase móvil, razón por la cual viajó más arriba de la placa y tuvo la más alta\(R_f\) de la serie.
.png)
Tanto el benzaldehído como el alcohol bencílico son capaces de formar enlaces de hidrógeno con la fase estacionaria, pero el alcohol bencílico tuvo el menor\(R_f\) debido a que puede formar más enlaces de hidrógeno (a través tanto de los átomos de oxígeno como de hidrógeno del\(\ce{OH}\) grupo, Figura 2.19a). Esto provocó que el alcohol bencílico se adhiriera más fuertemente a la sílice/alúmina que al benzaldehído, lo que provocó que pasara más tiempo en la fase estacionaria.
Para demostrar un efecto estructural diferente sobre\(R_f\), se muestra una placa TLC eluida de acetofenona y benzofenona en la Figura 2.20. Ambos compuestos son similares en que pueden formar enlaces de hidrógeno a la fase estacionaria a través de su átomo de oxígeno. Sin embargo, el mayor tamaño de la benzofenona hace que tenga un poco\(R_f\) más alto que la acetofenona.
.png)
Este resultado se puede explicar de múltiples maneras:
- El átomo de oxígeno en la benzofenona está más abarrotado por los anillos aromáticos que el átomo de oxígeno de la acetofenona, lo que puede impedir su capacidad de formar enlaces de hidrógeno fuertemente con el gel de sílice. Esto puede conducir a una menor cantidad de tiempo adsorbida por la fase estacionaria.
- El volumen no polar adicional de la benzofenona hace que se disuelva mejor en el eluyente débilmente polar, lo que hace que pase más tiempo en la fase móvil.
Polaridad de fase móvil
La capacidad de la cromatografía para separar componentes en una mezcla depende del equilibrio de un compuesto entre las fases estacionaria y móvil. Dado que la fase móvil es un factor importante, es posible cambiar la\(R_f\) de un compuesto cambiando la polaridad de la fase móvil.
Cuando una fase móvil se hace más polar que originalmente, todos los compuestos viajan más lejos y tienen una mayor\(R_f\).
Esta tendencia general se demuestra en la Figura 2.21b+c, donde la TLC de tres compuestos activos UV (carriles 2-4) se realizó usando dos disolventes mixtos diferentes. La primera placa se ejecutó usando una mezcla 6:1 de hexano:acetato de etilo, lo que significa que el disolvente se creó usando 6 volúmenes de hexano por cada 1 volumen de acetato de etilo. Este disolvente mixto es en su mayoría no polar debido al alto porcentaje de hexano, pero es más polar que el hexano lineal, debido a la presencia de algo de acetato de etilo (que tiene enlaces polares, Figura 2.21a). La segunda placa se ejecutó utilizando una mezcla 3:2 de hexano:acetato de etilo, la cual es más polar que la mezcla 6:1 debido a que hay un mayor porcentaje de acetato de etilo presente.
.png)
| Carril | \(R_f\)en 6:1 (eluyente menos polar) | \(R_f\)en 3:2 (eluyente más polar) |
|---|---|---|
| 2 | \ (R_f\) en 6:1 (eluyente menos polar) ">0.33 | \ (R_f\) en 3:2 (eluyente más polar) ">0.54 |
| 3 (punto inferior) | \ (R_f\) en 6:1 (eluyente menos polar) ">0.02 | \ (R_f\) en 3:2 (eluyente más polar) ">0.17 |
| 3 (primer puesto) | \ (R_f\) en 6:1 (eluyente menos polar) ">0.28 | \ (R_f\) en 3:2 (eluyente más polar) ">0.52 |
| 4 | \ (R_f\) en 6:1 (eluyente menos polar) ">0.49 | \ (R_f\) en 3:2 (eluyente más polar) ">0.65 |
Obsérvese que en la Figura 2.21c todas las manchas mantuvieron su orden relativo pero viajaron a una mayor altura en la placa e incrementaron sus\(R_f\) valores (Cuadro 2.2) en el eluyente más polar.
Un aumento en la polaridad del disolvente aumenta\(R_f\) los valores por dos razones:
- Los compuestos moderadamente polares tienen una mayor atracción hacia la fase móvil.
Al equilibrar entre una fase estacionaria polar y un eluyente no polar, un compuesto polar tiende a favorecer la fase estacionaria polar y tener un bajo\(R_f\). Si se hace que el eluyente sea moderadamente polar, los compuestos polares son entonces más atraídos por la fase móvil, haciendo que el equilibrio cambie de tal manera que el compuesto pase más tiempo en la fase móvil, resultando en una mayor\(R_f\). - El disolvente polar puede ocupar sitios de unión sobre la superficie de sílice o alúmina, de manera que desplazan la muestra de la fase estacionaria.
Si un disolvente polar es capaz de formar enlaces de hidrógeno y, por lo tanto, está fuertemente asociado con la fase estacionaria, puede “bloquear” los sitios de unión y obligar a los compuestos menos polares a pasar más tiempo en la fase móvil. El resultado es un aumento\(R_f\) para compuestos polares y no polares por igual.


