2.11: Fuerzas intermoleculares y puntos de ebullición relativos (pb)
- Page ID
- 76723
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Objetivo de aprendizaje
- predecir los puntos de ebullición relativos de los compuestos orgánicos
Las fuerzas intermoleculares (IMF) se pueden utilizar para predecir puntos de ebullición relativos. Cuanto más fuertes sean los IMF, menor será la presión de vapor de la sustancia y mayor será el punto de ebullición. Por lo tanto, podemos comparar las fuerzas relativas de los IMF de los compuestos para predecir sus puntos de ebullición relativos.
Adhesión en H > dipolo-dipolo > Dispersión Londres (van der Waals)
Al comparar compuestos con los mismos IMF, utilizamos el tamaño y la forma como desatadores, ya que las fuerzas de dispersión de Londres aumentan a medida que aumenta el área de superficie. Dado que todos los compuestos exhiben cierto nivel de fuerzas de dispersión de Londres y los compuestos capaces de unirse a H también exhiben dipolo-dipolo, usaremos la frase “IMF dominante” para comunicar al FMI más responsable de las propiedades físicas del compuesto.
En la siguiente tabla, vemos ejemplos de estas relaciones. Al comparar los isómeros estructurales del pentano (pentano, isopentano y neopentano), todos tienen la misma fórmula molecular C 5 H 12. Sin embargo, a medida que la cadena de carbono se acorta para crear las ramas de carbono que se encuentran en isopentano y neopentano, la superficie total de las moléculas disminuye. La imagen visual de la teoría MO puede ser útil para ver cada compuesto como una nube de electrones en un sistema MO que abarca todo. La ramificación crea formas más esféricas señalando que la esfera permite el volumen máximo con la menor superficie. Los isómeros estructurales con la fórmula química C 2 H 6 O tienen diferentes IMF dominantes. La unión H del etanol resulta en un líquido para cócteles a temperatura ambiente, mientras que el dipolo-dipolo más débil del éter dimetílico da como resultado un gas a temperatura ambiente. En el último ejemplo, vemos los tres IMF comparados directamente para ilustrar la fuerza relativa IMF a los puntos de ebullición.
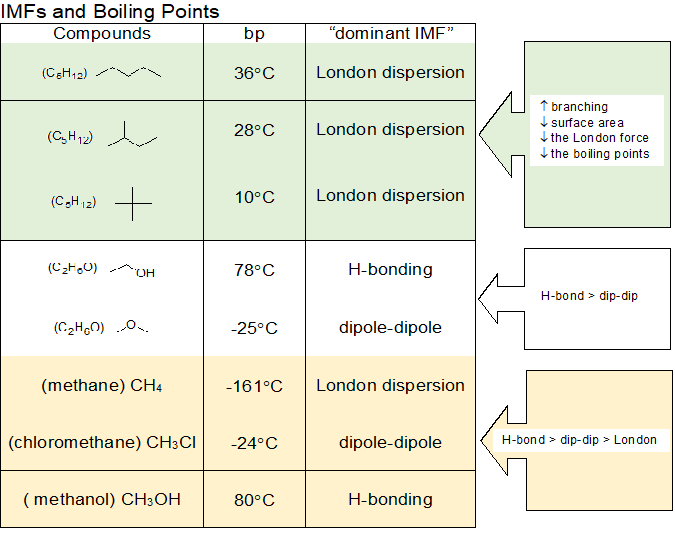
Puntos de ebullición y puntos de fusión
Los puntos de fusión y ebullición observables de diferentes moléculas orgánicas proporcionan una ilustración adicional de los efectos de las interacciones no covalentes. El principio general involucrado es simple: cuanto más fuertes son las interacciones no covalentes entre las moléculas, más energía se requiere, en forma de calor, para separarlas. Los puntos de fusión y ebullición más altos significan fuerzas intermoleculares no covalentes más fuertes.
Considera los puntos de ebullición de hidrocarburos cada vez más grandes. Más carbonos significa una mayor superficie posible para la interacción hidrofóbica y, por lo tanto, mayores puntos de ebullición.
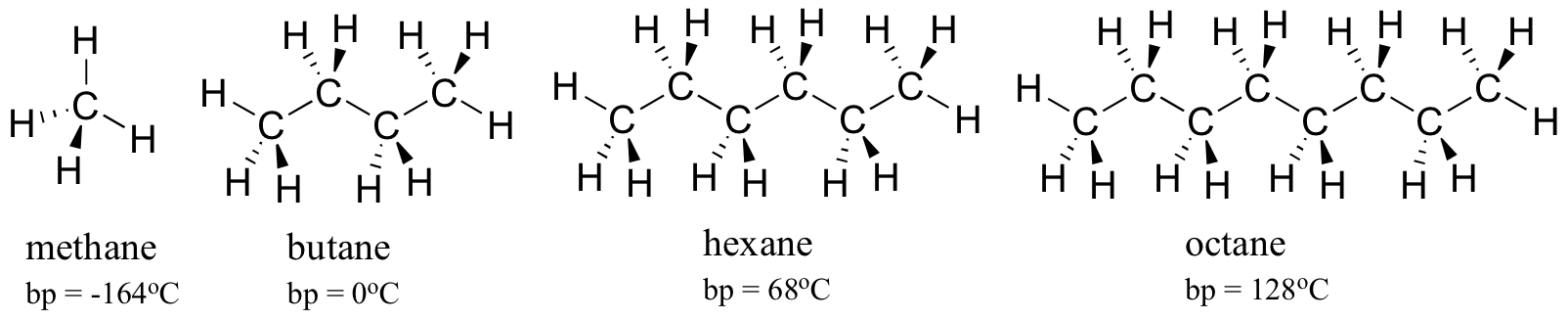
Como era de esperar, la fuerza de los enlaces intermoleculares de hidrógeno y las interacciones dipolo-dipolo se refleja en puntos de ebullición más altos. Basta con observar la tendencia del hexano (solo interacciones de dispersión no polares en Londres), 3-hexanona (interacciones dipolo-dipolo) y 3-hexanol (enlaces de hidrógeno).

De particular interés para los biólogos (y prácticamente cualquier otra cosa que esté viva en el universo) es el efecto de los enlaces de hidrógeno en el agua. Debido a que es capaz de formar redes estrechas de enlaces de hidrógeno intermoleculares, el agua permanece en fase líquida a temperaturas de hasta 100 O C, (ligeramente inferiores a gran altitud). El mundo obviamente sería un lugar muy diferente si el agua hierve a los 30 O C.

