7.3: Errores en la Meiosis
- Page ID
- 54116
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Los trastornos hereditarios pueden surgir cuando los cromosomas se comportan de manera anormal durante la meiosis. Los trastornos cromosómicos se pueden dividir en dos categorías: anomalías en el número de cromosomas y reordenamientos estructurales cromosómicos Debido a que incluso pequeños segmentos de cromosomas pueden abarcar muchos genes, los trastornos cromosómicos son característicamente dramáticos y a menudo fatales.
Trastornos en el número cromosómico
El aislamiento y observación microscópica de los cromosomas constituye la base de la citogenética y es el método principal por el cual los médicos detectan anomalías cromosómicas en humanos. Un cariotipo es el número y la aparición de cromosomas, incluyendo su longitud, patrón de bandas y posición del centrómero. Para obtener una visión del cariotipo de un individuo, los citólogos fotografían los cromosomas y luego cortan y pegan cada cromosoma en una tabla, o cariograma (Figura\(\PageIndex{1}\)).
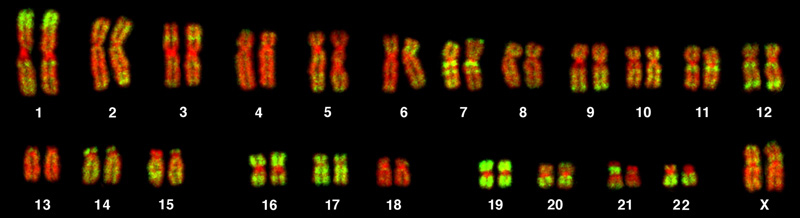
CARRERAS EN ACCIÓN: Los genetistas utilizan cariogramas para identificar aberraciones cromosómicas
El cariotipo es un método mediante el cual se pueden identificar rasgos caracterizados por anomalías cromosómicas a partir de una sola célula. Para observar el cariotipo de un individuo, las células de una persona (como los glóbulos blancos) se extraen primero de una muestra de sangre u otro tejido. En el laboratorio, las células aisladas son estimuladas para comenzar a dividirse activamente. Luego se aplica un químico a las células para detener la mitosis durante la metafase. A continuación, las células se fijan a un portaobjetos.
El genetista luego tiñe los cromosomas con uno de varios tintes para visualizar mejor los patrones de bandas distintos y reproducibles de cada par de cromosomas. Después de la tinción, los cromosomas se visualizan mediante microscopía de campo brillante. Un citogenetista experimentado puede identificar cada banda. Además de los patrones de bandas, los cromosomas se identifican aún más sobre la base del tamaño y la ubicación del centrómero. Para obtener la representación clásica del cariotipo en la que se alinean pares homólogos de cromosomas en orden numérico de mayor a menor, el genetista obtiene una imagen digital, identifica cada cromosoma y organiza manualmente los cromosomas en este patrón (Figura\(\PageIndex{1}\)).
En su forma más básica, el cariograma puede revelar anomalías genéticas en las que un individuo tiene demasiados o muy pocos cromosomas por célula. Ejemplos de ello son el síndrome de Down, que se identifica por una tercera copia del cromosoma 21, y el síndrome de Turner, que se caracteriza por la presencia de un solo cromosoma X en mujeres en lugar de dos. Los genetistas también pueden identificar grandes deleciones o inserciones de ADN. Por ejemplo, el síndrome de Jacobsen, que involucra rasgos faciales distintivos así como defectos cardíacos y hemorrágicos, se identifica por una deleción en el cromosoma 11. Finalmente, el cariotipo puede identificar translocaciones, que ocurren cuando un segmento de material genético se rompe de un cromosoma y se vuelve a unir a otro cromosoma o a una parte diferente del mismo cromosoma. Las translocaciones están implicadas en ciertos cánceres, incluyendo la leucemia mielógena crónica.
Al observar un cariograma, los genetistas pueden visualizar realmente la composición cromosómica de un individuo para confirmar o predecir anomalías genéticas en la descendencia incluso antes del nacimiento.
No disyunciones, duplicaciones y eliminaciones
De todos los trastornos cromosómicos, las anomalías en el número de cromosomas son las más fácilmente identificables a partir de un cariograma. Los trastornos del número de cromosomas incluyen la duplicación o pérdida de cromosomas completos, así como cambios en el número de conjuntos completos de cromosomas. Son causadas por la no disyunción, que ocurre cuando pares de cromosomas homólogos o cromátidas hermanas no logran separarse durante la meiosis. El riesgo de no disyunción aumenta con la edad de los padres.
La no disyunción puede ocurrir durante la meiosis I o II, con diferentes resultados (Figura\(\PageIndex{2}\)). Si los cromosomas homólogos no logran separarse durante la meiosis I, el resultado son dos gametos que carecen de ese cromosoma y dos gametos con dos copias del cromosoma. Si las cromátidas hermanas no logran separarse durante la meiosis II, el resultado es un gameto que carece de ese cromosoma, dos gametos normales con una copia del cromosoma y un gameto con dos copias del cromosoma.
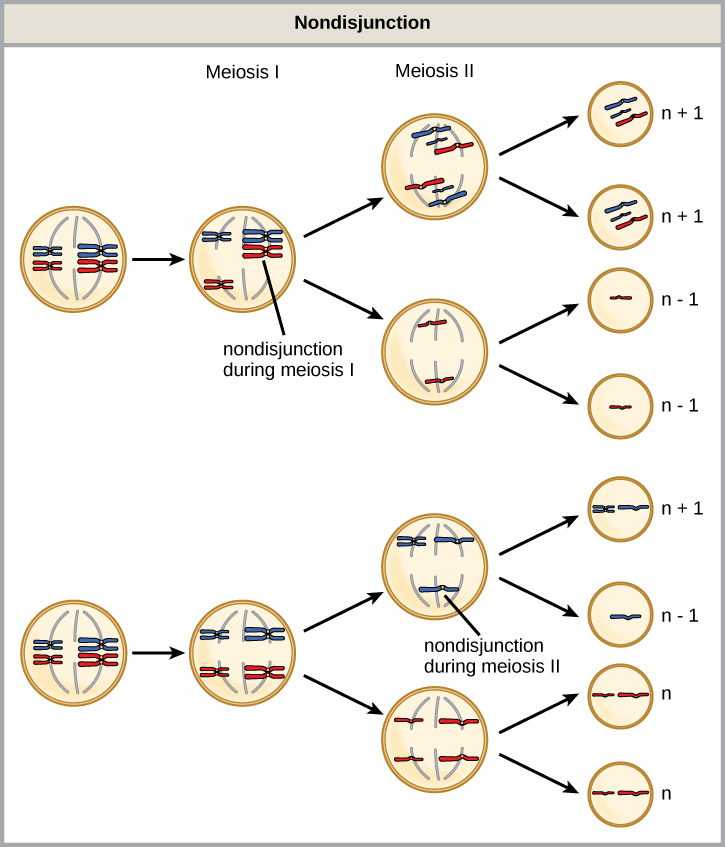
Un individuo con el número apropiado de cromosomas para su especie se llama euploide; en humanos, la euploidía corresponde a 22 pares de autosomas y un par de cromosomas sexuales. Un individuo con un error en el número de cromosomas se describe como aneuploide, término que incluye monosomía (pérdida de un cromosoma) o trisomía (ganancia de un cromosoma extraño). Los cigotos humanos monosómicos que carecen de una sola copia de un autosoma invariablemente no logran desarrollarse hasta nacer porque solo tienen una copia de genes esenciales. La mayoría de las trisomías autosómicas tampoco logran desarrollarse hasta el nacimiento; sin embargo, las duplicaciones de algunos de los cromosomas más pequeños (13, 15, 18, 21 o 22) pueden resultar en crías que sobreviven de varias semanas a muchos años. Los individuos trisómicos sufren de un tipo diferente de desequilibrio genético: un exceso en la dosis génica. Las funciones celulares se calibran a la cantidad de producto génico producido por dos copias (dosis) de cada gen; agregar una tercera copia (dosis) altera este equilibrio. La trisomía más común es la del cromosoma 21, que conduce al síndrome de Down. Los individuos con este trastorno hereditario tienen rasgos físicos característicos y retrasos en el desarrollo en el crecimiento y la cognición. La incidencia del síndrome de Down se correlaciona con la edad materna, de tal manera que las mujeres mayores tienen más probabilidades de dar a luz a niños con síndrome de Down (Figura\(\PageIndex{3}\)).
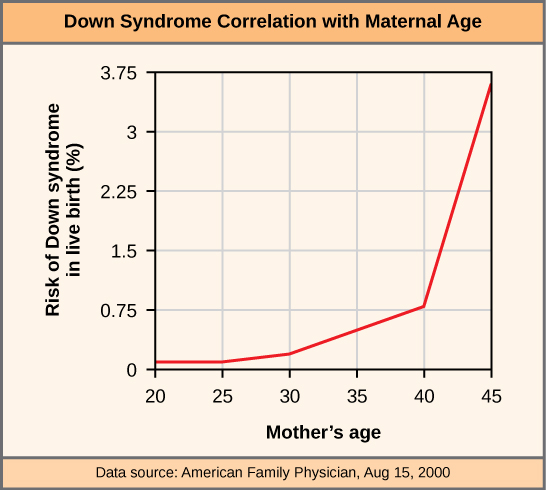
CONCEPT EN ACCIÓN
Visualiza la adición de un cromosoma que conduce al síndrome de Down en esta videosimulación.
Los humanos muestran dramáticos efectos deletéreos con trisomías y monosomías autosómicas. Por lo tanto, puede parecer contradictorio que las hembras y los machos humanos puedan funcionar normalmente, a pesar de portar diferentes números del cromosoma X. En parte, esto ocurre debido a un proceso llamado inactivación X. Temprano en el desarrollo, cuando los embriones de mamífero hembra constan de apenas unos pocos miles de células, un cromosoma X en cada célula se inactiva condensándose en una estructura llamada cuerpo Barr. Los genes en el cromosoma X inactivo no se expresan. El cromosoma X particular (derivado materna o paterno) que se inactiva en cada célula es aleatorio, pero una vez que se produce la inactivación, todas las células que descienden de esa célula tendrán el mismo cromosoma X inactivo. Por este proceso, las hembras compensan su doble dosis genética del cromosoma X.
En los gatos llamados “carey”, se observa la inactivación de X como variegación de color de capa (Figura\(\PageIndex{4}\)). Las hembras heterocigóticas para un gen de color de pelaje ligado al X expresarán uno de los dos colores de pelaje diferentes en diferentes regiones de su cuerpo, correspondientes a cualquier cromosoma X que esté inactivado en el progenitor de células embrionarias de esa región. Cuando veas a un gato carey, sabrás que tiene que ser hembra.

En un individuo que porta un número anormal de cromosomas X, los mecanismos celulares inactivarán todas menos una X en cada una de sus células. Como resultado, las anomalías del cromosoma X suelen estar asociadas con defectos mentales y físicos leves, así como esterilidad. Si el cromosoma X está completamente ausente, el individuo no se desarrollará.
Se han caracterizado varios errores en el número de cromosomas sexuales. Los individuos con tres cromosomas X, llamados triplo-X, aparecen femeninos pero expresan retrasos en el desarrollo y fertilidad reducida. El complemento cromosómico XXY, correspondiente a un tipo de síndrome de Klinefelter, corresponde a individuos masculinos con testículos pequeños, senos agrandados y vello corporal reducido. El cromosoma X extra sufre inactivación para compensar el exceso de dosis genética. El síndrome de Turner, caracterizado como complemento cromosómico X0 (es decir, un solo cromosoma sexual), corresponde a un individuo femenino con baja estatura, piel palmeada en la región del cuello, deficiencias auditivas y cardíacas y esterilidad.
Un individuo con más del número correcto de conjuntos de cromosomas (dos para especies diploides) se llama poliploide. Por ejemplo, la fertilización de un óvulo diploide anormal con un espermatozoide haploide normal produciría un cigoto triploide. Los animales poliploides son extremadamente raros, con solo algunos ejemplos entre los gusanos planos, crustáceos, anfibios, peces y lagartos. Los animales triploides son estériles porque la meiosis no puede proceder normalmente con un número impar de conjuntos de cromosomas. En contraste, la poliploidía es muy común en el reino vegetal, y las plantas poliploides tienden a ser más grandes y robustas que las euploides de sus especies.
Reordenamientos estructurales cromosómicos
Los citólogos han caracterizado numerosos reordenamientos estructurales en cromosomas, incluyendo duplicaciones parciales, deleciones, inversiones y translocaciones. Las duplicaciones y deleciones suelen producir descendencia que sobrevive pero presenta anomalías físicas y mentales. Cri-du-Chat (del francés para “grito del gato”) es un síndrome asociado con anomalías del sistema nervioso y características físicas identificables que resulta de una deleción de la mayor parte del brazo pequeño del cromosoma 5 (Figura\(\PageIndex{5}\)). Los bebés con este genotipo emiten un grito agudo característico en el que se basa el nombre del trastorno.
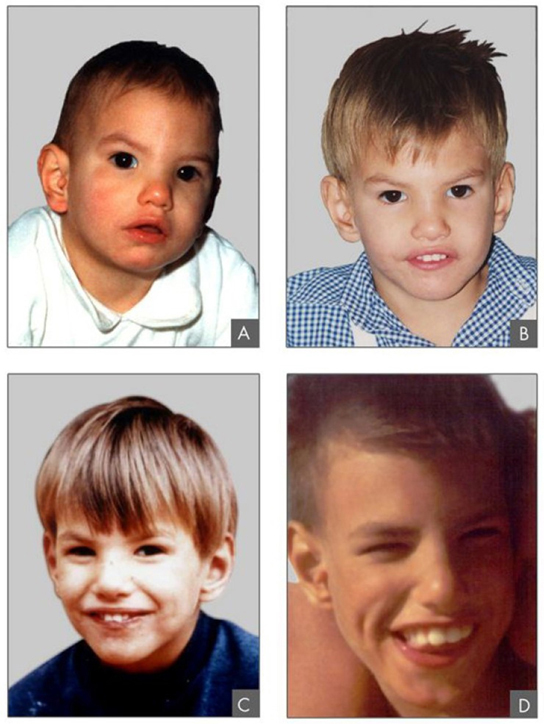
Las inversiones y translocaciones cromosómicas se pueden identificar observando las células durante la meiosis porque los cromosomas homólogos con un reordenamiento en uno de los pares deben contorsionarse para mantener el alineamiento génico apropiado y emparejarse eficazmente durante la profase I.
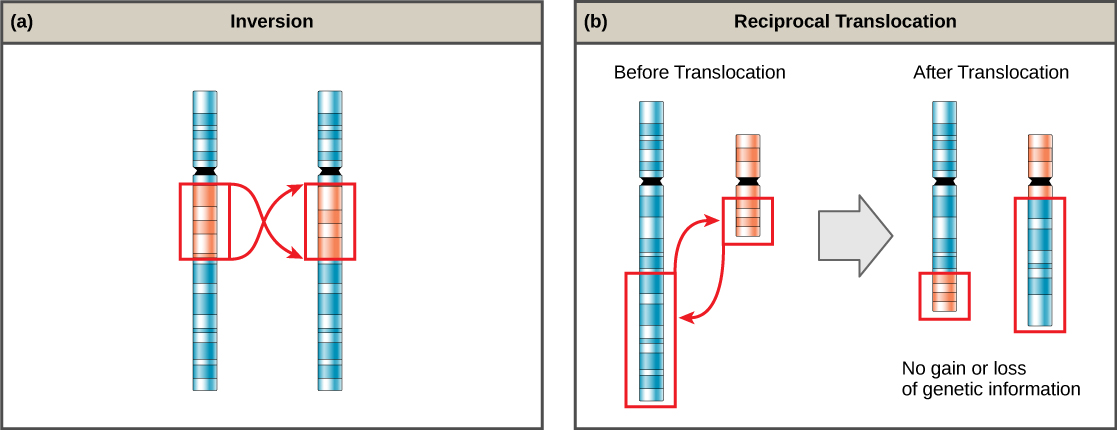
Una inversión cromosómica es el desprendimiento, rotación de 180° y reinserción de parte de un cromosoma (Figura\(\PageIndex{6}\)). A menos que interrumpan una secuencia génica, las inversiones solo cambian la orientación de los genes y es probable que tengan efectos más leves que los errores aneuploides.
EVOLUCIÓN EN ACCIÓN: La inversión del cromosoma 18
No todos los reordenamientos estructurales de los cromosomas producen individuos inviables, deteriorados o infértiles. En raras ocasiones, tal cambio puede resultar en la evolución de una nueva especie. De hecho, una inversión en el cromosoma 18 parece haber contribuido a la evolución de los humanos. Esta inversión no está presente en nuestros parientes genéticos más cercanos, los chimpancés.
Se cree que la inversión del cromosoma 18 ocurrió en los primeros humanos después de su divergencia de un ancestro común con chimpancés hace aproximadamente cinco millones de años. Los investigadores han sugerido que un largo tramo de ADN se duplicó en el cromosoma 18 de un antepasado de humanos, pero que durante la duplicación se invirtió (insertado en el cromosoma en orientación inversa.
Una comparación de genes humanos y chimpancé en la región de esta inversión indica que dos genes, ROCK1 y USP14, están más separados en el cromosoma 18 humano que en el cromosoma del chimpancé correspondiente. Esto sugiere que uno de los puntos de ruptura de inversión ocurrió entre estos dos genes. Curiosamente, los humanos y los chimpancés expresan USP14 a distintos niveles en tipos celulares específicos, incluyendo células corticales y fibroblastos. Quizás la inversión del cromosoma 18 en un humano ancestral reposicionó genes específicos y restablecía sus niveles de expresión de manera útil. Debido a que tanto ROCK1 como USP14 codifican enzimas, un cambio en su expresión podría alterar la función celular. No se sabe cómo esta inversión contribuyó a la evolución de los homínidos, pero parece ser un factor significativo en la divergencia de los humanos de otros primates. 1
Una translocación ocurre cuando un segmento de un cromosoma se disocia y se vuelve a unir a un cromosoma diferente, no homólogo. Las translocaciones pueden ser benignas o tener efectos devastadores, dependiendo de cómo se alteren las posiciones de los genes con respecto a las secuencias reguladoras. En particular, las translocaciones específicas se han asociado con varios cánceres y con esquizofrenia. Las translocaciones recíprocas resultan del intercambio de segmentos cromosómicos entre dos cromosomas no homólogos de tal manera que no hay ganancia o pérdida de información genética (Figura\(\PageIndex{6}\)).
Resumen de la Sección
El número, tamaño, forma y patrón de bandas de los cromosomas los hacen fácilmente identificables en un cariograma y permiten la evaluación de muchas anomalías cromosómicas. Los trastornos en el número de cromosomas, o aneuploidías, suelen ser letales para el embrión, aunque algunos genotipos trisómicos son viables. Debido a la inactivación de X, las aberraciones en los cromosomas sexuales suelen tener efectos más leves en un individuo. Las aneuploidías también incluyen casos en los que los segmentos de un cromosoma se duplican o eliminan. Las estructuras cromosómicas también se pueden reorganizar, por ejemplo, mediante inversión o translocación. Ambas aberraciones pueden tener efectos negativos sobre el desarrollo o la muerte. Debido a que obligan a los cromosomas a asumir emparejamientos contorsionados durante la meiosis I, las inversiones y translocaciones a menudo se asocian con una fertilidad reducida debido a la probabilidad de no disyunción.
Notas al pie
- 1 V Goidts, et al., “Duplicación segmentaria asociada con la inversión específica humana del cromosoma 18: un ejemplo más del impacto de las duplicaciones segmentarias en la evolución del cariotipo y genoma en primates”, Human Genetics, 115 (2004) :116—22.
Glosario
- aneuploide
- un individuo con un error en el número de cromosomas; incluye deleciones y duplicaciones de segmentos cromosómicos
- autosome
- cualquiera de los cromosomas no sexuales
- inversión cromosómica
- el desprendimiento, rotación de 180° y reinserción de un brazo cromosómico
- euploide
- un individuo con el número apropiado de cromosomas para su especie
- cariograma
- la imagen fotográfica de un cariotipo
- cariotipo
- el número y la apariencia de los cromosomas individuales, incluyendo el tamaño, los patrones de bandas y la posición del centrómero
- monosomía
- un genotipo diploide en el que falta un cromosoma
- no disyunción
- el fracaso de los homólogos sinapsados para separarse completamente y migrar a polos separados durante la primera división celular de la meiosis
- poliploide
- un individuo con un número incorrecto de conjuntos de cromosomas
- translocación
- el proceso por el cual un segmento de un cromosoma se disocia y se vuelve a unir a un cromosoma diferente no homólogo
- trisomía
- un genotipo diploide en el que se duplica un cromosoma completo
- X inactivación
- la condensación de cromosomas X en cuerpos de Barr durante el desarrollo embrionario en hembras para compensar la doble dosis genética


