2.2:La evolución de la teoría atómica
( \newcommand{\kernel}{\mathrm{null}\,}\)
Habilidades para desarrollar
- Describir el desarrollo de la teoría atómica moderna
- Resumir e interpretar los resultados de los experimentos de Thomson, Millikan, y Rutherford
- Describir las tres partículas subatómicas que componen los átomos.
- Definir isótopos y dar ejemplos de varios elementos.
En los dos siglos desde que Dalton desarrolló sus ideas, los científicos han logrado avances significativos en nuestra comprensión sobre la teoría atómica. Muchos de estos desarrollos vinieron de los resultados de varios experimentos seminales que enseñaron los detalles de la estructura interna de los átomos. Aquí, discutiremos algunos de esos desarrollos claves, con un énfasis en la aplicación del método científico y un énfasis en la comprensión de cómo se analizó la evidencia experimental. Mientras las personas y fechas históricas detrás de estos experimentos pueden ser bastante interesantes, es muy importante entender los conceptos que resultaron de sus trabajos.
La Teoría Atómica Después del Siglo Diecinueve
Si la materia estuviera compuesta de átomos, ¿De qué estaban compuestos los átomos? ¿Eran las partículas más pequeñas, o había algo más pequeño? A fines de 1800, varios científicos interesados en preguntas como estas investigaron las descargas eléctricas que se podían producir en gases de baja presión, con el descubrimiento más importante realizado por el físico inglés J. J. Thomson, quien utilizó un tubo de rayos catódicos. Este aparato consistía en un tubo de vidrio sellado del cual se le había eliminado casi todo el aire; el tubo contenía dos electrodos metálicos. Cuando se aplicaba alto voltaje a través de los electrodos, aparecía un haz visible llamado rayo catódico entre ellos. Este haz se desvió hacia la carga positiva y se alejó de la carga negativa, y se produjo de la misma manera con propiedades idénticas cuando se usaban diferentes metales para los electrodos. En experimentos similares, el rayo se desvió simultáneamente por un campo magnético aplicado, y las mediciones de la extensión de la desviación y la intensidad del campo magnético le permitieron a Thomson calcular la relación carga-masa de las partículas de rayo catódico. Los resultados de estas mediciones indicaron que estas partículas eran mucho más ligeras que los átomos. (Figure 2.2.1).

Según sus observaciones, esto es lo que Thomson propuso y por qué lo propuso: las partículas son atraídas por cargas positivas (+) y repeladas por las cargas negativas (-), por eso deben ser cargadas negativamente (las cargas iguales se repelan y las cargas diferentes se atraen); son menos masivas que los átomos y son indistinguibles, independientemente del material de origen, por eso deben ser constituyentes fundamentales y subatómicos de todos los átomos. Aunque fue una controversia en ese momento, la idea de Thomson fue aceptada gradualmente, y su partícula de rayos catódicos es lo que ahora llamamos un electrón, una partícula subatómica cargada negativamente con una masa más de mil veces menos que la de un átomo. El término "electrón" fue acuñado en 1891 por el físico irlandés George Stoney, de "ión eléctrico".
En 1909, el físico estadounidense Robert A. Millikan descubrió más información sobre el electrón a través de sus experimentos de "gota de aceite". Millikan creó gotas microscópicas de aceite, que se podían cargar eléctricamente por fricción cuando se formaban o cuando se usaban rayos X. Estas gotitas inicialmente cayeron debido a la gravedad, pero su progreso hacia abajo podría ser frenado o revertido por un campo eléctrico que estaba más bajo en el aparato. Al ajustar la intensidad del campo eléctrico y al hacer mediciones cuidadosas y cálculos apropiados, Millikan pudo determinar la carga en gotas individuales. (Figure 2.2.2).
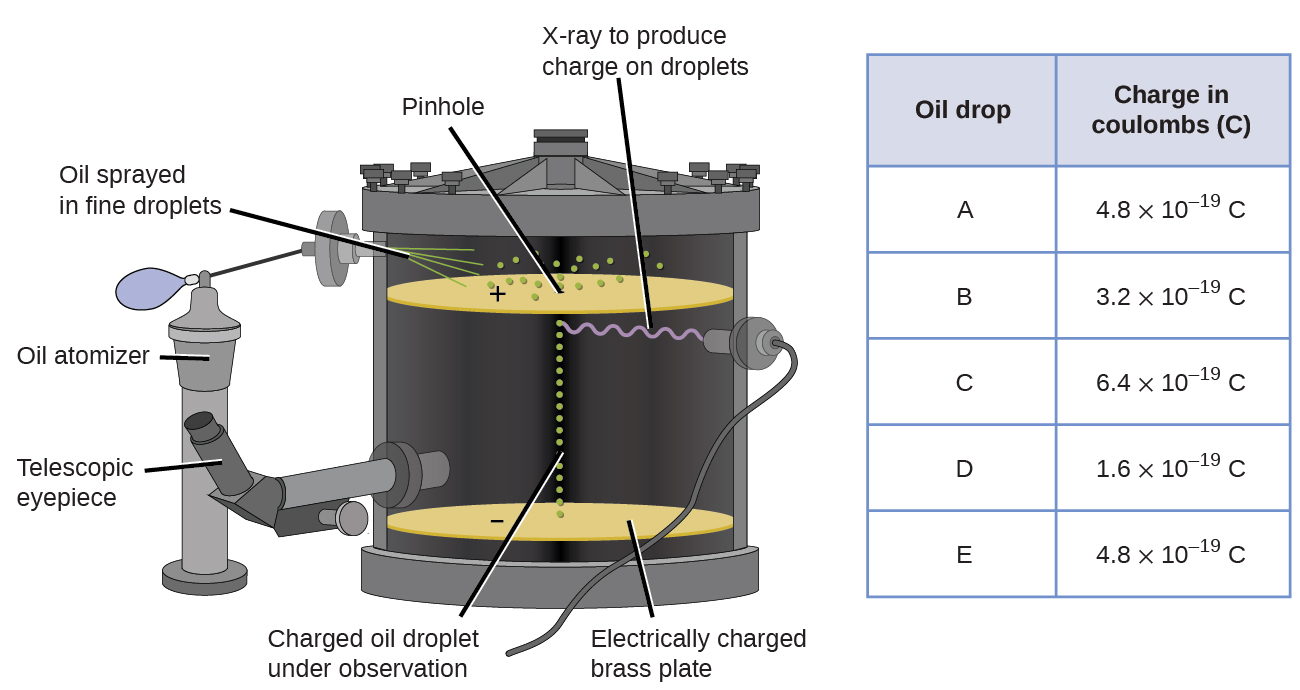
Al observar los datos de carga que Millikan colecto, es posible que usted haya reconocido que la carga de una gota de aceite es siempre un múltiplo de una carga específica, 1,6 × 10 -19 C. Millikan concluyó que este valor tenía que ser una carga fundamental —la carga de un solo electrón— con sus cargas medidas debidas a un exceso de un electrón (1 veces 1,6 × 10 -19 C), dos electrones (2 veces 1,6 × 10 -19 C), tres electrones (3 veces 1,6 × 10 -19 C), y así sucesivamente, en una gota de aceite dada. Ya que la carga de un electrón ahora se conocía debido a la investigación de Millikan, y la relación carga-masa ya se conocía debido a la investigación de Thomson (1,759 × 10 11 C/kg), solo se necesitaba un cálculo simple para determinar la masa del electrón también.
Massofelectron=1.602×10−19C×1kg1.759×1011C=9.107×10−31kg
Científicos habían establecido que el átomo no era indivisible como Dalton había creído, y debido al trabajo de Thomson, Millikan y otros, se conocía la carga y la masa de las partículas subatómicas negativas - los electrones. Sin embargo, la parte positivamente cargada de un átomo aún no se entendía bien. En 1904, Thomson propuso el modelo de átomos de "pudín de ciruela", que describía una masa cargada positivamente con una cantidad igual de carga negativa en forma de electrones incustrados en ella, ya que todos los átomos son eléctricamente neutros. Un modelo competitivo fue propuesto en 1903 por Hantaro Nagaoka, quien postuló un átomo similar a Saturno, que consistía en una esfera cargada positivamente rodeada por un halo de electrones. (Figura 2.2.3).
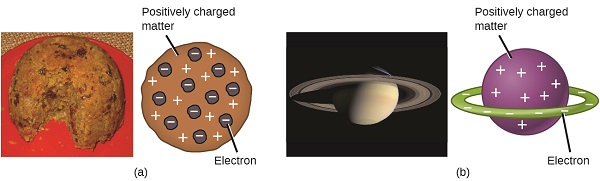
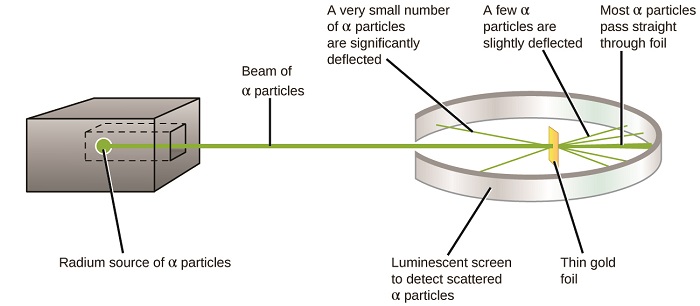
El siguiente gran avance en la comprensión del átomo vino de Ernest Rutherford, un físico de Nueva Zelanda que pasó su carrera científica en Canadá y en Inglaterra. Realizó una serie de experimentos usando un haz de partículas alfa de alta velocidad y cargadas positivamente (partículas α) que fueron producidas por la descomposición radioactiva del radio; las partículas α consisten en dos protones y dos neutrones (aprenderá más sobre la desintegración radiactiva en el capítulo sobre química nuclear). Rutherford y sus colegas Hans Geiger (se hizo famoso luego por el contador Geiger) y Ernest Marsden apuntaron un haz de partículas α, su fuente estaba incrustada en un bloque de plomo para absorber la mayor parte de la radiación, en una pieza muy delgada de lámina de oro. El examinó la dispersión resultante de las partículas α usando una pantalla luminiscente que brillaba brevemente al ser golpeada por una partícula α.
¿Qué descubrieron? La mayoría de las partículas pasaron a través de la lámina sin ser desviadas. Sin embargo, algunos se desviaron un poco y un número muy pequeño se desviaron casi directamente hacia la fuente (Figura 2.2.4). Rutherford describió el hallazgo de estos resultados: “Fue el evento más increíble que me haya sucedido en mi vida. Fue casi tan increíble como si hubiera disparado una cascara de 15 pulgadas a un trozo de papel de seda y te volvería a golpear "1 (p. 68).
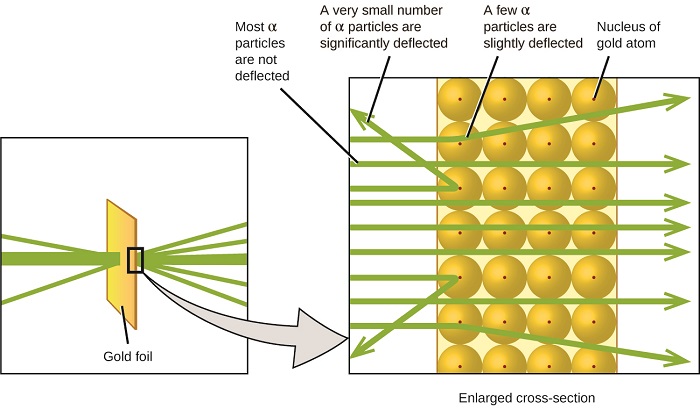
Esto es lo que Rutherford dedujo: porque la mayoría de las partículas α en movimiento rápido pasaron a través de los átomos de oro sin desviarse, deben haber viajado a través del espacio esencialmente vacío dentro del átomo. Las partículas alfa están cargadas positivamente, por eso desviaciones pasaron cuando se encontraron con otra carga positiva (las cargas iguales se repelen la una a la otra). Como las cargas iguales se repelen la una a la otra, las pocas partículas α cargadas positivamente que cambiaron de manera abrupta deben haber golpeado, o acercado se, a otra cosa que también tenía una carga positiva que estaba altamente concentrada. Dado que las desviaciones ocurrieron solo una pequeña fracción del tiempo, esta carga solo ocupó una pequeña cantidad de espacio en la lámina de oro. Analizando una serie de experimentos en detalle, Rutherford sacó dos conclusiones:
1. El volumen ocupado por un átomo debe consistir en una gran cantidad de espacio vacío.
2. Un cuerpo pequeño cargado positivamente, relativamente pesado, el núcleo, debe estar en el centro de cada átomo.
Este análisis llevó Rutherford a proponer un modelo en el que un átomo tiene un núcleo muy pequeño, cargado positivamente, en el que se concentra la mayor parte de la masa del átomo, rodeado de electrones con carga negativa, para que el átomo sea eléctricamente neutro. (Figura 2.2.5).
Después de muchos más experimentos, Rutherford también descubrió que los núcleos de otros elementos contienen el núcleo de hidrógeno como un "bloque de construcción", él llamó esta partícula fundamental el protón, la partícula subatómica cargada positivamente que se encuentra en el núcleo. Con una adición, que usted aprenderá siguiente mente, este modelo nuclear del átomo, propuesto hace más de un siglo, todavía se usa hoy.
Otro descubrimiento importante fue el descubrimiento de isótopos. A principios de la década de 1900, los científicos identificaron varias sustancias que parecían ser elementos nuevos, aislándolos de los minerales radiactivos. Por ejemplo, un "nuevo elemento" producido por la desintegración radiactiva del torio se llamó mesothorium inicialmente. Sin embargo, un análisis más detallado mostró que el mesothorio era químicamente idéntico al radio (otro producto de desintegración), a pesar de tener una masa atómica diferente. Este resultado, junto con descubrimientos similares para otros elementos, llevó al químico inglés Frederick Soddy a darse cuenta de que un elemento podía tener tipos de átomos con diferentes masas que no se distinguían químicamente. Estos diferentes tipos se llaman isótopos, átomos del mismo elemento que difieren en masa. Soddy recibió el Premio Nobel de Química en 1921 por este descubrimiento.
Quedó un problema: se sabía que el núcleo contenía casi toda la masa de un átomo, con el número de protones que solo daba la mitad, o menos, de esa masa. Se hicieron diferentes propuestas para explicar qué constituía la masa que sobraba, incluyendo la existencia de partículas neutras en el núcleo. Como es de esperar, la detección de partículas sin carga es un gran desafío, y no fue hasta 1932 cuando James Chadwick encontró evidencia de neutrones, partículas subatómicas sin carga con una masa aproximadamente igual a la de los protones. La existencia del neutrón también explicó los isótopos: difieren en masa porque tienen diferentes números de neutrones, pero son químicamente idénticos porque tienen el mismo número de protones. Esto se explicará con más detalle más adelante en este capítulo.
Resumen
Aunque nadie ha visto el interior de un átomo, experimentos han demostrado mucho sobre la estructura atómica. El tubo de rayos catódicos de Thomson mostró que los átomos contienen pequeñas partículas con carga negativa que se llaman electrones. Millikan descubrió que hay una carga eléctrica fundamental: la carga de un electrón. El experimento de la lámina de oro de Rutherford mostró que los átomos tienen un núcleo pequeño, denso y cargado positivamente; las partículas cargadas positivamente dentro del núcleo se llaman protones. Chadwick descubrió que el núcleo también contiene partículas neutrales que se llaman neutrones. Soddy demostró que los átomos del mismo elemento pueden tener masa diferente; estos se llaman isótopos.
Notas al Pie de la Página
- Ernest Rutherford, "El Desarrollo de la Teoría de la Estructura Atómica", ed. J.A. Ratcliffe, en Background to Modern Science, eds. Joseph Needham y Walter Pagel, (Cambridge, Reino Unido: Cambridge University Press,1938), 61–74. Accedido el 22 de Septiembre del 2014, https://ia600508.us.archive.org/3/it...e032734mbp.pdf.
Glosario
- Partícula alfa (partícula α)
- Partícula con carga positiva que consiste en dos protones y dos neutrones.
- electrón
- Partícula subatómica con carga negativa y masa relativamente baja encontrada afuera del núcleo.
- isótopos
- Átomos que contienen el mismo número de protones, pero diferentes números de neutrones.
- neutrón
- Partícula subatómica que no está cargada encontrada en el núcleo.
- protón
- Partícula subatómica con carga positiva encontrada en el núcleo.
- núcleo
- Centro masivo y cargado positivamente de un átomo que contiene protones y neutrones.
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


