7.3: Símbolos y estructuras de Lewis
- Page ID
- 1855
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\(\newcommand{\longvect}{\overrightarrow}\)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)habilidades para desarrollar
- Escribir los símbolos de Lewis para los átomos e iones neutrales.
- Dibujar las estructuras de Lewis que representan la unión en moléculas simples.
Hasta ahora, hemos discutido los diversos tipos de enlaces que se forman entre los átomos y / o los iones. En todos los casos, estos enlaces involucran compartir o transferir los electrones de la capa de valencia entre los átomos. En esta sección, exploraremos el método típico para representar electrones de capa de valencia y enlaces químicos, los símbolos de Lewis y las estructuras de Lewis.
Símbolos de Lewis
Usamos los símbolos de Lewis para describir las configuraciones electrónicas de valencia de los átomos y los iones monoatómicos. Un símbolo de Lewis consiste en un símbolo elemental rodeado por un punto para cada uno de sus electrones de valencia:
![]()
La figura \(\PageIndex{1}\) muestra los símbolos de Lewis para los elementos del tercer período de la tabla periódica. Los puntos de electrones se organizan típicamente en cuatro pares ubicados en los cuatro "lados" del símbolo atómico.
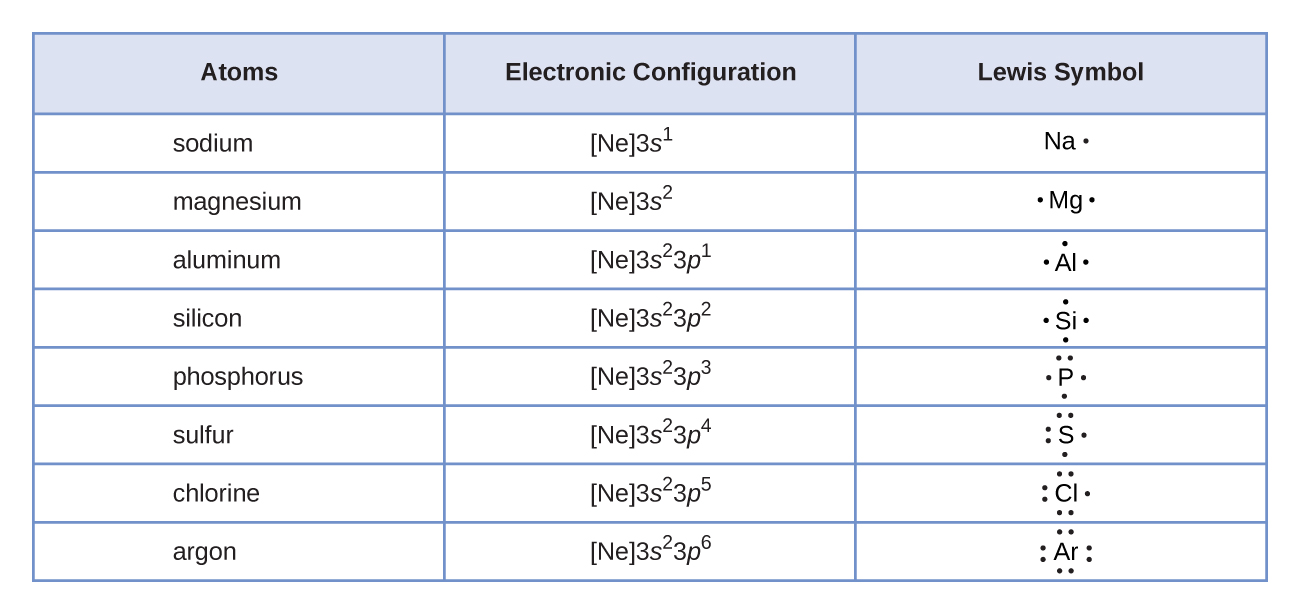
Los símbolos de Lewis se pueden usar para ilustrar la formación de cationes a partir de átomos, como se muestra aquí para el sodio y el calcio:

Del mismo modo, se pueden usar para mostrar la formación de aniones a partir de átomos, como se muestra aquí para el cloro y el azufre:

La figura \(\PageIndex{2}\) demuestra el uso de los símbolos de Lewis para mostrar la transferencia de electrones durante la formación de compuestos iónicos.
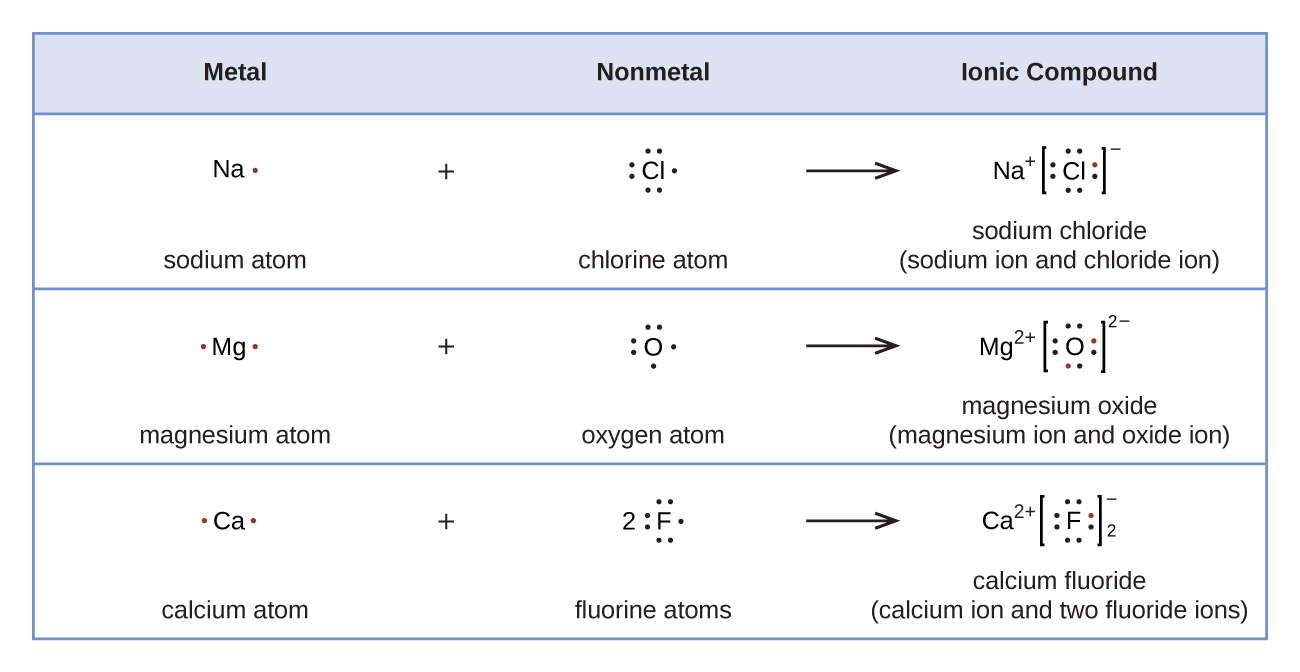
Estructuras de Lewis
También usamos los símbolos de Lewis para indicar la formación de enlaces covalentes, que se muestran en las estructuras de Lewis, dibujos que describen el enlace en moléculas e iones poliatómicos. Por ejemplo, cuando dos átomos de cloro forman una molécula de cloro, comparten un par de electrones:
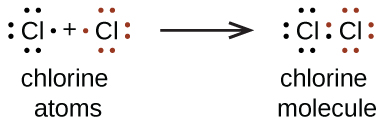
La estructura de Lewis indica que cada átomo de Cl tiene tres pares de electrones que no se usan en la unión (llamados pares solitarios) y un par de electrones compartido (escrito entre los átomos). Un guión (o línea) se usa generalmente para indicar un par compartido de electrones:
![]()
En el modelo de Lewis, un solo par de electrones compartido es un enlace simple. Cada átomo de Cl interactúa con un total de ocho electrones de valencia: los seis en los pares solitarios y los dos en el enlace simple.
La regla del octeto
Las otras moléculas de halógeno (F2, Br2, I2 y At2) forman enlaces como los de la molécula de cloro: un enlace simple entre los átomos y tres pares de electrones por cada átomo. Esto permite que cada átomo de halógeno tenga una configuración electrónica de gas noble. La tendencia de los átomos del grupo principal a formar suficientes enlaces para obtener ocho electrones de valencia se conoce como la regla del octeto.
A menudo, el número de enlaces que puede formar un átomo se puede predecir a partir del número de electrones necesarios para alcanzar un octeto (ocho electrones de valencia); esto es especialmente cierto para los no metales del segundo período de la tabla periódica (C, N, O y F). Por ejemplo, cada átomo de un elemento del grupo 14 tiene cuatro electrones en su capa más externa y, por lo tanto, requiere cuatro electrones más para alcanzar un octeto. Estos cuatro electrones se pueden obtener formando cuatro enlaces covalentes, como se ilustra aquí para el carbono en CCl4 (tetracloruro de carbono) y silicio en SiH4 (silano). Debido a que el hidrógeno solo necesita dos electrones para llenar su capa de valencia, es una excepción a la regla del octeto y solo necesita formar un enlace. Los elementos de transición y los elementos de transición internos tampoco siguen la regla del octeto, ya que tienen electrones d y f involucrados en sus capas de valencia.
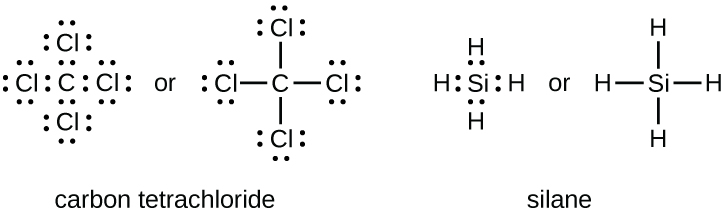
Los elementos del grupo 15, como el nitrógeno, tienen cinco electrones de valencia en el símbolo atómico de Lewis: un par solitario y tres electrones no apareados. Para obtener un octeto, estos átomos forman tres enlaces covalentes, como en NH3 (amoníaco). El oxígeno y otros átomos en el grupo 16 obtienen un octeto formando dos enlaces covalentes:
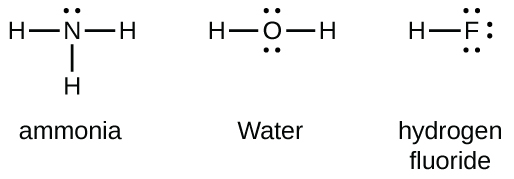
Los enlaces dobles y triples
Como se mencionó anteriormente, cuando un par de átomos comparte un par de electrones, es un enlace simple. Sin embargo, un par de átomos puede necesitar compartir más de un par de electrones para lograr el octeto requerido. Un doble enlace se forma cuando dos pares de electrones se comparten entre un par de átomos, como entre los átomos de carbono y oxígeno en CH2O (formaldehído) y entre los dos átomos de carbono en C2H4 (etileno):
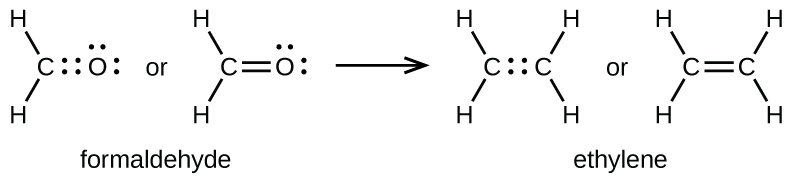
Un enlace triple se forma cuando tres pares de electrones se comparten por un par de átomos, como en el monóxido de carbono (CO) y el ion cianuro (CN-):
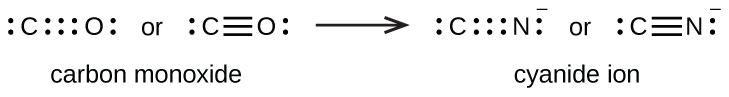
Escritura de estructuras de Lewis con la regla del octeto
Para moléculas muy simples e iones moleculares, podemos escribir las estructuras de Lewis simplemente emparejando los electrones no apareados en los átomos constituyentes. Vea estos ejemplos:
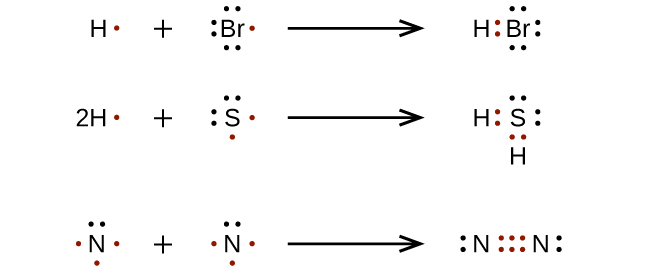
- Determine el número total de electrones de valencia (capa externa) entre todos los átomos. Para los cationes, reste un electrón por cada carga positiva. Para los aniones, agregue un electrón por cada carga negativa.
- Dibuje una estructura esquelética de la molécula o ion, organizando los átomos alrededor de un átomo central. (En general, el elemento menos electronegativo se debe colocar en el centro).
- Conecte cada átomo al átomo central con un solo enlace (un par de electrones).
- Distribuye los electrones restantes como pares solitarios en los átomos terminales (excepto el hidrógeno), completando un octeto alrededor de cada átomo.
- Coloque todos los electrones restantes en el átomo central.
- Reorganice los electrones de los átomos externos para hacer enlaces múltiples con el átomo central para obtener octetos siempre que sea posible.
Determinemos las estructuras de Lewis de SiH4, \(\ce{CHO2-}\), NO+ y OF2 como ejemplos en el siguiente procedimiento:
- Determine el número total de electrones de valencia (capa externa) en la molécula o el ion.
- Para una molécula, agregamos el número de electrones de valencia en cada átomo en la molécula:
\(\begin{align} &\phantom{+}\ce{SiH4}\\ &\phantom{+}\textrm{Si: 4 valence electrons/atom × 1 atom = 4}\\ &\underline{\textrm{+H: 1 valence electron/atom × 4 atoms = 4}}\\ &\hspace{271px}\textrm{= 8 valence electrons} \end{align}\)
- Para un ion negativo, como \(\ce{CHO2-}\), agregamos el número de electrones de valencia en los átomos al número de cargas negativas en el ion (se gana un electrón por cada carga negativa):
\(\ce{CHO2-}\\
\textrm{C: 4 valence electrons/atom × 1 atom} \hspace{6px}= \phantom{1}4\\
\textrm{H: 1 valence electron/atom × 1 atom} \hspace{12px}= \phantom{1}1\\
\textrm{O: 6 valence electrons/atom × 2 atoms = 12}\\
\underline{+\hspace{100px}\textrm{1 additional electron} \hspace{9px}= \phantom{1}1}\\
\hspace{264px}\textrm{= 18 valence electrons}\) - Para un ion positivo, como NO+, sumamos el número de electrones de valencia en los átomos en el ion y luego restamos el número de cargas positivas en el ion (se pierde un electrón por cada carga positiva única) del número total de electrones de valencia.
\(\ce{NO+}\\
\textrm{N: 5 valence electrons/atom × 1 atom} = \phantom{−}5\\
\textrm{O: 6 valence electron/atom × 1 atom}\hspace{5px} = \phantom{−}6\\
\underline{\textrm{+ −1 electron (positive charge)} \hspace{44px}= −1}\\
\hspace{260px}\textrm{= 10 valence electrons}\) - Ya que OF2 es una molécula neutra, simplemente agregamos el número de electrones de valencia:
\(\phantom{+ }\ce{OF2}\\
\phantom{+ }\textrm{O: 6 valence electrons/atom × 1 atom} \hspace{10px}= 6\\
\underline{\textrm{+ F: 7 valence electrons/atom × 2 atoms} = 14}\\
\hspace{280px}\textrm{= 20 valence electrons}\)
- Para una molécula, agregamos el número de electrones de valencia en cada átomo en la molécula:
- Dibuje una estructura esquelética de la molécula o el ion, organizando los átomos alrededor de un átomo central y conectando cada átomo al átomo central con un solo enlace (un par de electrones). (Tenga en cuenta que denotamos iones con corchetes alrededor de la estructura, indicando la carga fuera de los corchetes:)
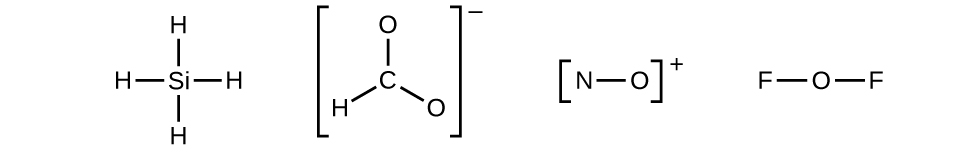
- Cuando varios arreglos de átomos son posibles, como para \(\ce{CHO2-}\), debemos usar evidencia experimental para elegir la estructura correcta. En general, los elementos menos electronegativos son más propensos a ser átomos centrales. En \(\ce{CHO2-}\), el átomo de carbono menos electronegativo ocupa la posición central con los átomos de oxígeno e hidrógeno que lo rodean. Otros ejemplos incluyen P en POCl3, S en SO2 y Cl en \(\ce{ClO4-}\). Una excepción es que el hidrógeno casi nunca es un átomo central. Como el elemento más electronegativo, el flúor tampoco puede ser un átomo central.
- Distribuye los electrones restantes como pares solitarios en los átomos terminales (excepto el hidrógeno) para completar sus capas de valencia con un octeto de electrones.
- No hay electrones restantes en SiH4, por eso no se modifica:
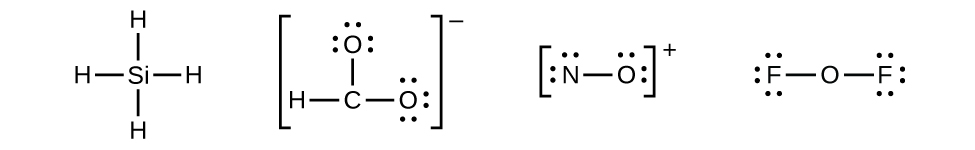
- Coloque todos los electrones restantes en el átomo central.
- Para SiH4, \(\ce{CHO2-}\), y NO+, no quedan electrones; ya colocamos todos los electrones determinados en el Paso 1.
- Para OF2, teníamos 16 electrones restantes en el Paso 3, y colocamos 12, quedando con 4 electrones para colocarlos en el átomo central:
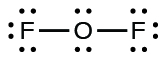
- Reorganice los electrones de los átomos externos para hacer enlaces múltiples con el átomo central para obtener octetos siempre que sea posible.
- SiH4: Si ya tiene un octeto, por eso no hay que hacer nada.
- \(\ce{CHO2-}\): Hemos distribuido los electrones de valencia como pares solitarios en los átomos de oxígeno, pero el átomo de carbono falta de un octeto:
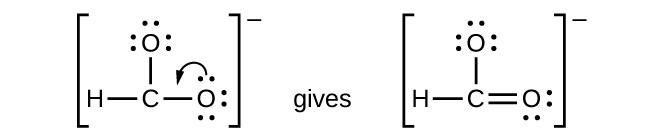
- NO+: Para este ion, agregamos ocho electrones externos, pero ninguno de los átomos tiene un octeto. No podemos agregar más electrones ya que ya hemos usado el total que encontramos en el Paso 1, por lo que debemos mover los electrones para formar un enlace múltiple:
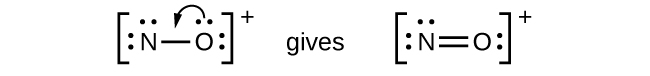
- Esto todavía no produce un octeto, por lo que debemos mover otro par, formando un enlace triple:
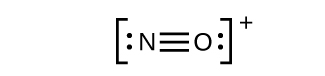
- En OF2, cada átomo tiene un octeto dibujado, por eso nada cambia.
Ejemplo \(\PageIndex{1}\): ESCRITURA DE ESTRUCTURAS DE LEWIS
La misión Cassini-Huygens de NASA detectó una gran nube de cianuro de hidrógeno tóxico (HCN) en Titán, una de las lunas de Saturno. Titan también contiene etano (H3CCH3), acetileno (HCCH) y amoníaco (NH3). ¿Cuáles son las estructuras de Lewis de estas moléculas?
Solución
Calcule el número de electrones de valencia.
- HCN: (1 × 1) + (4 × 1) + (5 × 1) = 10
- H3CCH3: (1 × 3) + (2 × 4) + (1 × 3) = 14
- HCCH: (1 × 1) + (2 × 4) + (1 × 1) = 10
- NH3: (5 × 1) + (3 × 1) = 8
Dibuje un esqueleto y conecte los átomos con enlaces simples. Recuerde que H nunca es un átomo central:
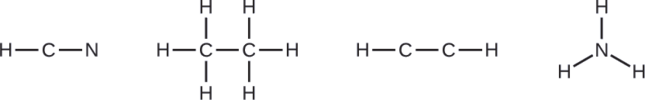
Donde sea necesario, distribuye los electrones a los átomos terminales:
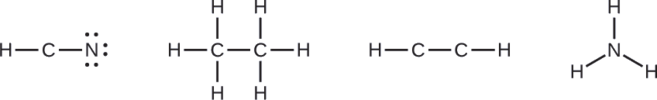
- HCN: seis electrones colocados en N
- H3CCH3: no quedan electrones
- HCCH: no hay átomos terminales capaces de aceptar electrones.
- NH3: no hay átomos terminales capaces de aceptar electrones.
Donde sea necesario, coloque los electrones restantes en el átomo central:
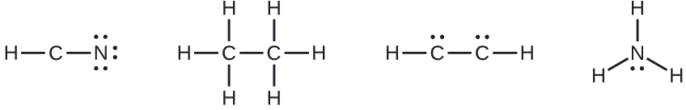
- HCN: no quedan electrones
- H3CCH3: no quedan electrones
- HCCH: cuatro electrones colocados en el carbono
- NH3: dos electrones colocados en nitrógeno
Cuando sea necesario, reorganice los electrones para formar enlaces múltiples con el objetivo de obtener un octeto en cada átomo:
- HCN: forma dos mas enlaces de C–N
- H3CCH3: todos los átomos tienen el número correcto de electrones.
- HCCH: forma un triple enlace entre los dos átomos de carbono.
- NH3: todos los átomos tienen el número correcto de electrones.

Ejercicio \(\PageIndex{1}\)
Tanto el monóxido de carbono, el CO, como el dióxido de carbono, el CO2, son productos de la combustión de combustibles fósiles. Ambos de estos gases también causan problemas: el CO es tóxico y el CO2 se ha implicado en el cambio climático global. ¿Cuáles son las estructuras de Lewis de estas dos moléculas?
- Respuesta
-
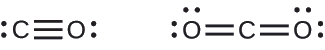
QUIMICA FULLERENO
El hollín de carbono se ha conocido desde tiempos prehistóricos, pero no fue hasta hace bastante poco que se descubrió la estructura molecular del componente principal del hollín. En 1996, el Premio Nobel de Química fue otorgado a Richard Smalley, Robert Curl y Harold Kroto por su trabajo en el descubrimiento de una nueva forma del carbono, el C60 molecula de buckminsterfullereno. Una clase completa de compuestos, incluyendo esferas y tubos de varias formas, fueron descubiertos basados en C60. Este tipo de molécula, llamada el fullereno, consiste en una red compleja de átomos de carbono con enlaces simples y dobles dispuestos de tal manera que cada átomo de carbono obtiene un octeto completo de electrones. Debido a su tamaño y forma, los fullerenos pueden encapsular otras moléculas, por lo que han demostrado potencial en varias aplicaciones, desde el almacenamiento de hidrógeno hasta los sistemas de administración de fármacos dirigidos. También poseen propiedades electrónicas y ópticas únicas que se han usado en dispositivos con energía solar y sensores químicos.
Excepciones a la regla del octeto
Muchas moléculas covalentes tienen átomos centrales que no tienen ocho electrones en sus estructuras de Lewis. Estas moléculas se dividen en tres categorías:
- Las moléculas de electrones impares tienen un número impar de electrones de valencia y, por lo tanto, tienen un electrón no pareado.
- Las moléculas deficientes en electrones tienen un átomo central que tiene menos electrones de los necesarios para una configuración de gas noble.
- Las moléculas hipervalentes tienen un átomo central que tiene más electrones de los necesarios para una configuración de gas noble.
Moléculas de electrones impares
Llamamos las moléculas que contienen un número impar de electrones radicales libres. El óxido nítrico, NO, es un ejemplo de una molécula con electrones impar; se produce en los motores de combustión interna cuando el oxígeno y el nitrógeno reaccionan a altas temperaturas.
Para dibujar la estructura de Lewis para una molécula de electrón impar como NO, seguimos los mismos cinco pasos que seguiríamos para otras moléculas, pero con algunos cambios menores:
- Determine el número total de electrones de valencia (capa externa). La suma de los electrones de valencia es 5 (de N) + 6 (de O) = 11. El número impar nos dice inmediatamente que tenemos un radical libre, por lo que sabemos que no todos los átomos pueden tener ocho electrones en su capa de valencia.
- Dibuje una estructura esquelética de la molécula. Podemos dibujar fácilmente un esqueleto con un enlace sencillo N – O: N – O.
- Distribuye los electrones restantes como pares solitarios en los átomos terminales. En este caso, no hay un átomo central, por lo que distribuimos los electrones alrededor de ambos átomos. Damos ocho electrones al átomo más electronegativo en estas situaciones; así el oxígeno tiene la capa de valencia llena:
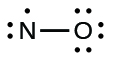
4.Coloque todos los electrones restantes en el átomo central. Dado que no quedan electrones, este paso no se aplica.
5.Reorganice los electrones para hacer enlaces múltiples con el átomo central para obtener octetos siempre que sea posible. Sabemos que una molécula de electrón impar no puede tener un octeto para cada átomo, pero queremos que cada átomo esté lo más cerca posible de un octeto. En este caso, el nitrógeno tiene solo cinco electrones a su alrededor. Para acercarnos a un octeto para el nitrógeno, tomamos uno de los pares solitarios del oxígeno y lo usamos para formar un NO doble enlace. (No podemos tomar otro par de electrones en oxígeno y formar un enlace triple porque el nitrógeno tendría nueve electrones:)
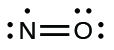
Moléculas deficientes en electrones
También encontraremos algunas moléculas que contienen átomos centrales que no tienen una capa de valencia llena. En general, estas son moléculas con átomos centrales de los grupos 2 y 13 y átomos externos que son hidrógeno u otros átomos que no forman enlaces múltiples. Por ejemplo, en las estructuras de Lewis del dihidruro de berilio, BeH2 y trifluoruro de boro, BF3, los átomos de berilio y boro tienen cada uno solo cuatro y seis electrones, respectivamente. Es posible dibujar una estructura con un enlace doble entre un átomo de boro y un átomo de flúor en BF3, cumpliendo con la regla del octeto, pero la evidencia experimental indica que las longitudes de los enlaces son más cercanas a las esperadas para los enlaces simples B – F. Esto sugiere que la mejor estructura de Lewis tiene tres enlaces simples B – F y un boro deficiente en electrones. La reactividad del compuesto también es consistente con un boro deficiente en electrones. Sin embargo, los enlaces B – F son un poco más cortos de lo que realmente se espera para los enlaces simples B – F, lo que indica que se encuentra algún carácter de doble enlace en la molécula real.
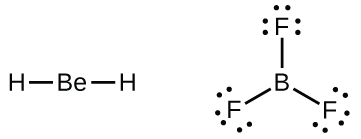
Un átomo como el átomo de boro en BF3, que no tiene ocho electrones, es muy reactivo. Se combina fácilmente con una molécula que contiene un átomo con un solo par de electrones. Por ejemplo, el NH3 reacciona con BF3 porque el par solitario en el nitrógeno se puede compartir con el átomo de boro:
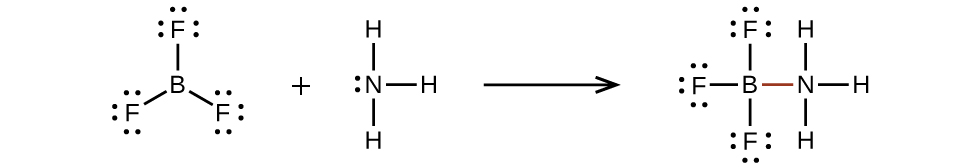
Las moléculas hipervalentes
Los elementos en el segundo período de la tabla periódica (n = 2) pueden alojar solo ocho electrones en sus orbitales de capa de valencia porque tienen solo cuatro orbitales de valencia (uno 2s y tres orbitales 2p). Los elementos en los períodos tercero y superior (n ≥ 3) tienen más de cuatro orbitales de valencia y pueden compartir más de cuatro pares de electrones con otros átomos porque tienen orbitales d vacíos en la misma capa. Las moléculas formadas a partir de estos elementos se llaman a veces moléculas hipervalentes. La tabla \(\PageIndex{5}\) muestra las estructuras de Lewis para dos moléculas hipervalentes, PCl5 y SF6.
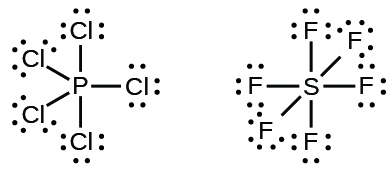
Tabla \(\PageIndex{5}\): En PCl5, el átomo central del fósforo comparte cinco pares de electrones. En SF6, el azufre comparte seis pares de electrones.
En algunas moléculas hipervalentes, como IF5 y XeF4, algunos de los electrones en la capa externa del átomo central son pares solitarios:
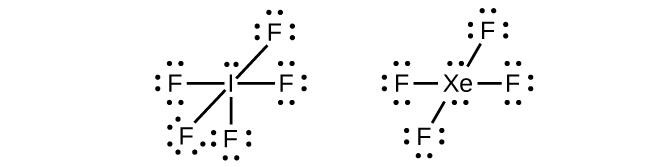
Cuando escribimos las estructuras de Lewis para estas moléculas, encontramos que nos quedan electrones después de llenar las capas de valencia de los átomos externos con ocho electrones. Estos electrones adicionales deben ser asignados al átomo central.
Ejemplo \(\PageIndex{2}\): LAS VIOLACIONES DE LA REGLA OCTETA
El Xenon es un gas noble, pero forma una serie de compuestos estables. Examinamos \(\ce{XeF4}\) anteriormente. ¿Cuáles son las estructuras de Lewis de \(\ce{XeF2}\) y \(\ce{XeF6}\)?
Solución
Podemos dibujar la estructura de Lewis de cualquier molécula covalente siguiendo los seis pasos discutidos anteriormente. En este caso, podemos condensar los últimos pasos, porque no todos se aplican.
Paso 1: Calcule el número de electrones de valencia:
\(\ce{XeF6}\): 8 + (6 × 7) = 50
Paso 2: Dibuje un esqueleto que une los átomos por enlaces simples. El xenón será el átomo central porque el flúor no puede ser un átomo central:
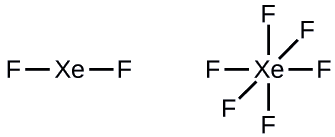
Paso 3: Distribuye los electrones restantes.
XeF2: Colocamos tres pares de electrones solitarios alrededor de cada átomo de F, que representan 12 electrones y le dan a cada átomo de F 8 electrones. Por lo tanto, quedan seis electrones (tres pares solitarios). Estos pares solitarios se deben colocar en el átomo Xe. Esto es aceptable porque los átomos de Xe tienen una capa de valencia vacía de d orbitales y pueden acomodar más de ocho electrones. La estructura de Lewis de XeF2 muestra dos pares de enlaces y tres pares de electrones solitarios alrededor del átomo de Xe:
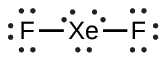
XeF6: Colocamos tres pares de electrones solitarios alrededor de cada átomo F, lo que representa 36 electrones. Quedan dos electrones, y este par solitario se coloca en el átomo Xe:
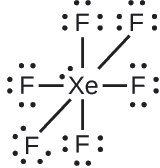
Ejercicio \(\PageIndex{2}\): INTERHALÓGENOS
Los halógenos forman una clase de compuestos llamados los interhalógenos, en los cuales los átomos de halógeno se unen covalentemente entre sí. Escriba las estructuras de Lewis para los interhalógenos. \(\ce{BrCl3}\) and \(\ce{ICl4-}\).
- Respuesta
-
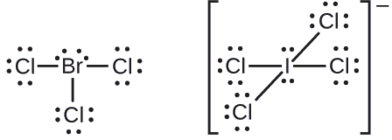
Resumen
Las estructuras electrónicas de valencia se pueden visualizar dibujando símbolos de Lewis (para átomos e iones monoatómicos) y estructuras de Lewis (para moléculas e iones poliatómicos). Se usan pares solitarios, electrones no apareados y enlaces simples, dobles o triples para indicar dónde se encuentran los electrones de valencia alrededor de cada átomo en una estructura de Lewis. La mayoría de las estructuras, especialmente las que contienen elementos de la segunda fila, siguen la regla del octeto, en la que cada átomo (excepto H) está rodeado por ocho electrones. Se producen excepciones a la regla del octeto para moléculas de electrones impares (radicales libres), moléculas deficientes en electrones y moléculas hipervalentes.
Glosario
- doble enlace
- Un enlace covalente en el que dos pares de electrones se comparten entre dos átomos.
- radicales libres
- Moléculas que contienen un número impar de electrones.
- molécula hipervalente
-
Molécula que contiene al menos un elemento del grupo principal que tiene más de ocho electrones en su capa de valencia.
- Estructura de Lewis
- Un diagrama que muestra pares solitarios y pares de electrones de enlace en una molécula o un ion.
- Símbolo de Lewis
- Símbolo para un elemento o ion monoatómico que usa un punto para representar cada electrón de valencia en el elemento o ion.
- único par
- (un par de) electrones de valencia que no se usan para formar un enlace covalente
- Regla del octeto
- Una regla que establece que los átomos del grupo principal formarán estructuras en las que ocho electrones de valencia interactúan con cada núcleo, contando los electrones de enlace como interactuando con ambos átomos conectados por el enlace.
- enlace sencillo
- Un enlace en el que un solo par de electrones se comparte entre dos átomos.
- triple enlace
-
enlace en el que tres pares de electrones se comparten entre dos átomos
Contribuyentes
Paul Flowers (University of North Carolina - Pembroke), Klaus Theopold (University of Delaware) and Richard Langley (Stephen F. Austin State University) with contributing authors. Textbook content produced by OpenStax College is licensed under a Creative Commons Attribution License 4.0 license. Download for free at http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110).
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


