5.4: Soluciones para problemas seleccionados
- Page ID
- 79250
Ejercicio 5.1.1:
Todos estos heteroátomos se encuentran en la esquina superior derecha de la tabla periódica. Todos son bastante electronegativos y todos tienen pares solitarios.
Ejercicio 5.2.2:
- La electronegatividad del heteroátomo unido al grupo carbonilo en un carboxiloide es un factor que le permite salir y formar su propio anión estable.
- Si bien el carbono y el hidrógeno son más electronegativos que muchos de los elementos de la tabla periódica, no son lo suficientemente estables como aniones para formarse fácilmente por sí mismos.
Ejercicio 5.2.3:
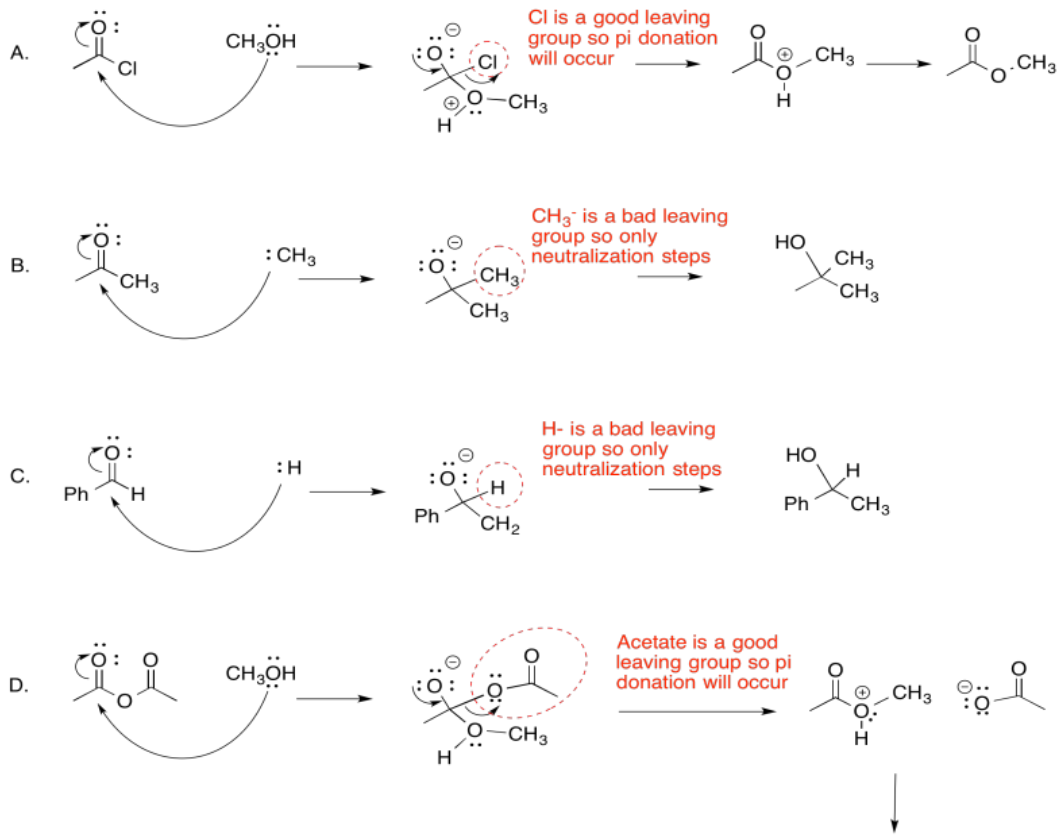
Ejercicio 5.2.4:
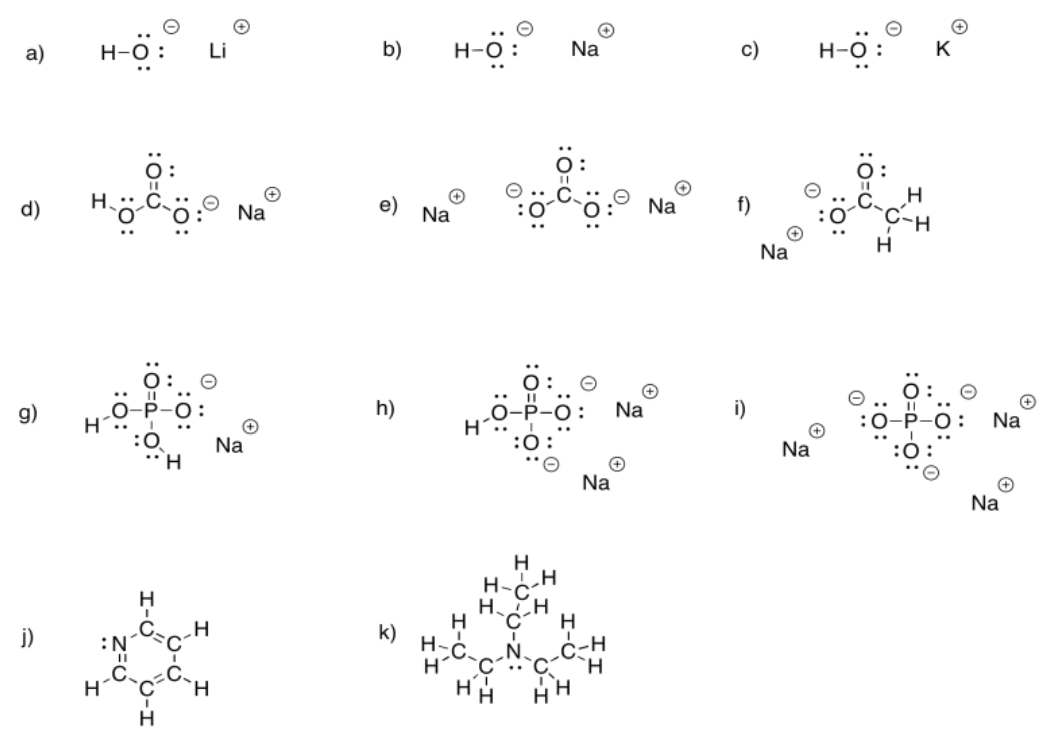
Ejercicio 5.3.1:
Podríamos esperar que los carboxiloides con los elementos más electronegativos unidos al carbonilo sean los más reactivos y menos estables hacia la sustitución (es decir, los carboxiloides con los heteroátomos más electronegativos se sustituirían más fácilmente).
En ese caso, predeciríamos que los carboxiloides con el sustituyente más electronegativo (oxígeno) serían los más reactivos. Hay una serie de tipos diferentes y vamos a pensar en cómo se relacionan entre sí en breve.
Después de los derivados del oxígeno predeciríamos ya sea los derivados del nitrógeno o el cloruro, dependiendo de qué escala de electronegatividad pasemos a usar (recuerde, la electronegatividad no es una propiedad experimentalmente pura, sino el resultado de un cálculo que se puede realizar de diferentes maneras). El derivado de azufre sería menos reactivo.
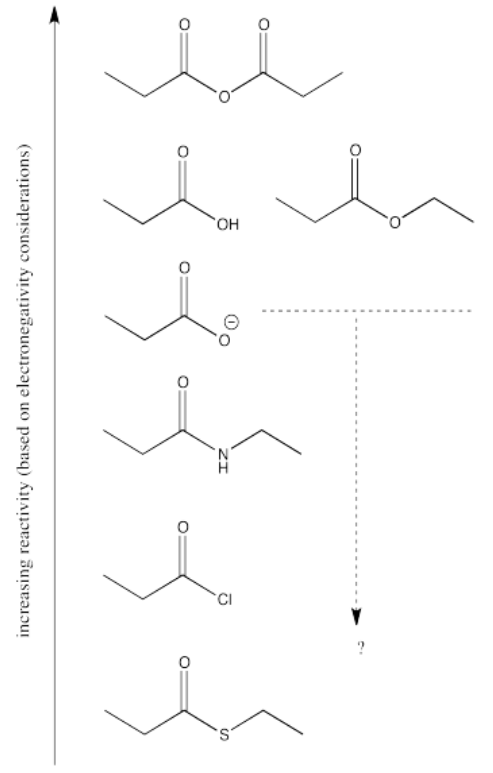
Todavía hay varios derivados de oxígeno diferentes para comparar: ácidos carboxílicos (OH), carboxilatos (O-), ésteres (OR, en los que R es una cadena alquílica o carbonada) y anhídrido de ácido (OC=O). El más fácil de diferenciar es el carboxilato, debido a su carga negativa. Debe ser menos atractivo para un nucleófilo que los otros derivados del oxígeno, porque ofrecería más repulsión a un par solitario entrante.
Sin embargo, realmente no podemos predecir si sería menos reactivo que los análogos de nitrógeno, cloro o azufre, porque ¿quién sabe si la carga o la naturaleza del átomo importan más?
A medida que sucede, el cargo probablemente importe más. Aprendemos que simplemente mirando la tendencia experimental y viendo que el carboxilato es el menos reactivo de todos los carboxiloides.
Volviendo a los otros tres derivados de oxígeno, sería difícil diferenciar entre el efecto de un átomo de hidrógeno remoto versus una cadena alquílica en el éster frente al ácido carboxílico, por lo que diremos que esos dos son aproximadamente los mismos. Por otro lado, el grupo carbonilo adicional aceptor de electrones en el anhídrido de ácido probablemente tenga un efecto profundo, por lo que esperaríamos que ese compuesto atraiga más fuertemente a los nucleófilos.
Por supuesto, la serie que hemos producido anteriormente no es la “respuesta correcta”. No coincide con la serie experimentalmente observada de reactividades carboxiloides. Sin embargo, es muy útil en términos de construir una comprensión de los carboxiloides. Nos dice que la electronegatividad puede jugar un papel aquí, pero que no puede ser el único factor.
Algún otro factor es poner fuera de orden algunos de los derivados. En particular, el cloruro de ácido (C=OCl) y el tioéster (C=OSR) no encajan.
Ejercicio 5.3.2:
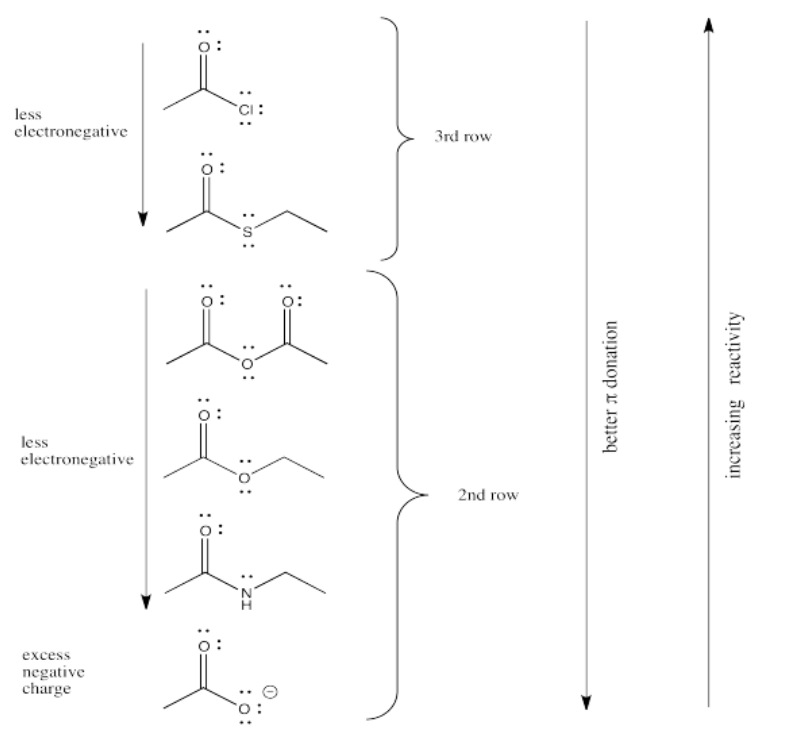
La electronegatividad es un factor abvious que podría influir en la capacidad de un átomo para donar π, pero acabamos de ver ese factor en la sección anterior, así que veamos otra propiedad atómica en su lugar. Por supuesto, diferentes átomos tienen diferentes tamaños. En particular, si observamos los átomos involucrados en los sustituyentes carboxiloides, podemos dividirlos en átomos de segunda fila y átomos de tercera fila.
De hecho, está bien documentado que el grado de superposición entre dos orbitales influye en qué tan bien se unen entre sí. Dado que el carbono está en la segunda fila, tiene aproximadamente el mismo tamaño que, y se superpone bastante bien con, otros átomos de la segunda fila. Los átomos de la tercera fila son un poco demasiado grandes, por otro lado.
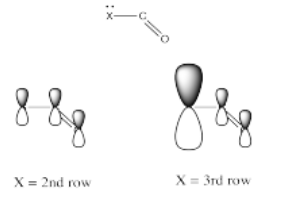
Ese factor rompe los carboxiloides en dos grupos diferentes. Suponiendo que la donación de π-es un factor importante, el azufre y el cloro pueden colocarse por encima de los demás en temas de reactividad. No pueden donar tan bien como la lata de oxígeno o nitrógeno.
A partir de ahí, las diferencias entre los átomos de una misma fila pueden resolverse en función de las diferencias de electronegatividad.
Ejercicio 5.3.3:
Los enlaces amida se encuentran entre los carboxiloides más estables posibles. Esa estabilidad los hace adecuados para formar estructuras útiles que no se descompondrán fácilmente. Recuerde, cualquier cambio que ocurra en la materia ocurre a través de reacciones químicas, incluyendo la formación y descomposición de biomateriales. El cierre de una posible reacción química significa que un material será más duradero.
Ejercicio 5.3.4:

Ejercicio 5.3.5:
Una posibilidad es la presencia de un sustituyente electronegativo adicional. En el cloruro de oxalil, la presencia de un carbonilo adicional junto al grupo cloruro de ácido electrófilo haría que cada carbonilo fuera aún más electrófilo. En el cloruro de tionilo, la presencia de dos cloros, en lugar de solo uno, podría hacer que este compuesto sea mucho menos estable y más electrófilo.
Ejercicio 5.4.1:
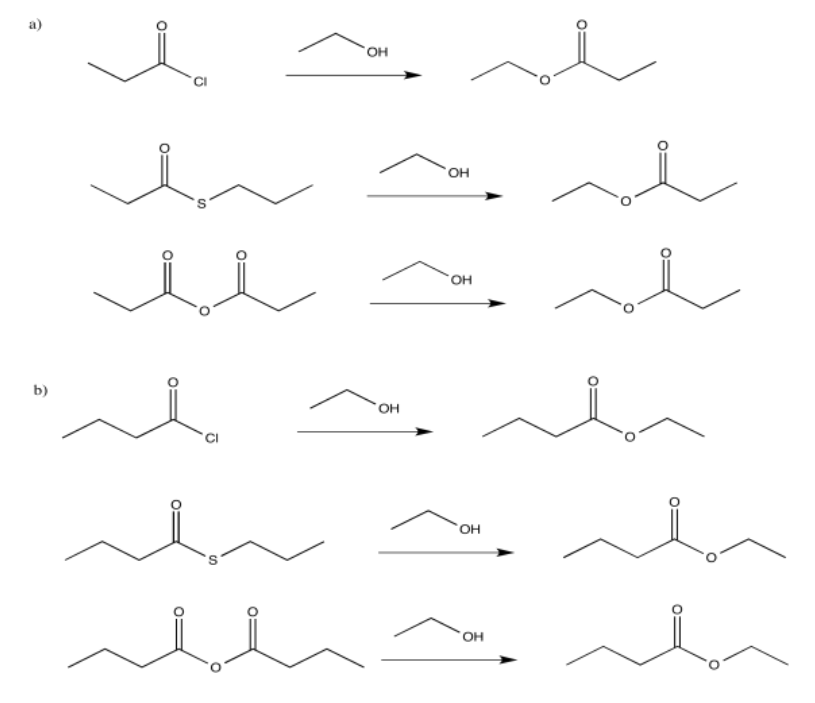
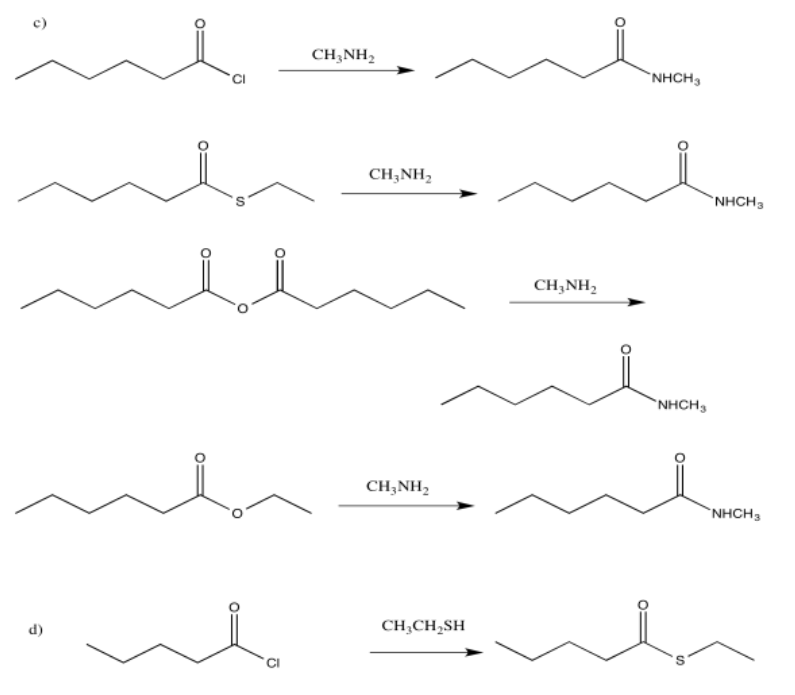
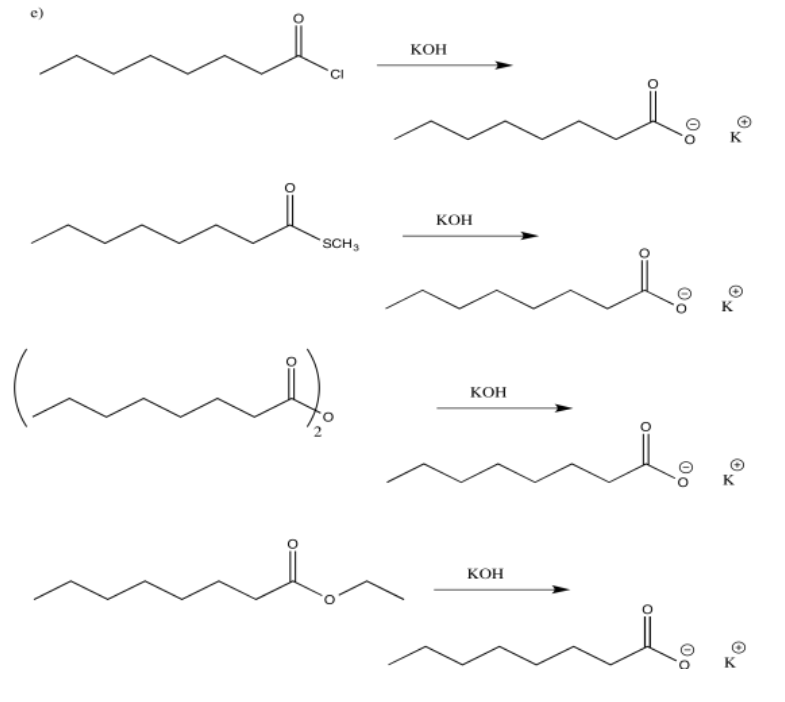
Ejercicio 5.4.2:
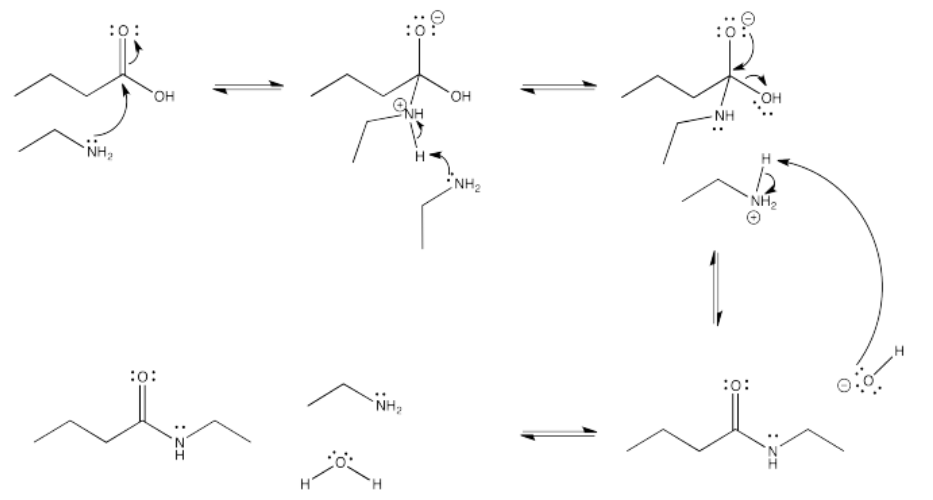
Ejercicio 5.4.3:
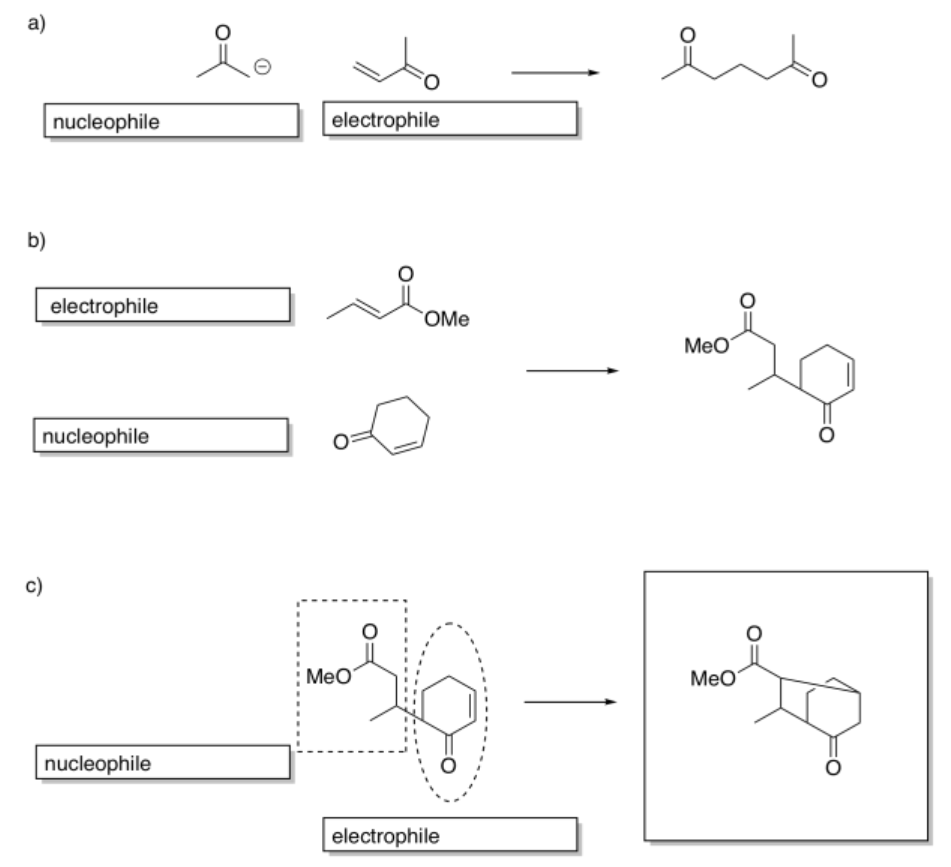
a)
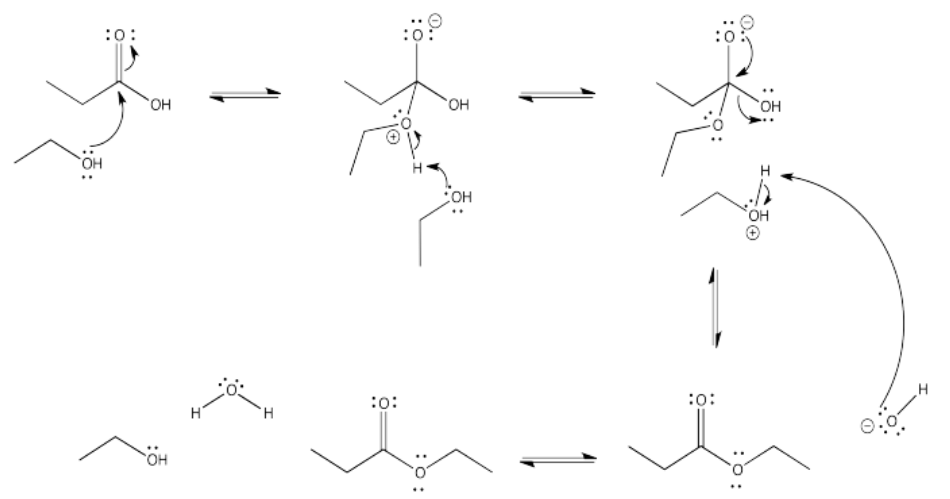
b)
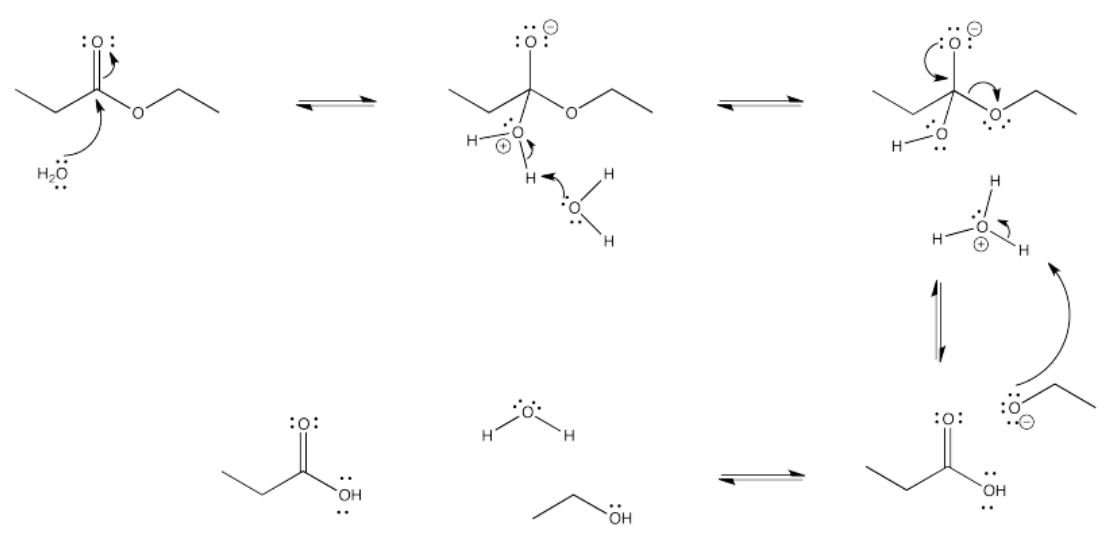
Ejercicio 5.4.4
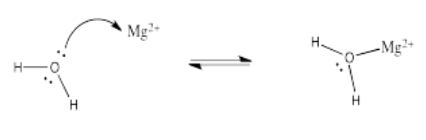
Ejercicio 5.4.5:

Ejercicio 5.4.6:
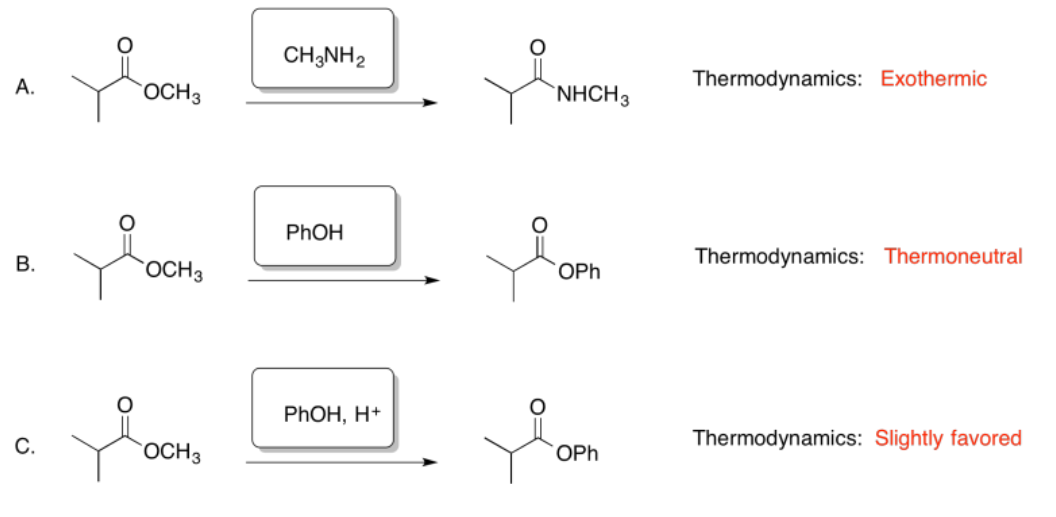
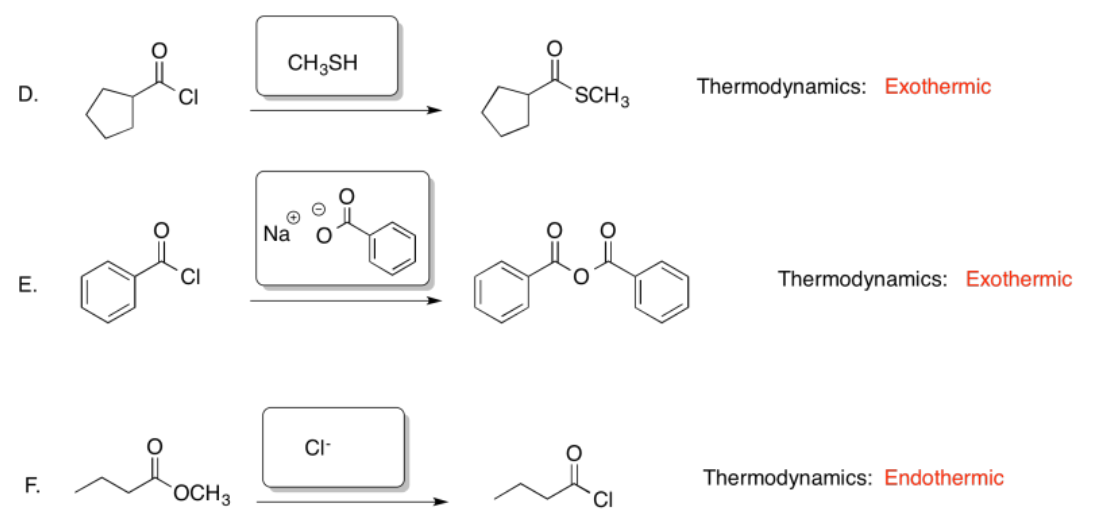
Ejercicio 5.4.7:
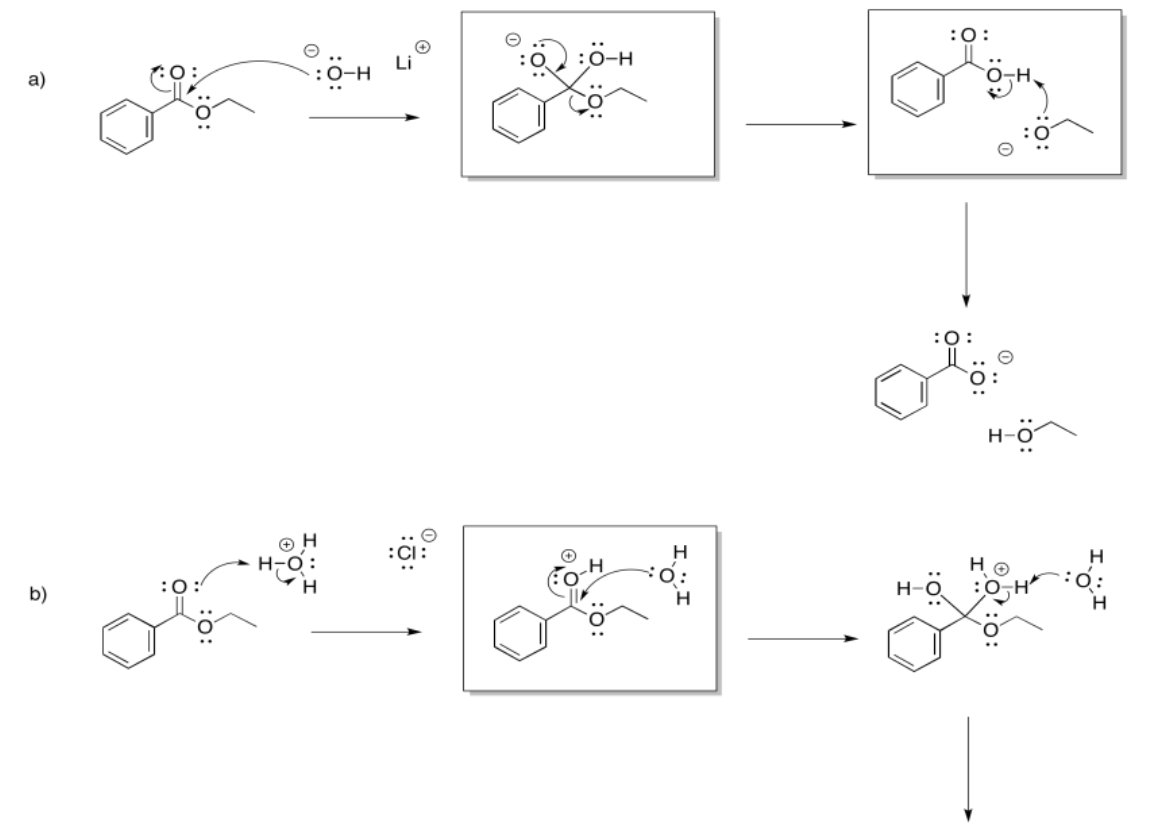
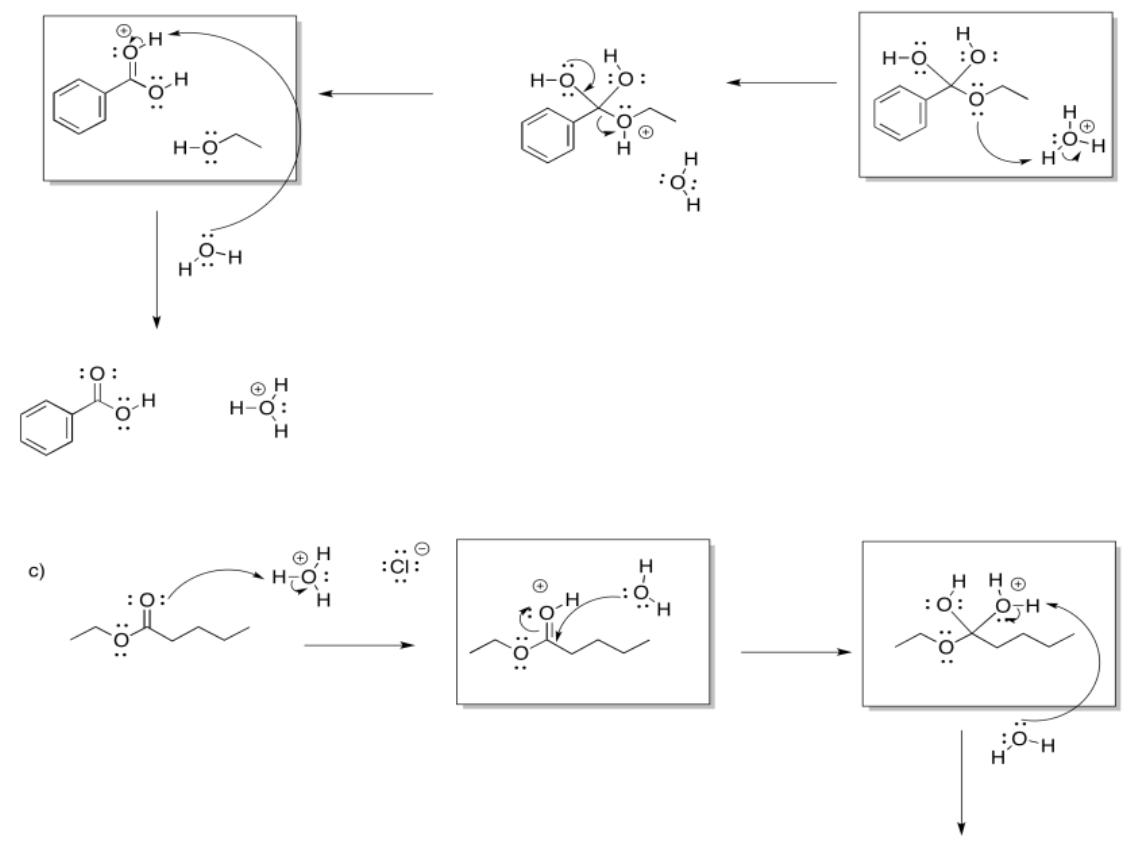
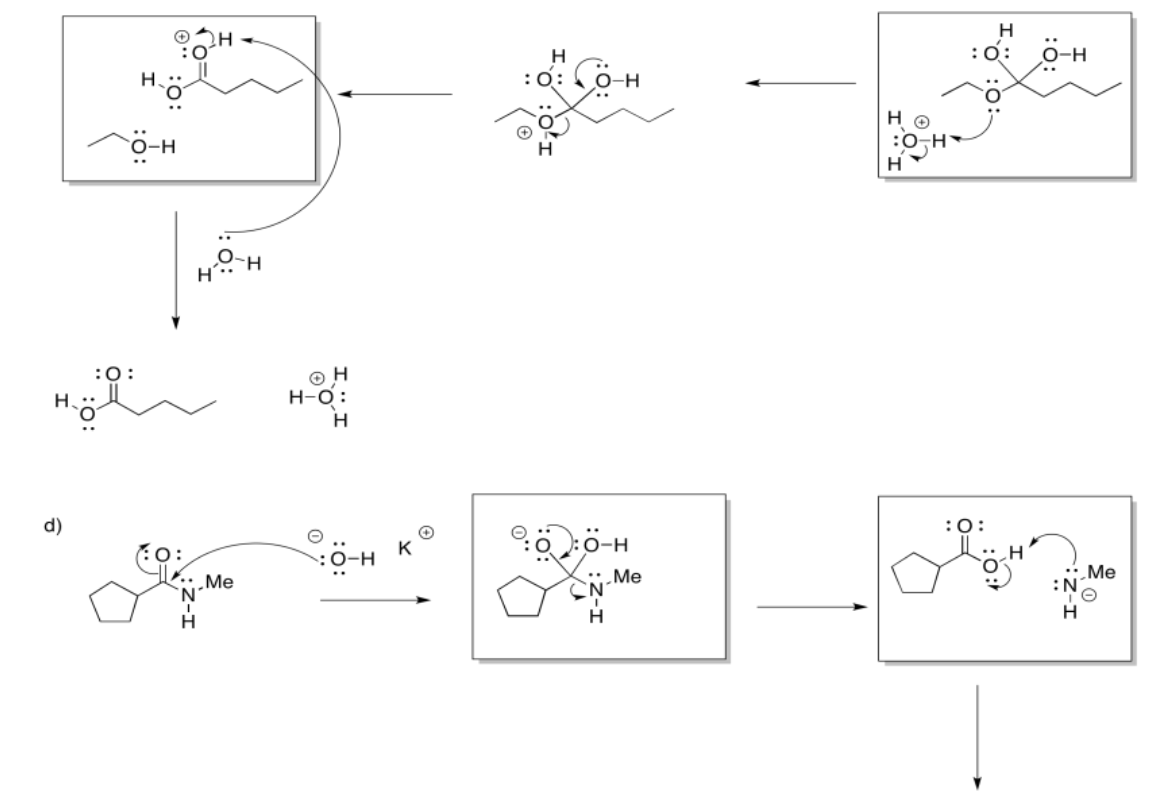
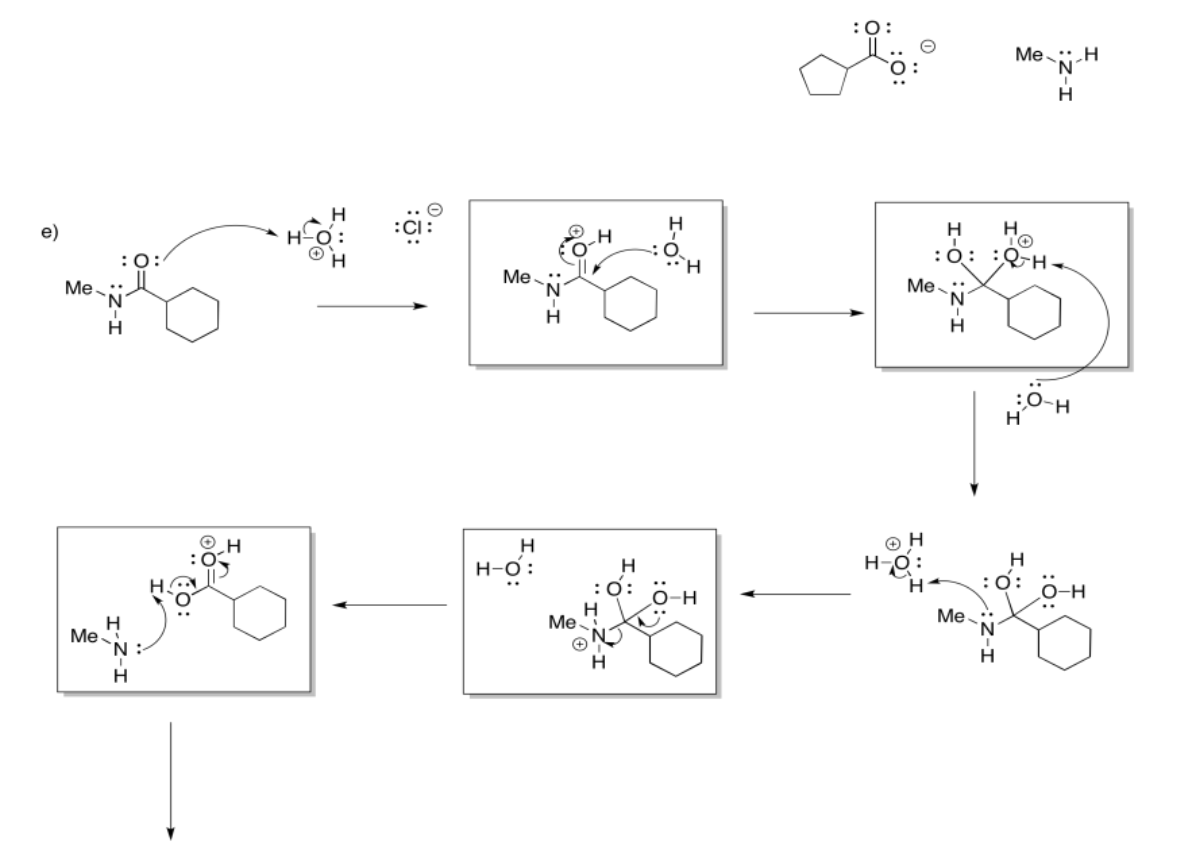
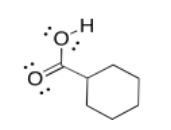
Ejercicio 5.5.4:

Ejercicio 5.5.8:
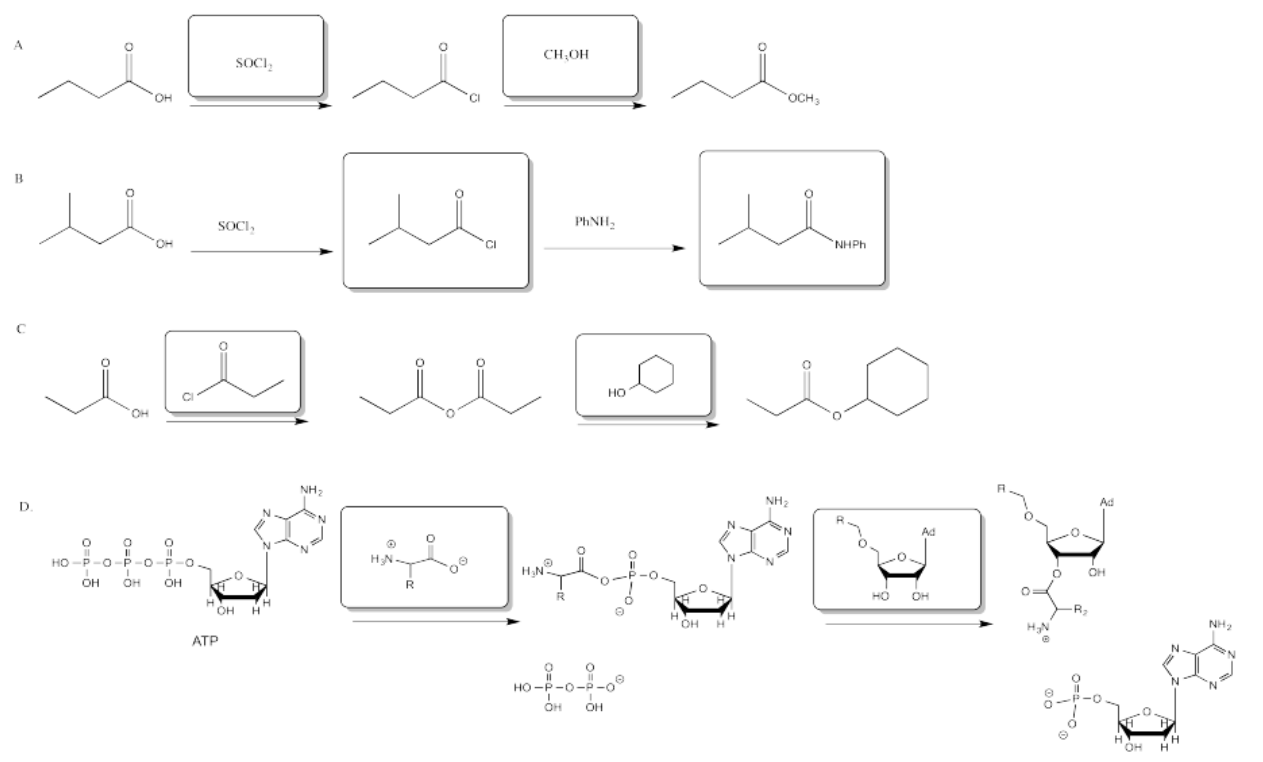
Ejercicio 5.6.1:
Debido a que los cloruros de ácido están en la parte superior del diagrama de reactividad de carboxiloides (la colina de esquí), y es probable que otros haluros sean similares en reactividad al cloruro, esta reacción sería cuesta arriba de los otros carboxiloides.
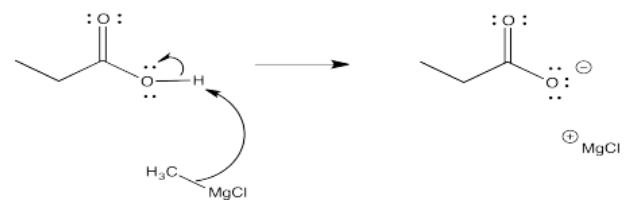
Ejercicio 5.6.4:
Ejercicio 5.6.5:
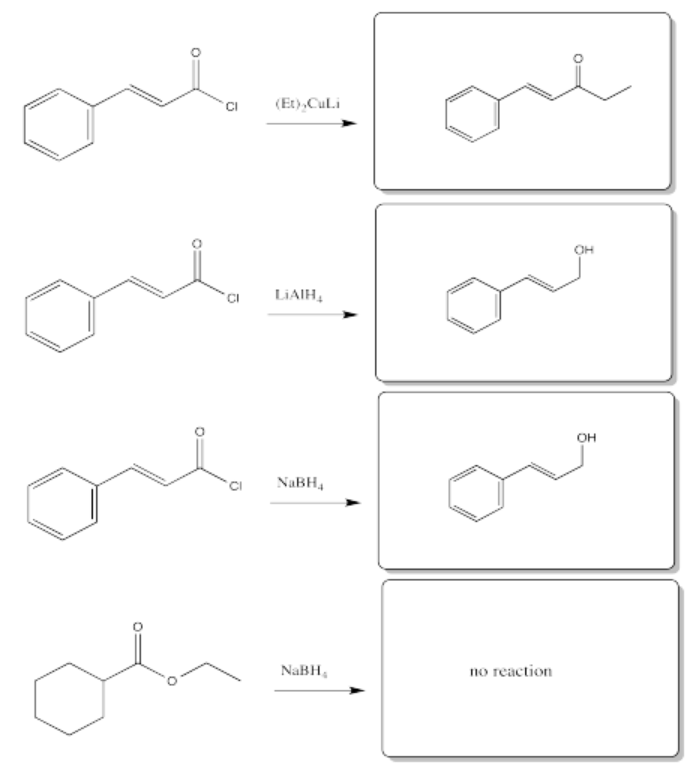
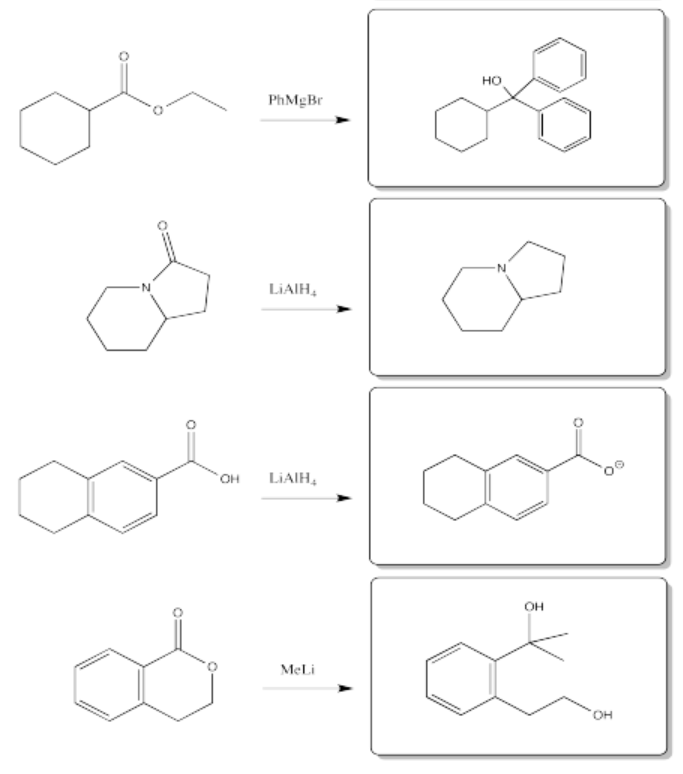
Las amidas y carboxilatos son los carboxilatos menos reactivos, por lo que podría no ser demasiado sorprendente que no reaccionen con estos nucleófilos.
Ejercicio 5.6.6:
Los cloruros de ácido reaccionan típicamente con estos reactivos de cuprato.
Ejercicio 5.6.7:
Los borohidruros podrían reaccionar presumiblemente con cloruros de ácido, anhidridos y tioésteres, que son los carboxiloides más reactivos. Probablemente no puedan reaccionar con amids o iones carboxilato, que están aún más abajo que los ésteres.
Ejercicio 5.6.11:
Ejercicio 5.7.1:
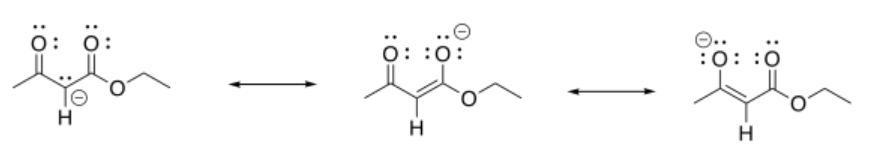
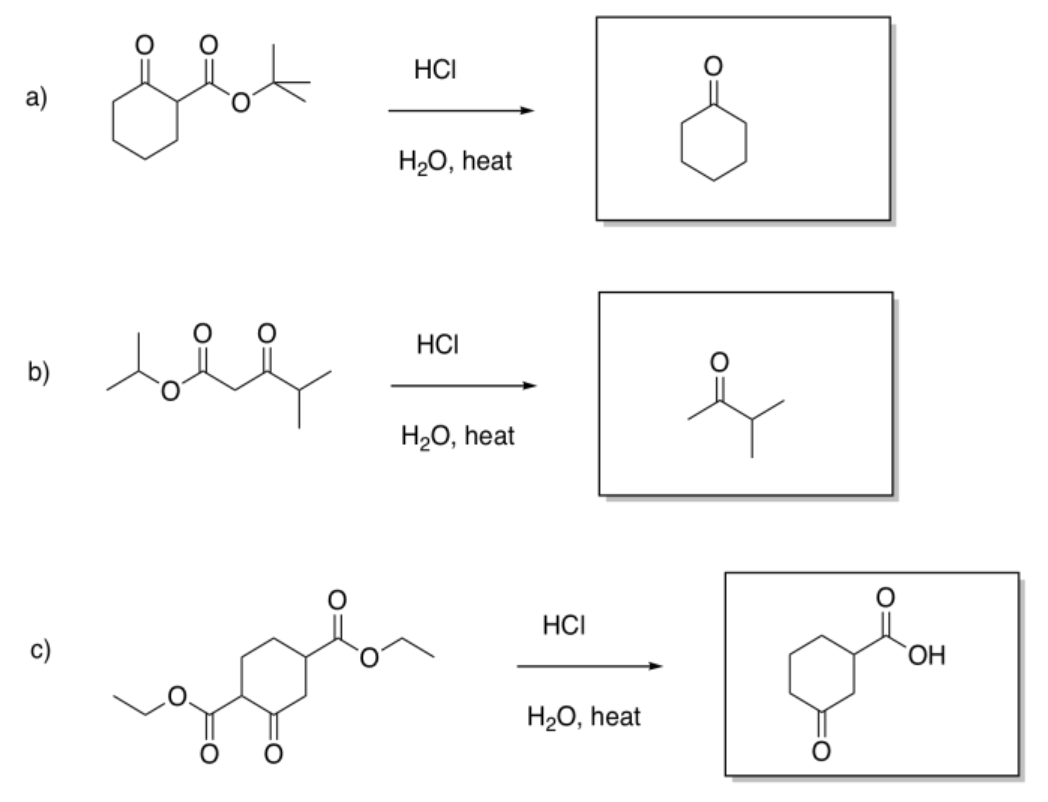
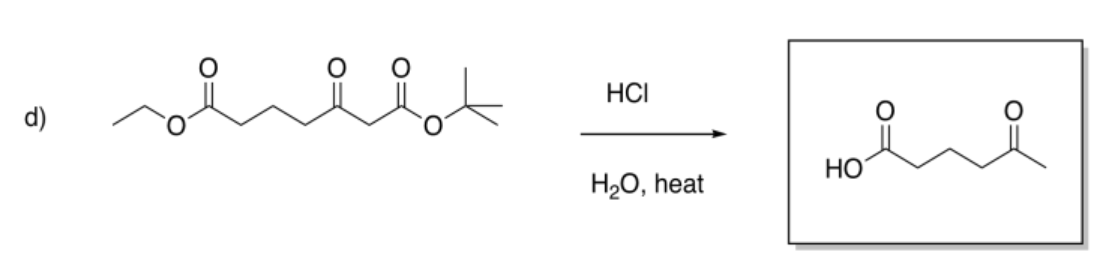
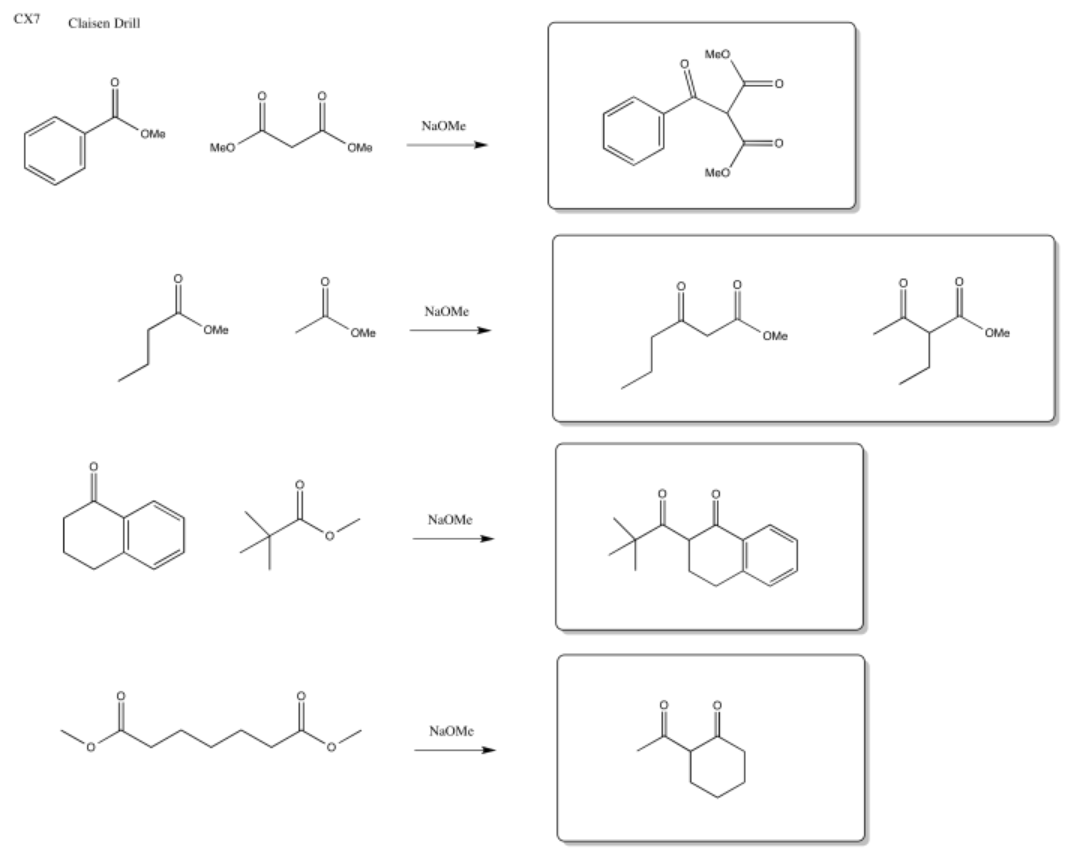
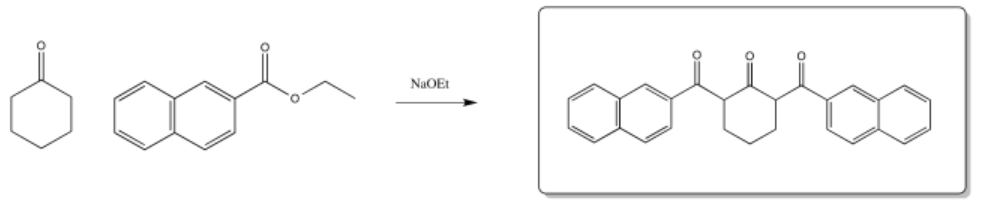
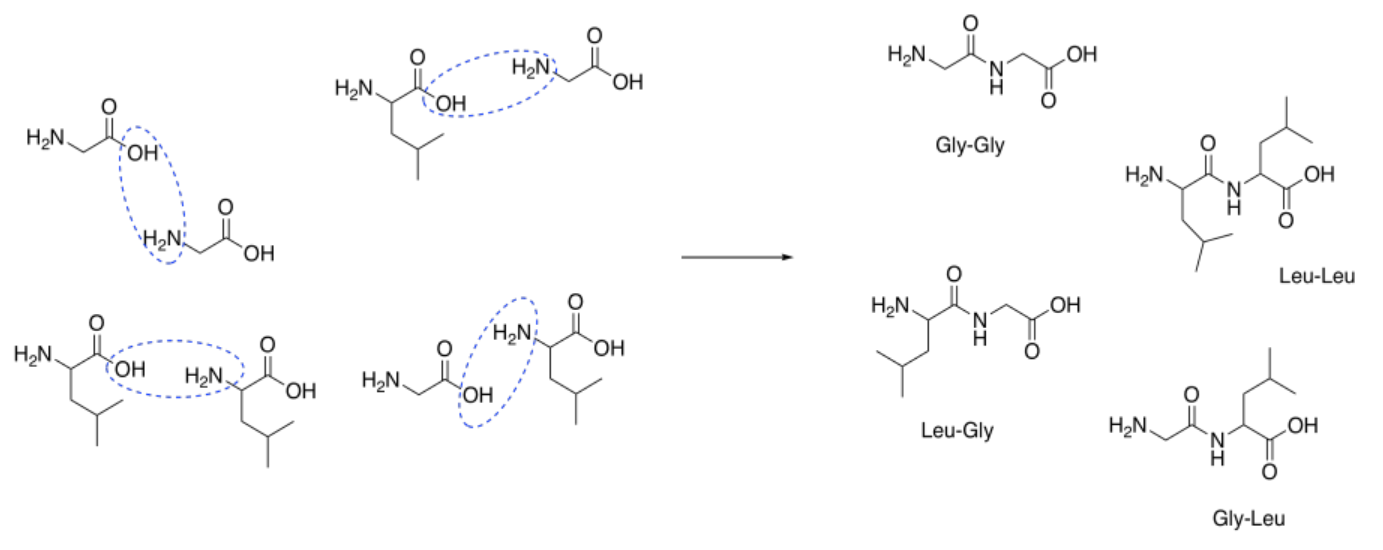
Esa combinación daría los siguientes dipéptidos:
ala-ala ala-gly ala-val
gly-gly gly-ala gly-val
val-val val-ala val-gly
Por supuesto, también podríamos obtener tripéptidos, como ala-ala-gly-val, y así sucesivamente.
Los ácidos carboxílicos suelen requerir activación antes de que puedan actuar como nucleófilos. Ese problema es realmente complicado aquí porque el ácido carboxílico está en equilibrio con una sal carboxilato (leer más en la página).
La reactividad relativa de los carboxiloides es el resultado de un equilibrio entre los efectos de extracción de electrones sigma y la donación de pi. Un átomo electronegativo unido a un carbonilo tiende a retirar la densidad electrónica, lo que hace que el carbonilo sea aún más positivo y electrófilo. Por otro lado, la pi-donación de un átomo vecino con un par solitario en realidad disminuye la electrofilicidad al formar un sistema estable y conjugado.
En un carbamato, se agrega un átomo electronegativo adicional al carbonilo: tiene un oxígeno así como un nitrógeno adyacente al grupo C=O. Ese átomo aleja la densidad electrónica del carbonilo, haciéndolo más electrófilo. Sin embargo, la pi-donación a partir del oxígeno adicional no resulta en un sistema conjugado más estable. El sistema pi máximo tiene todavía solo tres átomos de largo; o bien implica la conjugación de la unidad O-C=O o la unidad N-C=O. No conduce, por ejemplo, a un sistema conjugado aún más estable de cuatro átomos de longitud.
Como resultado, el oxígeno agregado probablemente contribuye más al efecto de extracción de electrones que a la estabilización del sistema pi.
A menudo se usa la sal hidrocloruro más polar de EDCI, como se muestra en la imagen. Este compuesto más polar se disuelve bien en disolventes polares, como el agua, que también disuelven los aminoácidos.
También se puede imaginar el grupo amino en EDCI actuando como un sitio para la catálisis, transportando protones de un lugar a otro.
Problema CX10.1.
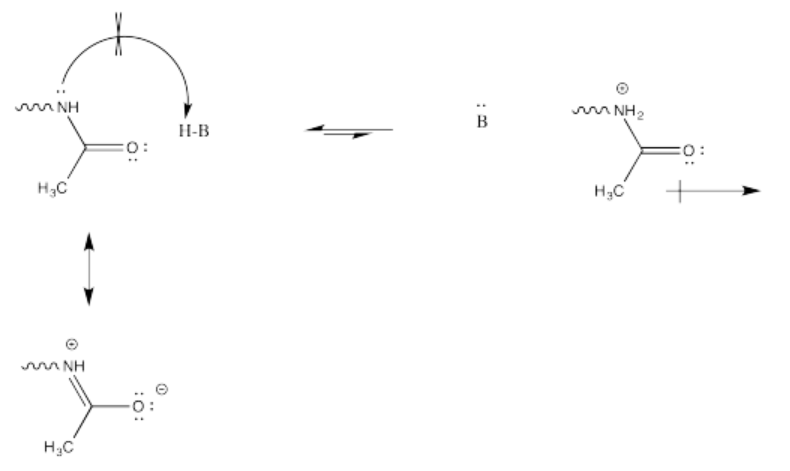
Este cambio en la carga resulta porque, aunque las aminas se protonan fácilmente, las amidas no lo son. La protonación de una amida resultaría en un catión adyacente al carbono carbonílico muy positivo, conduciendo a una acumulación de carga positiva localizada. Eso no sería fácil. Además, no es muy probable que el nitrógeno de la amida done sus electrones a un protón en primer lugar. Sus protones están demasiado ocupados. Están atados en conjugación con el carbonilo, por lo que realmente no están disponibles para actuar como el par solitario de una base.