16.4: Tasas de Procesos Espontáneos
- Page ID
- 74975
La frase lo más rápido posible señala una gran dificultad para lidiar con procesos espontáneos. Algunos de ellos ocurren con bastante rapidez, pero otros son tan lentos como para ser imperceptibles. Un proceso espontáneo rápido ocurre cuando se mezclan 2 mol H 2 O con 2 mol de “agua pesada”, D 2 O, hecha del isótopo deuterio\({}_{\text{1}}^{\text{2}}\text{H}\), o D. Las dos especies comienzan a transferir protones y deuterones (iones D +) tan pronto como se agitan juntos, y rápidamente obtenemos una mezcla que consiste en 2 mol H—O—D y 1 mol cada uno de H—O—H y D—O—D. Suponiendo que los átomos de deuterio se comportan químicamente de la misma manera que los átomos de hidrógeno ordinarios, esto es lo que significa leyes de probabilidad predecirían. Hay cuatro posibilidades igualmente probables para una molécula de agua seleccionada al azar:
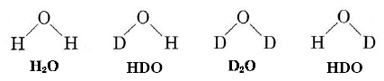 Dos de las cuatro posibilidades tienen la fórmula molecular HDO, por lo que la probabilidad de encontrar una molécula de HDO en nuestra mezcla es 1/2. La mitad de las moléculas (2 mol) serán HDO. De igual manera 1/4 de los 4 mol de agua será H 2 O y 1/4 será D 2 O.
Dos de las cuatro posibilidades tienen la fórmula molecular HDO, por lo que la probabilidad de encontrar una molécula de HDO en nuestra mezcla es 1/2. La mitad de las moléculas (2 mol) serán HDO. De igual manera 1/4 de los 4 mol de agua será H 2 O y 1/4 será D 2 O.
El cambio de la situación improbable de 2 mol H 2 O + 2 mol D 2 O a los más probables 2 mol HDO + 1 mol H 2 O + 1 mol D 2 O ocurre rápidamente debido a la facilidad con que los protones y deuterones pueden transferirse de una molécula de agua a otra. Sin embargo, cuando tal proceso de barajado es lento, la situación es bastante diferente. Por ejemplo, esperaríamos que mezclar 2 mol H 2 con 2 mol D 2 produciría 2 mol HD y un mol cada uno de H 2 y D 2. A temperatura ambiente, sin embargo, no pasa nada, incluso en un periodo de días, porque no hay una manera fácil de que los átomos de H o D intercambien parejas. La reorganización requiere romper un enlace H—H o D-D, y esto toma alrededor de 400 kJ mol —1. Las moléculas están atrapadas en una situación de baja probabilidad porque no hay vía por la que puedan alcanzar una mayor probabilidad. Si se proporciona tal vía, elevando la temperatura o añadiendo un catalizador, las moléculas comienzan a intercambiar H y D y se mueven hacia la situación más probable.
La moraleja de esta historia es que decir que una reacción es espontánea no es lo mismo que decir que ocurrirá si se mezclan los reactivos. Más bien, significa que la reacción puede ocurrir pero puede ser tan lenta que no parece pasar nada. En el caso de una reacción espontánea lenta vale la pena buscar un catalizador, pero si sabemos que la reacción es no espontánea, no tiene sentido ni siquiera mezclar los reactivos, y mucho menos buscar un catalizador. Una reacción no espontánea no puede ocurrir por sí misma sin intervención externa.


