9.6: Comportamiento de gas no ideal
- Page ID
- 75814
- Describir los factores físicos que conducen a desviaciones del comportamiento ideal del gas
- Explicar cómo se representan estos factores en la ecuación de van der Waals
- Definir la compresibilidad (Z) y describir cómo su variación con la presión refleja un comportamiento no ideal
- Cuantificar el comportamiento no ideal comparando cálculos de las propiedades del gas usando la ley de gas ideal y la ecuación de van der Waals
Hasta el momento, la ley de gas ideal, PV = nRT, se ha aplicado a una variedad de diferentes tipos de problemas, que van desde la estequiometría de reacción y problemas empíricos y de fórmulas moleculares hasta la determinación de la densidad y masa molar de un gas. Sin embargo, como se mencionó en los módulos anteriores de este capítulo, el comportamiento de un gas a menudo no es ideal, lo que significa que las relaciones observadas entre su presión, volumen y temperatura no son descritas con precisión por las leyes de gas. En esta sección se consideran las razones de estas desviaciones del comportamiento ideal del gas.
Una forma en la que se puede juzgar la precisión de PV = nRT es comparando el volumen real de 1 mol de gas (su volumen molar, Vm) con el volumen molar de un gas ideal a la misma temperatura y presión. Esta relación se denomina factor de compresibilidad (Z) con:
\[\mathrm{Z=\dfrac{molar\: volume\: of\: gas\: at\: same\:\mathit{T}\:and\:\mathit{P}}{molar\: volume\: of\: ideal\: gas\: at\: same\:\mathit{T}\:and\:\mathit{P}}}=\left(\dfrac{PV_m}{RT}\right)_\ce{measured} \nonumber \]
Por lo tanto, el comportamiento ideal del gas se indica cuando esta relación es igual a 1, y cualquier desviación de 1 es una indicación de comportamiento no ideal. La figura\(\PageIndex{1}\) muestra gráficas de Z en un amplio rango de presión para varios gases comunes.
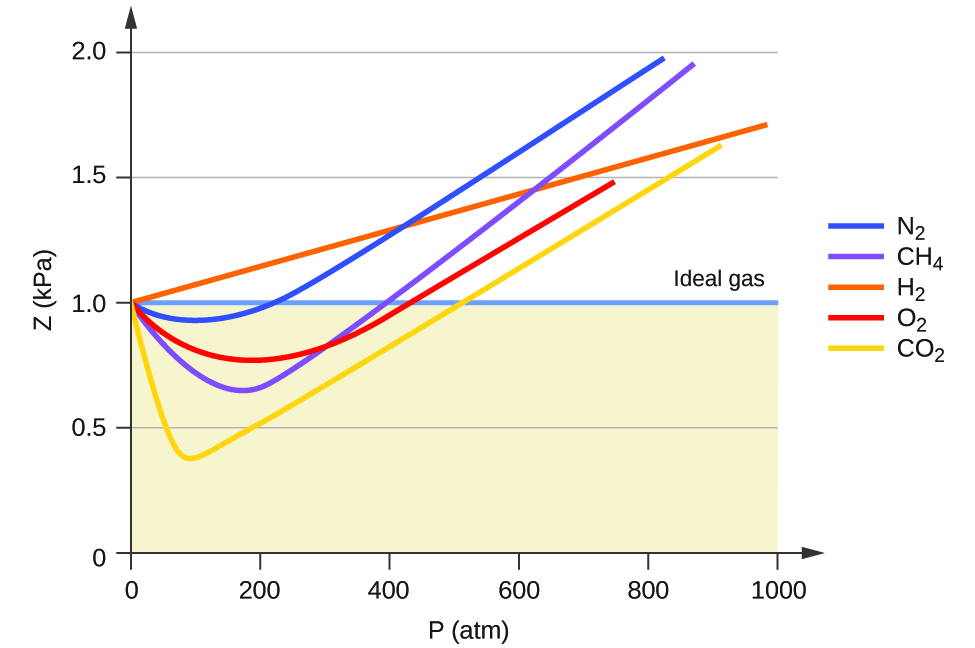
Como es evidente a partir de la Figura\(\PageIndex{1}\), la ley de gas ideal no describe bien el comportamiento del gas a presiones relativamente altas. Para determinar por qué esto es, considere las diferencias entre las propiedades reales del gas y lo que se espera de un hipotético gas ideal.
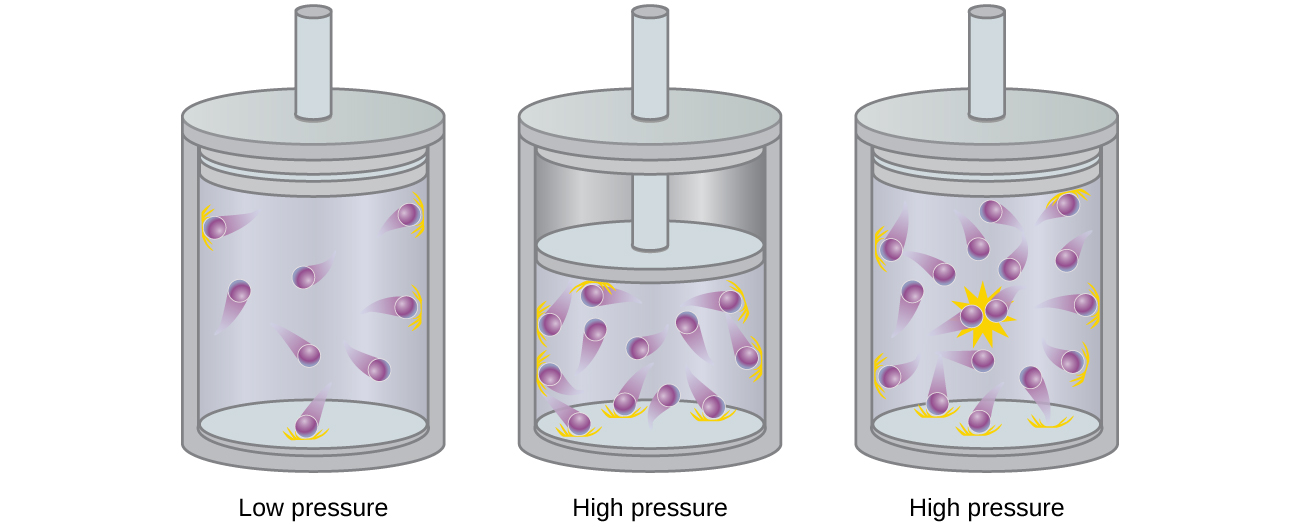
Las partículas de un hipotético gas ideal no tienen volumen significativo y no se atraen ni repelen entre sí. En general, los gases reales se aproximan a este comportamiento a presiones relativamente bajas y altas temperaturas. Sin embargo, a altas presiones, las moléculas de un gas se apiñan más juntas, y se reduce la cantidad de espacio vacío entre las moléculas. A estas presiones más altas, el volumen de las propias moléculas de gas se vuelve apreciable en relación con el volumen total ocupado por el gas (Figura\(\PageIndex{2}\)). Por lo tanto, el gas se vuelve menos compresible a estas altas presiones, y aunque su volumen sigue disminuyendo con el aumento de la presión, esta disminución no es proporcional como lo predice la ley de Boyle.
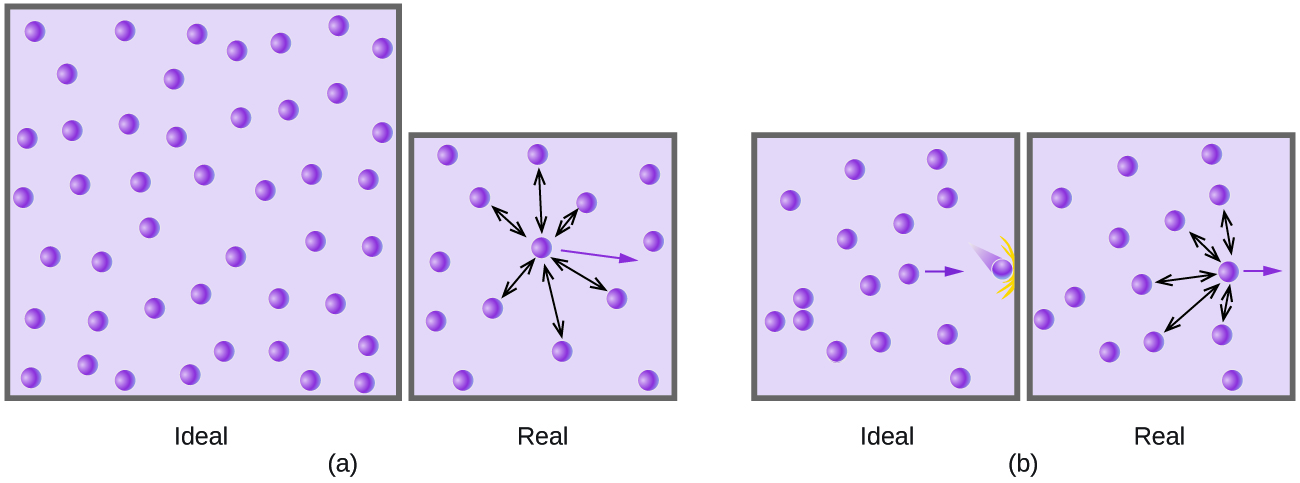
A presiones relativamente bajas, las moléculas de gas prácticamente no tienen atracción entre sí porque están (en promedio) tan separadas, y se comportan casi como partículas de un gas ideal. A presiones más altas, sin embargo, la fuerza de atracción tampoco es insignificante. Esta fuerza acerca un poco más las moléculas, disminuyendo ligeramente la presión (si el volumen es constante) o disminuyendo el volumen (a presión constante) (Figura\(\PageIndex{3}\)). Este cambio es más pronunciado a bajas temperaturas debido a que las moléculas tienen menor KE en relación con las fuerzas de atracción, por lo que son menos efectivas para superar estas atracciones después de chocar entre sí.
Hay varias ecuaciones diferentes que aproximan mejor el comportamiento del gas que la ley de gas ideal. El primero, y más simple, de estos fue desarrollado por el científico holandés Johannes van der Waals en 1879. La ecuación de van der Waals mejora la ley de gas ideal al agregar dos términos: uno para dar cuenta del volumen de las moléculas de gas y otro para las fuerzas atractivas entre ellas.
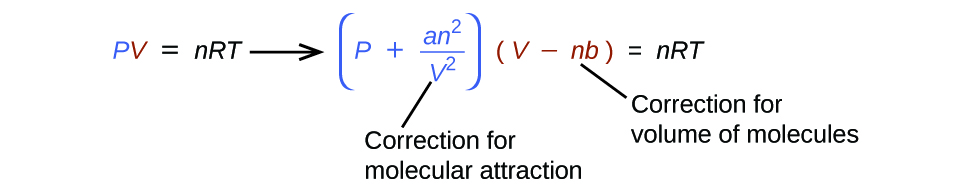
La constante a corresponde a la fuerza de atracción entre moléculas de un gas en particular, y la constante b corresponde al tamaño de las moléculas de un gas particular. La “corrección” al término de presión en la ley de gas ideal es\(\dfrac{n^2a}{V^2}\), y la “corrección” al volumen es nb. Tenga en cuenta que cuando V es relativamente grande y n es relativamente pequeño, ambos términos de corrección se vuelven despreciables, y la ecuación de van der Waals se reduce a la ley de gas ideal, PV = nRT. Tal condición corresponde a un gas en el que un número relativamente bajo de moléculas está ocupando un volumen relativamente grande, es decir, un gas a una presión relativamente baja. Los valores experimentales para las constantes de van der Waals de algunos gases comunes se dan en la Tabla\(\PageIndex{1}\).
| Gas | a (L 2 atm/mol 2) | b (L/mol) |
|---|---|---|
| N 2 | 1.39 | 0.0391 |
| O 2 | 1.36 | 0.0318 |
| CO 2 | 3.59 | 0.0427 |
| H 2 O | 5.46 | 0.0305 |
| Él | 0.0342 | 0.0237 |
| CCl 4 | 20.4 | 0.1383 |
A bajas presiones, la corrección para atracción intermolecular, a, es más importante que la de volumen molecular, b. A altas presiones y pequeños volúmenes, la corrección para el volumen de las moléculas adquiere importancia porque las moléculas mismas son incompresibles y constituyen una fracción apreciable del volumen total. A cierta presión intermedia, las dos correcciones tienen influencias opuestas y el gas parece seguir la relación dada por PV = nRT en un pequeño rango de presiones. Este comportamiento se refleja en las “inmersiones” en varias de las curvas de compresibilidad mostradas en la Figura\(\PageIndex{1}\). La fuerza de atracción entre las moléculas inicialmente hace que el gas sea más compresible que un gas ideal, ya que aumenta la presión (Z disminuye con el aumento de P). A presiones muy altas, el gas se vuelve menos compresible (Z aumenta con P), ya que las moléculas de gas comienzan a ocupar una fracción cada vez más significativa del volumen total de gas.
Estrictamente hablando, la ecuación de gas ideal funciona bien cuando las atracciones intermoleculares entre las moléculas de gas son insignificantes y las moléculas de gas en sí mismas no ocupan una parte apreciable de todo el volumen. Estos criterios se cumplen en condiciones de baja presión y alta temperatura. En tales condiciones, se dice que el gas se comporta de manera ideal, y las desviaciones de las leyes de gas son lo suficientemente pequeñas como para que puedan ser ignoradas; sin embargo, este no es el caso muy a menudo.
Un matraz de 4.25 l contiene 3.46 mol de CO 2 a 229 °C. Calcular la presión de esta muestra de CO 2:
- de la ley de gas ideal
- de la ecuación de van der Waals
- Explique las razones de la diferencia.
Solución
a) De la ley de gas ideal:
b) De la ecuación de van der Waals:
\(\left(P+\dfrac{n^2a}{V^2}\right)×(V−nb)=nRT⟶P=\dfrac{nRT}{(V−nb)}−\dfrac{n^2a}{V^2}\)
\(P=\mathrm{\dfrac{3.46\:mol×0.08206\:L\:atm\:mol^{−1}\:K^{−1}×502\: K}{(4.25\:L−3.46\:mol×0.0427\:L\:mol^{−1})}−\dfrac{(3.46\:mol)^2×3.59\:L^2\:atm\:mol^2}{(4.25\:L)^2}}\)
Esto finalmente produce P = 32.4 atm.
(c) Esto no es muy diferente del valor de la ley de gas ideal porque la presión no es muy alta y la temperatura no es muy baja. El valor es algo diferente porque las moléculas de CO 2 sí tienen cierto volumen y atracciones entre las moléculas, y la ley de gas ideal asume que no tienen volumen ni atracciones.
Un matraz de 560-mL contiene 21.3 g de N 2 a 145 °C. Calcular la presión de N 2:
- de la ley de gas ideal
- de la ecuación de van der Waals
- Explique las razones de la diferencia.
- Contestar a
-
46.562 atm
- Respuesta b
-
46.594 atm
- Respuesta c
-
La ecuación de van der Waals toma en cuenta el volumen de las propias moléculas de gas así como las atracciones intermoleculares.
Resumen
Las moléculas de gas poseen un volumen finito y experimentan fuerzas de atracción mutua. En consecuencia, el comportamiento del gas no es necesariamente descrito bien por la ley de gas ideal. En condiciones de baja presión y alta temperatura, estos factores son insignificantes, la ecuación ideal del gas es una descripción precisa del comportamiento del gas y se dice que el gas exhibe un comportamiento ideal. Sin embargo, a temperaturas más bajas y presiones más altas, se requieren correcciones para el volumen molecular y las atracciones moleculares para explicar el tamaño molecular finito y las fuerzas de atracción. La ecuación de van der Waals es una versión modificada de la ley de gas ideal que puede utilizarse para dar cuenta del comportamiento no ideal de los gases bajo estas condiciones.
Ecuaciones Clave
- \(\mathrm{Z=\dfrac{molar\:volume\: of\: gas\: at\: same\:\mathit{T}\:and\:\mathit{P}}{molar\: volume\: of\: ideal\: gas\: at\: same\:\mathit{T}\:and\:\mathit{P}}}=\left(\dfrac{P×V_m}{R×T}\right)_\ce{measured}\)
- \(\left(P+\dfrac{n^2a}{V^2}\right)×(V−nb)=nRT\)
Glosario
- factor de compresibilidad (Z)
- relación del volumen molar medido experimentalmente para un gas a su volumen molar calculado a partir de la ecuación de gas ideal
- ecuación de van der Waals
- versión modificada de la ecuación de gas ideal que contiene términos adicionales para tener en cuenta el comportamiento del gas no ideal


