14.3: Fortalezas Relativas de Ácidos y Bases
- Page ID
- 75856
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
- Evaluar las fuerzas relativas de ácidos y bases según sus constantes de ionización
- Racionalizar tendencias en la fuerza ácido-base en relación con la estructura molecular
- Realizar cálculos de equilibrio para sistemas ácido-base débiles
Podemos clasificar las fortalezas de los ácidos por la medida en que se ionizan en solución acuosa. La reacción de un ácido con agua viene dada por la expresión general:
\[\ce{HA}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{A-}(aq) \nonumber \]
El agua es la base que reacciona con el ácido\(\ce{HA}\),\(\ce{A^{−}}\) es la base conjugada del ácido\(\ce{HA}\), y el ion hidronio es el ácido conjugado del agua. Un ácido fuerte produce el 100% (o muy casi) de\(\ce{H3O+}\) y\(\ce{A^{−}}\) cuando el ácido se ioniza en agua; La figura\(\PageIndex{1}\) enumera varios ácidos fuertes. Un ácido débil da pequeñas cantidades de\(\ce{H3O+}\) y\(\ce{A^{−}}\).
| Seis Ácidos Fuertes | Seis bases fuertes | ||
|---|---|---|---|
| \(\ce{HClO4}\) | ácido perclórico | \(\ce{LiOH}\) | hidróxido de litio |
| \(\ce{HCl}\) | ácido clorhídrico | \(\ce{NaOH}\) | hidróxido de sodio |
| \(\ce{HBr}\) | ácido bromhídrico | \(\ce{KOH}\) | hidróxido de potasio |
| \(\ce{HI}\) | ácido yodhídrico | \(\ce{Ca(OH)2}\) | hidróxido de calcio |
| \(\ce{HNO3}\) | ácido nítrico | \(\ce{Sr(OH)2}\) | hidróxido de estroncio |
| \(\ce{H2SO4}\) | ácido sulfúrico | \(\ce{Ba(OH)2}\) | hidróxido de bario |
Las resistencias relativas de los ácidos se pueden determinar midiendo sus constantes de equilibrio en soluciones acuosas. En soluciones de la misma concentración, los ácidos más fuertes se ionizan en mayor medida, y así producen mayores concentraciones de iones hidronio que los ácidos más débiles. La constante de equilibrio para un ácido se llama constante de ionización ácida, K a. Para la reacción de un ácido\(\ce{HA}\):
\[\ce{HA}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{A-}(aq) \nonumber \]
escribimos la ecuación para la constante de ionización como:
\[K_\ce{a}=\ce{\dfrac{[H3O+][A- ]}{[HA]}} \nonumber \]
donde las concentraciones son las que están en equilibrio. Como se señala en la sección sobre constantes de equilibrio, aunque el agua es un reactivo en la reacción, también es el disolvente, por lo que su actividad tiene un valor de 1, lo que no cambia el valor de\(K_a\).
Es un error común afirmar que la concentración molar del disolvente está involucrada de alguna manera en la ley de equilibrio. Este error es resultado de un malentendido de la termodinámica de solución. Por ejemplo, a menudo se afirma que K a = K eq [H 2 O] para soluciones acuosas. Esta ecuación es incorrecta porque es una interpretación errónea de la ecuación correcta K a = K eq (\(\textit{a}_{H_2O}\)). Porque\(\textit{a}_{H_2O}\) = 1 para una solución diluida, K a = K eq (1), o K a = K eq.
Cuanto mayor sea el\(K_a\) de un ácido, mayor será la concentración\(\ce{H3O+}\) y\(\ce{A^{−}}\) relativa a la concentración del ácido no ionizado,\(\ce{HA}\). Así, un ácido más fuerte tiene una constante de ionización mayor que un ácido más débil. Las constantes de ionización aumentan a medida que aumentan las fuerzas de los ácidos.
Los siguientes datos sobre las constantes de ionización ácida indican el orden de concentración ácida:\(\ce{CH3CO2H} < \ce{HNO2} < \ce{HSO4-}\)
\[ \begin{aligned} \ce{CH3CO2H}(aq) + \ce{H2O}(l) &⇌\ce{H3O+}(aq)+\ce{CH3CO2-}(aq) \quad &K_\ce{a}=1.8×10^{−5} \\[4pt] \ce{HNO2}(aq)+\ce{H2O}(l) &⇌\ce{H3O+}(aq)+\ce{NO2-}(aq) &K_\ce{a}=4.6×10^{-4} \\[4pt] \ce{HSO4-}(aq)+\ce{H2O}(l) &⇌\ce{H3O+}(aq)+\ce{SO4^2-}(aq) & K_\ce{a}=1.2×10^{−2} \end{aligned} \nonumber \]
Otra medida de la fuerza de un ácido es su porcentaje de ionización. El porcentaje de ionización de un ácido débil es la relación entre la concentración del ácido ionizado y la concentración inicial de ácido, multiplicado por 100:
\[\% \:\ce{ionization}=\ce{\dfrac{[H3O+]_{eq}}{[HA]_0}}×100\% \label{PercentIon} \]
Debido a que la relación incluye la concentración inicial, el porcentaje de ionización para una solución de un ácido débil determinado varía dependiendo de la concentración original del ácido, y en realidad disminuye con el aumento de la concentración de ácido.
Calcular el porcentaje de ionización de una solución 0.125- M de ácido nitroso (un ácido débil), con un pH de 2.09.
Solución
El porcentaje de ionización para un ácido es:
\[\ce{\dfrac{[H3O+]_{eq}}{[HNO2]_0}}×100 \nonumber \]
La ecuación química para la disociación del ácido nitroso es:
\[\ce{HNO2}(aq)+\ce{H2O}(l)⇌\ce{NO2-}(aq)+\ce{H3O+}(aq). \nonumber \]
Ya que\(10^{−pH} = \ce{[H3O+]}\), encontramos que\(10^{−2.09} = 8.1 \times 10^{−3}\, M\), por lo que ese porcentaje de ionización (Ecuación\ ref {Percention}) es:
\[\dfrac{8.1×10^{−3}}{0.125}×100=6.5\% \nonumber \]
Recuerde, el logaritmo 2.09 indica una concentración de iones hidronio con solo dos cifras significativas.
Calcular el porcentaje de ionización de una solución 0.10 M de ácido acético con un pH de 2.89.
- Contestar
-
1.3% ionizado
Podemos clasificar las fortalezas de las bases por su tendencia a formar iones hidróxido en solución acuosa. La reacción de una base de Brønsted-Lowry con agua viene dada por:
\[\ce{B}(aq)+\ce{H2O}(l)⇌\ce{HB+}(aq)+\ce{OH-}(aq) \nonumber \]
El agua es el ácido que reacciona con la base,\(\ce{HB^{+}}\) es el ácido conjugado de la base\(\ce{B}\), y el ion hidróxido es la base conjugada del agua. Una base fuerte produce 100% (o muy casi) de OH − y HB + cuando reacciona con agua; la Figura\(\PageIndex{1}\) enumera varias bases fuertes. Una base débil produce una pequeña proporción de iones hidróxido. Los hidróxidos iónicos solubles como el NaOH se consideran bases fuertes porque se disocian completamente cuando se disuelven en agua.
Como hicimos con los ácidos, podemos medir las resistencias relativas de las bases midiendo su constante de ionización de bases (K b) en soluciones acuosas. En soluciones de la misma concentración, las bases más fuertes se ionizan en mayor medida, y así producen concentraciones de iones hidróxido mayores que las bases más débiles. Una base más fuerte tiene una constante de ionización más grande que una base más débil. Para la reacción de una base,\(\ce{B}\):
\[\ce{B}(aq)+\ce{H2O}(l)⇌\ce{HB+}(aq)+\ce{OH-}(aq), \nonumber \]
escribimos la ecuación para la constante de ionización como:
\[K_\ce{b}=\ce{\dfrac{[HB+][OH- ]}{[B]}} \nonumber \]
donde las concentraciones son las que están en equilibrio. Nuevamente, no vemos agua en la ecuación porque el agua es el solvente y tiene una actividad de 1. Las reacciones químicas y constantes de ionización de las tres bases mostradas son:
\[ \begin{aligned} \ce{NO2-}(aq)+\ce{H2O}(l) &⇌\ce{HNO2}(aq)+\ce{OH-}(aq) \quad &K_\ce{b}=2.17×10^{−11} \\[4pt] \ce{CH3CO2-}(aq)+\ce{H2O}(l) &⇌\ce{CH3CO2H}(aq)+\ce{OH-}(aq) &K_\ce{b}=5.6×10^{−10} \\[4pt] \ce{NH3}(aq)+\ce{H2O}(l) &⇌\ce{NH4+}(aq)+\ce{OH-}(aq) &K_\ce{b}=1.8×10^{−5} \end{aligned} \nonumber \]
Una tabla de constantes de ionización de bases débiles aparece en el Cuadro E2. Al igual que con los ácidos, el porcentaje de ionización se puede medir para soluciones básicas, pero variará dependiendo de la constante de ionización de la base y la concentración inicial de la solución.
Considere las reacciones de ionización para un par ácido-base conjugado,\(\ce{HA − A^{−}}\):
\[\ce{HA}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{A-}(aq) \nonumber \]
con\(K_\ce{a}=\ce{\dfrac{[H3O+][A- ]}{[HA]}}\).
\[\ce{A-}(aq)+\ce{H2O}(l)⇌\ce{OH-}(aq)+\ce{HA}(aq) \nonumber \]
con\(K_\ce{b}=\ce{\dfrac{[HA][OH]}{[A- ]}}\).
Al sumar estas dos ecuaciones químicas se obtiene la ecuación para la autoionización del agua:
\[\begin{align*} \cancel{\ce{HA}(aq)}+\ce{H2O}(l)+\cancel{\ce{A-}(aq)}+\ce{H2O}(l) &⇌ \ce{H3O+}(aq)+\cancel{\ce{A-}(aq)}+\ce{OH-}(aq)+\cancel{\ce{HA}(aq)} \\[4pt] \ce{2H2O}(l) &⇌\ce{H3O+}(aq)+\ce{OH-}(aq) \end{align*} \nonumber \]
Como se muestra en el capítulo anterior sobre equilibrio, la\(K\) expresión para una ecuación química derivada de sumar dos o más ecuaciones es el producto matemático de las\(K\) expresiones de las otras ecuaciones. Multiplicando las expresiones de acción masiva juntas y cancelando términos comunes, vemos que:
\[K_\ce{a}×K_\ce{b}=\ce{\dfrac{[H3O+][A- ]}{[HA]}×\dfrac{[HA][OH- ]}{[A- ]}}=\ce{[H3O+][OH- ]}=K_\ce{w} \nonumber \]
Por ejemplo, la constante de ionización ácida del ácido acético (CH 3 COOH) es 1.8 × 10 −5, y la constante de ionización de base de su base conjugada, ion acetato (\(\ce{CH3COO-}\)), es 5.6 × 10 −10. El producto de estas dos constantes es efectivamente igual a\(K_w\):
\[K_\ce{a}×K_\ce{b}=(1.8×10^{−5})×(5.6×10^{−10})=1.0×10^{−14}=K_\ce{w} \nonumber \]
El grado en que un ácido,\(\ce{HA}\), dona protones a las moléculas de agua depende de la fuerza de la base conjugada\(\ce{A^{−}}\),, del ácido. Si\(\ce{A^{−}}\) es una base fuerte, los protones que se donen a las moléculas de agua son recapturados por\(\ce{A^{−}}\). Así hay relativamente poco\(\ce{A^{−}}\) y\(\ce{H3O+}\) en solución, y el ácido,\(\ce{HA}\), es débil. Si\(\ce{A^{−}}\) es una base débil, el agua se une más fuertemente a los protones, y la solución contiene principalmente\(\ce{A^{−}}\) y\(\ce{H3O^{+}}\) —el ácido es fuerte. Los ácidos fuertes forman bases conjugadas muy débiles y los ácidos débiles forman bases conjugadas más fuertes (Figura\(\PageIndex{2}\)).
 "style="ancho: 784px; alto: 271px;” width="784px” height="271px” src=”/@api /deki/files/65684/CNX_Chem_14_03_strengths.jpg “>
"style="ancho: 784px; alto: 271px;” width="784px” height="271px” src=”/@api /deki/files/65684/CNX_Chem_14_03_strengths.jpg “>
La figura\(\PageIndex{3}\) enumera una serie de ácidos y bases en orden de las fuerzas decrecientes de los ácidos y las correspondientes resistencias crecientes de las bases. El ácido y la base en una fila dada se conjugan entre sí.
Los primeros seis ácidos en la Figura\(\PageIndex{3}\) son los ácidos fuertes más comunes. Estos ácidos están completamente disociados en solución acuosa. Las bases conjugadas de estos ácidos son bases más débiles que el agua. Cuando uno de estos ácidos se disuelve en agua, sus protones se transfieren completamente al agua, la base más fuerte.
Aquellos ácidos que se encuentran entre el ion hidronio y el agua en la Figura\(\PageIndex{3}\) forman bases conjugadas que pueden competir con el agua por la posesión de un protón. Tanto los iones hidronio como las moléculas de ácido no ionizado están presentes en equilibrio en una solución de uno de estos ácidos. Los compuestos que son ácidos más débiles que el agua (los que se encuentran debajo del agua en la columna de ácidos) en la Figura no\(\PageIndex{3}\) muestran ningún comportamiento ácido observable cuando se disuelven en agua. Sus bases conjugadas son más fuertes que el ion hidróxido, y si se formara alguna base conjugada, reaccionaría con agua para volver a formar el ácido.
 "style="ancho: 798px; alto: 715px;” width="798px” height="715px” src=”/@api /deki/files/65685/CNX_Chem_14_03_Corresp.jpg “>
"style="ancho: 798px; alto: 715px;” width="798px” height="715px” src=”/@api /deki/files/65685/CNX_Chem_14_03_Corresp.jpg “>
El grado en que una base forma ión hidróxido en solución acuosa depende de la fuerza de la base respecto a la del ión hidróxido, como se muestra en la última columna de la Figura\(\PageIndex{3}\). Una base fuerte, como una de las que se encuentran debajo del ion hidróxido, acepta protones del agua para producir el 100% del ácido conjugado y el ion hidróxido. Esas bases que se encuentran entre el agua y el ion hidróxido aceptan protones del agua, pero resulta una mezcla del ión hidróxido y la base. Las bases que son más débiles que el agua (las que se encuentran por encima del agua en la columna de bases) no muestran ningún comportamiento básico observable en solución acuosa.
Utilice el\(K_b\) para el ion nitrito,\(\ce{NO2-}\), para calcular el\(K_a\) para su ácido conjugado.
Solución
K b for\(\ce{NO2-}\) se da en esta sección como 2.17 × 10 −11. El ácido conjugado de\(\ce{NO2-}\) es HNO 2; K a para HNO 2 se puede calcular usando la relación:
\[K_\ce{a}×K_\ce{b}=1.0×10^{−14}=K_\ce{w} \nonumber \]
Resolviendo para K a, obtenemos:
\[\begin{align*} K_\ce{a} &=\dfrac{K_\ce{w}}{K_\ce{b}} \\[4pt] &=\dfrac{1.0×10^{−14}}{2.17×10^{−11}} \\[4pt] &=4.6×10^{−4} \end{align*} \nonumber \]
Esta respuesta se puede verificar encontrando la K a para HNO 2 en la Tabla E1
Podemos determinar las fuerzas ácidas relativas de\(\ce{NH4+}\) y\(\ce{HCN}\) comparando sus constantes de ionización. La constante de ionización de\(\ce{HCN}\) se da en la Tabla E1 como 4.9 × 10 −10. La constante de ionización de no\(\ce{NH4+}\) está listada, pero la constante de ionización de su base conjugada\(\ce{NH3}\),, se enumera como 1.8 × 10 −5. Determinar la constante de ionización de\(\ce{NH4+}\), y decidir cuál es el ácido más fuerte,\(\ce{HCN}\) o\(\ce{NH4+}\).
- Contestar
-
\(\ce{NH4+}\)es el ácido ligeramente más fuerte (K a para\(\ce{NH4+}\) = 5.6 × 10 −10).
La ionización de ácidos débiles y bases débiles
Muchos ácidos y bases son débiles; es decir, no se ionizan completamente en solución acuosa. Una solución de un ácido débil en agua es una mezcla del ácido no ionizado, el ion hidronio y la base conjugada del ácido, con el ácido no ionizado presente en la mayor concentración. Así, un ácido débil aumenta la concentración de iones hidronio en una solución acuosa (pero no tanto como la misma cantidad de un ácido fuerte).
El ácido acético (\(\ce{CH3CO2H}\)) es un ácido débil. Cuando agregamos ácido acético al agua, se ioniza en pequeña medida según la ecuación:
\[\ce{CH3CO2H}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CH3CO2-}(aq) \nonumber \]
dando una mezcla de equilibrio con la mayor parte del ácido presente en la forma no ionizada (molecular). Este equilibrio, al igual que otros equilibrios, es dinámico; las moléculas de ácido acético donan iones de hidrógeno a las moléculas de agua y forman iones hidronio e iones acetato a la misma velocidad que los iones hidronio donan iones de hidrógeno a iones acetato para reformar las moléculas de ácido acético y las moléculas de agua. Podemos decir midiendo el pH de una solución acuosa de concentración conocida que solo una fracción del ácido débil se ioniza en cualquier momento (Figura\(\PageIndex{4}\)). El ácido débil restante está presente en la forma no ionizada.
Para el ácido acético, en equilibrio:
\[K_\ce{a}=\ce{\dfrac{[H3O+][CH3CO2- ]}{[CH3CO2H]}}=1.8 \times 10^{−5} \nonumber \]

| Reacción de ionización | K a 25 °C |
|---|---|
| \(\ce{HSO4- + H2O ⇌ H3O+ + SO4^2-}\) | 1.2 × 10 −2 |
| \(\ce{HF + H2O ⇌ H3O+ + F-}\) | 3.5 × 10 −4 |
| \(\ce{HNO2 + H2O ⇌ H3O+ + NO2-}\) | 4.6 × 10 −4 |
| \(\ce{HNCO + H2O ⇌ H3O+ + NCO-}\) | 2 × 10 −4 |
| \(\ce{HCO2H + H2O ⇌ H3O+ + HCO2-}\) | 1.8 × 10 −4 |
| \(\ce{CH3CO2H + H2O ⇌ H3O+ + CH3CO2-}\) | 1.8 × 10 −5 |
| \(\ce{HCIO + H2O ⇌ H3O+ + CIO-}\) | 2.9 × 10 −8 |
| \(\ce{HBrO + H2O ⇌ H3O+ + BrO-}\) | 2.8 × 10 −9 |
| \(\ce{HCN + H2O ⇌ H3O+ + CN-}\) | 4.9 × 10 −10 |
El cuadro\(\PageIndex{1}\) da las constantes de ionización para varios ácidos débiles; las constantes de ionización adicionales se pueden encontrar en la Tabla E1.
En equilibrio, una solución de una base débil en agua es una mezcla de la base no ionizada, el ácido conjugado de la base débil y el ion hidróxido con la base no ionizada presente en la mayor concentración. Así, una base débil aumenta la concentración de iones hidróxido en una solución acuosa (pero no tanto como la misma cantidad de una base fuerte).
Por ejemplo, una solución de la base débil trimetilamina, (CH 3) 3 N, en agua reacciona de acuerdo con la ecuación:
\[\ce{(CH3)3N}(aq)+\ce{H2O}(l)⇌\ce{(CH3)3NH+}(aq)+\ce{OH-}(aq) \nonumber \]
Esto da una mezcla de equilibrio con la mayor parte de la base presente como la amina no ionizada. Este equilibrio es análogo al descrito para los ácidos débiles.
Podemos confirmar midiendo el pH de una solución acuosa de una base débil de concentración conocida que solo una fracción de la base reacciona con el agua (Figura 14.4.5). La base débil restante está presente como la forma sin reaccionar. La constante de equilibrio para la ionización de una base débil\(K_b\),, se denomina constante de ionización de la base débil, y es igual al cociente de reacción cuando la reacción está en equilibrio. Para trimetilamina, en equilibrio:
\[K_\ce{b}=\ce{\dfrac{[(CH3)3NH+][OH- ]}{[(CH3)3N]}} \nonumber \]
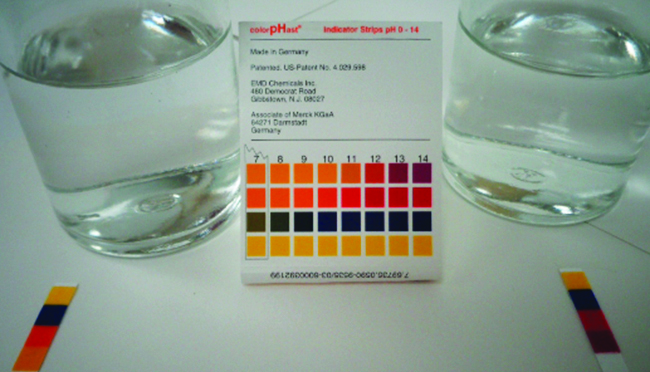
Las constantes de ionización de varias bases débiles se dan en la Tabla\(\PageIndex{2}\) y Tabla E2.
| Reacción de ionización | K b a 25 °C |
|---|---|
| \(\ce{(CH3)2NH + H2O ⇌ (CH3)2NH2+ + OH-}\) | 5.9 × 10 −4 |
| \(\ce{CH3NH2 + H2O ⇌ CH3NH3+ + OH-}\) | 4.4 × 10 −4 |
| \(\ce{(CH3)3N + H2O ⇌ (CH3)3NH+ + OH-}\) | 6.3 × 10 −5 |
| \(\ce{NH3 + H2O ⇌ NH4+ + OH-}\) | 1.8 × 10 −5 |
| \(\ce{C6H5NH2 + H2O ⇌ C6N5NH3+ + OH-}\) | 4.3 × 10 −10 |
El ácido acético es el ingrediente principal en el vinagre; por eso tiene un sabor agrio. En equilibrio, una solución contiene [CH 3 CO 2 H] = 0.0787 M y\(\ce{[H3O+]}=\ce{[CH3CO2- ]}=0.00118\:M\). ¿Cuál es el valor de\(K_a\) para el ácido acético?

Solución
Se nos pide calcular una constante de equilibrio a partir de concentraciones de equilibrio. En equilibrio, el valor de la constante de equilibrio es igual al cociente de reacción para la reacción:
\[\ce{CH3CO2H}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CH3CO2-}(aq) \nonumber \]
\[\begin{align*} K_\ce{a} &=\ce{\dfrac{[H3O+][CH3CO2- ]}{[CH3CO2H]}} \\[4pt] &=\dfrac{(0.00118)(0.00118)}{0.0787} \\[4pt] &=1.77×10^{−5} \end{align*} \nonumber \]
Cuál es la constante de equilibrio para la ionización del\(\ce{HSO4-}\) ion, el ácido débil utilizado en algunos limpiadores domésticos:
\[\ce{HSO4-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{SO4^2-}(aq) \nonumber \]
En una mezcla de NaHSO 4 y Na 2 SO 4 en equilibrio,\(\ce{[H3O+]}\) = 0.027 M;\(\ce{[HSO4- ]}=0.29\:M\); y\(\ce{[SO4^2- ]}=0.13\:M\).
- Contestar
-
\(K_a\)para\(\ce{HSO_4^-}= 1.2 ×\times 10^{−2}\)
Cafeína, C 8 H 10 N 4 O 2 es una base débil. ¿Cuál es el valor de K b para la cafeína si una solución en equilibrio tiene [C 8 H 10 N 4 O 2] = 0.050 M,\(\ce{[C8H10N4O2H+]}\) = 5.0 × 10 −3 M, y [OH −] = 2.5 × 10 −3 M?
Solución
En equilibrio, el valor de la constante de equilibrio es igual al cociente de reacción para la reacción:
\[\ce{C8H10N4O2}(aq)+\ce{H2O}(l)⇌\ce{C8H10N4O2H+}(aq)+\ce{OH-}(aq) \nonumber \]
por lo
\[K_\ce{b}=\ce{\dfrac{[C8H10N4O2H+][OH- ]}{[C8H10N4O2]}}=\dfrac{(5.0×10^{−3})(2.5×10^{−3})}{0.050}=2.5×10^{−4} \nonumber \]
Cuál es la constante de equilibrio para la ionización del\(\ce{HPO4^2-}\) ion, una base débil:
\[\ce{HPO4^2-}(aq)+\ce{H2O}(l)⇌\ce{H2PO4-}(aq)+\ce{OH-}(aq) \nonumber \]
En una solución que contiene una mezcla de\(\ce{NaH2PO4}\) y\(\ce{Na2HPO4}\) en equilibrio con:
- \([\ce{OH^{−}}] = 1.3 × 10^{−6} M\)
- \(\ce{[H2PO4^{-}]=0.042\:M}\)y
- \(\ce{[HPO4^{2-}]=0.341\:M}\).
- Contestar
-
K b para\(\ce{HPO4^2-}=1.6×10^{−7} \)
El pH de una solución 0.0516- M de ácido nitroso,\(\ce{HNO2}\), es 2.34. ¿Cuál es su\(K_a\)?
\[\ce{HNO2}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{NO2-}(aq) \nonumber \]
Solución
Determinamos una constante de equilibrio a partir de las concentraciones iniciales de HNO 2\(\ce{H3O+}\), y así\(\ce{NO2-}\) como una de las concentraciones finales, la concentración de ión hidronio en equilibrio. (Recuerde que el pH es simplemente otra forma de expresar la concentración de iones hidronio).
Podemos resolver este problema con los siguientes pasos en los que x es un cambio en la concentración de una especie en la reacción:
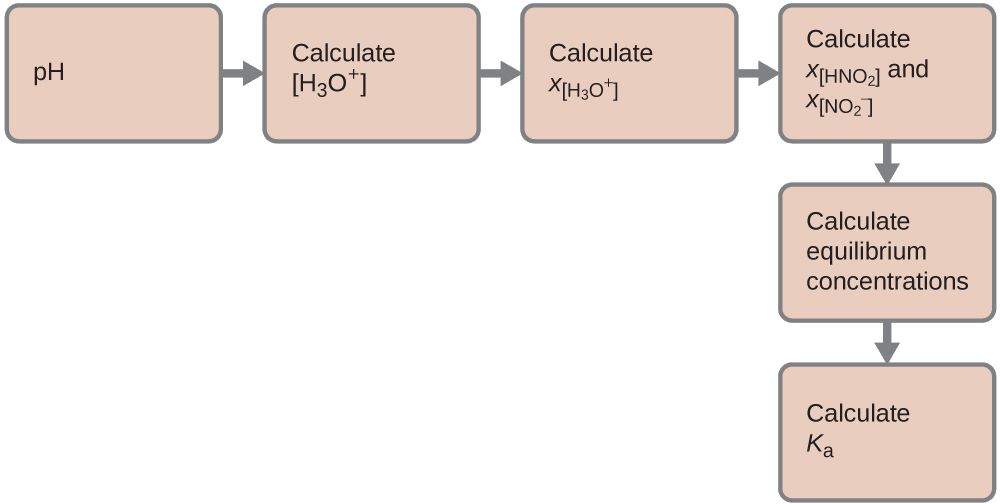
Podemos resumir las diversas concentraciones y cambios como se muestra aquí. Debido a que el agua es el disolvente, tiene una actividad fija igual a 1. Cualquier pequeña cantidad de agua producida o consumida durante la reacción no cambiará el papel del agua como disolvente, por lo que el valor de su actividad permanece igual a 1 a lo largo de la reacción.
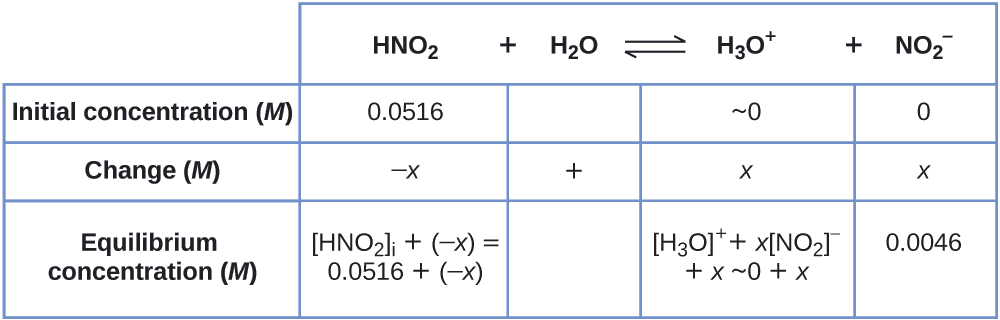
Para obtener los diversos valores en la tabla ICE (Inicial, Cambio, Equilibrio), primero calculamos\(\ce{[H3O+]}\), la concentración de equilibrio de\(\ce{H3O+}\), a partir del pH:
\[\ce{[H3O+]}=10^{−2.34}=0.0046\:M \nonumber \]
El cambio en la concentración de\(\ce{H3O+}\),\(x_{\ce{[H3O+]}}\), es la diferencia entre la concentración de equilibrio de H 3 O +, que determinamos a partir del pH, y la concentración inicial,\(\mathrm{[H_3O^+]_i}\). La concentración inicial de\(\ce{H3O+}\) es su concentración en agua pura, que es tanto menor que la concentración final que la aproximamos como cero (~0).
El cambio en la concentración de\(\ce{NO2-}\) es igual al cambio en la concentración de\(\ce{[H3O+]}\). Por cada 1 mol de\(\ce{H3O+}\) que se forma, 1 mol de\(\ce{NO2-}\) formas. La concentración de equilibrio de HNO 2 es igual a su concentración inicial más el cambio en su concentración.
Ahora podemos rellenar la tabla ICE con las concentraciones en equilibrio, como se muestra aquí:
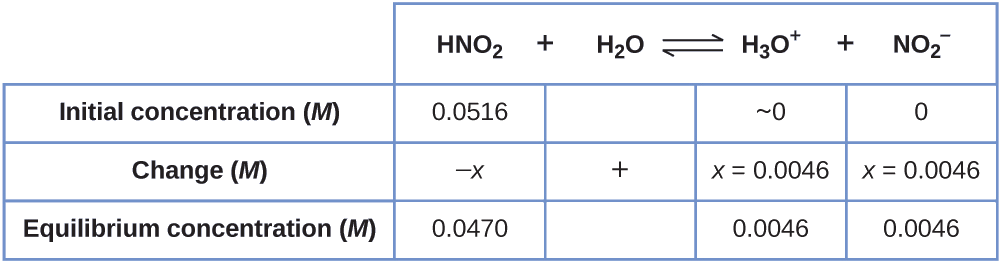
Finalmente, calculamos el valor de la constante de equilibrio utilizando los datos de la tabla:
\[K_\ce{a}=\ce{\dfrac{[H3O+][NO2- ]}{[HNO2]}}=\dfrac{(0.0046)(0.0046)}{(0.0470)}=4.5×10^{−4} \nonumber \]
El pH de una solución de amoníaco doméstico, una solución 0.950- M de NH 3, es 11.612. Qué es K b para NH 3.
- Contestar
-
\(K_b = 1.8 × 10^{−5}\)
El ácido fórmico, HCO 2 H, es el irritante que causa la reacción del cuerpo a las picaduras de hormigas.

¿Cuál es la concentración de ión hidronio y el pH en una solución 0.534- M de ácido fórmico?
\[\ce{HCO2H}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO2-}(aq) \hspace{20px} K_\ce{a}=1.8×10^{−4} \nonumber \]
Soluti en
1. Determinar x y concentraciones de equilibrio. La expresión de equilibrio es:
\[\ce{HCO2H}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{HCO2-}(aq) \nonumber \]
Debido a que el agua es el disolvente, tiene una actividad fija igual a 1. Cualquier pequeña cantidad de agua producida o consumida durante la reacción no cambiará el papel del agua como disolvente, por lo que el valor de su actividad permanece igual a 1 a lo largo de la reacción por lo que no es necesario considerarla al configurar la tabla ICE.
La tabla muestra las concentraciones iniciales (concentraciones antes de que el ácido se ioniza), los cambios en la concentración y las concentraciones de equilibrio a continuación (los datos dados en el problema aparecen en color):
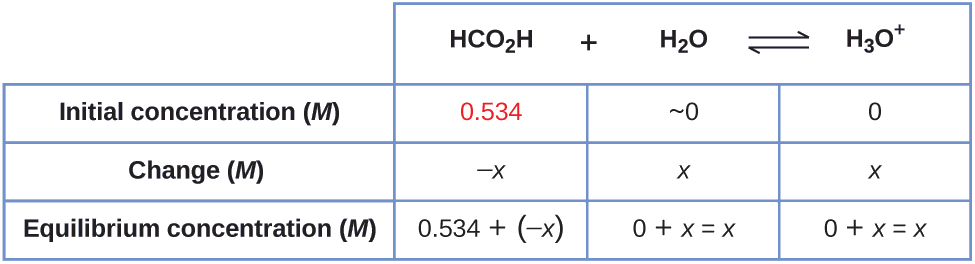
2. Resolver para\(x\) y las concentraciones de equilibrio. En equilibrio:
\[\begin{align*} K_\ce{a} &=1.8×10^{−4}=\ce{\dfrac{[H3O+][HCO2- ]}{[HCO2H]}} \\[4pt] &=\dfrac{(x)(x)}{0.534−x}=1.8×10^{−4} \end{align*} \nonumber \]
Ahora resuelve para\(x\). Debido a que la concentración inicial de ácido es razonablemente grande y\(K_a\) es muy pequeña, suponemos que\(x << 0.534\), lo que nos permite simplificar el término denominador como\((0.534 − x) = 0.534\). Esto da:
\[K_\ce{a}=1.8×10^{−4}=\dfrac{x^{2}}{0.534} \nonumber \]
Resolver para\(x\) lo siguiente:
\[\begin{align*} x^2 &=0.534×(1.8×10^{−4}) \\[4pt] &=9.6×10^{−5} \\[4pt] x &=\sqrt{9.6×10^{−5}} \\[4pt] &=9.8×10^{−3} \end{align*} \nonumber \]
Para verificar la suposición que\(x\) es pequeña en comparación con 0.534, calculamos:
\[\begin{align*} \dfrac{x}{0.534} &=\dfrac{9.8×10^{−3}}{0.534} \\[4pt] &=1.8×10^{−2} \, \textrm{(1.8% of 0.534)} \end{align*} \nonumber \]
\(x\)es inferior al 5% de la concentración inicial; el supuesto es válido.
Encontramos la concentración de equilibrio del ion hidronio en esta solución de ácido fórmico a partir de su concentración inicial y el cambio en esa concentración como se indica en la última línea de la tabla:
\[\begin{align*} \ce{[H3O+]} &=~0+x=0+9.8×10^{−3}\:M. \\[4pt] &=9.8×10^{−3}\:M \end{align*} \nonumber \]
El pH de la solución se puede encontrar tomando el log negativo del\(\ce{[H3O+]}\), así:
\[pH = −\log(9.8×10^{−3})=2.01 \nonumber \]
Sólo una pequeña fracción de un ácido débil ioniza en solución acuosa. ¿Cuál es el porcentaje de ionización de ácido acético en una solución 0.100- M de ácido acético, CH 3 CO 2 H?
\[\ce{CH3CO2H}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{CH3CO2-}(aq) \hspace{20px} K_\ce{a}=1.8×10^{−5} \nonumber \]
- Insinuación
-
Determinar\(\ce{[CH3CO2- ]}\) en equilibrio.) Recordemos que el porcentaje de ionización es la fracción de ácido acético que se ioniza × 100, o\(\ce{\dfrac{[CH3CO2- ]}{[CH3CO2H]_{initial}}}×100\).
- Contestar
-
porcentaje de ionización = 1.3%
El siguiente ejemplo muestra que la concentración de productos producidos por la ionización de una base débil se puede determinar mediante la misma serie de etapas utilizadas con un ácido débil.
Encuentra la concentración de ion hidróxido en una solución 0.25- M de trimetilamina, una base débil:
\[\ce{(CH3)3N}(aq)+\ce{H2O}(l)⇌\ce{(CH3)3NH+}(aq)+\ce{OH-}(aq) \hspace{20px} K_\ce{b}=6.3×10^{−5} \nonumber \]
Solución Este problema requiere que calculemos una concentración de equilibrio determinando los cambios de concentración a medida que la ionización de una base va al equilibrio. La solución se aborda de la misma manera que para la ionización del ácido fórmico en el Ejemplo\(\PageIndex{6}\). Los reactivos y productos serán diferentes y los números serán diferentes, pero la lógica será la misma:

1. Determinar x y concentraciones de equilibrio. La tabla muestra los cambios y concentraciones:
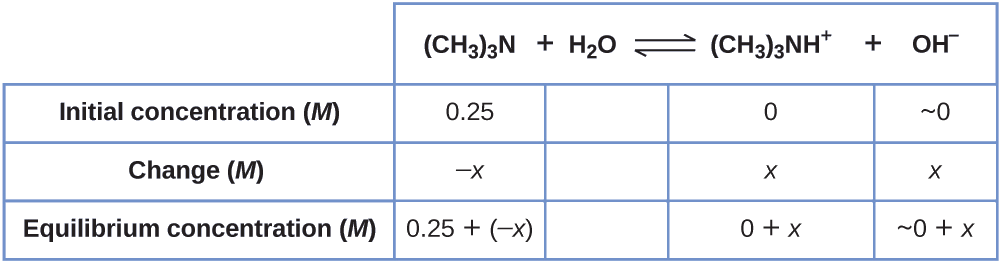
2. Resolver para\(x\) y las concentraciones de equilibrio. En equilibrio:
\[K_\ce{b}=\ce{\dfrac{[(CH3)3NH+][OH- ]}{[(CH3)3N]}}=\dfrac{(x)(x)}{0.25−x=}6.3×10^{−5} \nonumber \]
Si asumimos que x es pequeño con relación a 0.25, entonces podemos reemplazar (0.25 − x) en la ecuación anterior con 0.25. Resolver la ecuación simplificada da:
\[x=4.0×10^{−3} \nonumber \]
Este cambio es menor al 5% de la concentración inicial (0.25), por lo que se justifica la suposición.
Recordemos que, para este cálculo,\(x\) es igual a la concentración de equilibrio del ion hidróxido en la solución (ver tabulación anterior):
\[\begin{align*} (\ce{[OH- ]}=~0+x=x=4.0×10^{−3}\:M \\[4pt] &=4.0×10^{−3}\:M \end{align*} \nonumber \]
Luego calcule PoH de la siguiente manera:
\[\ce{pOH}=−\log(4.3×10^{−3})=2.40 \nonumber \]
Utilizando la relación introducida en la sección anterior de este capítulo:
\[\mathrm{pH + pOH=p\mathit{K}_w=14.00}\nonumber \]
permite el cálculo del pH:
\[\mathrm{pH=14.00−pOH=14.00−2.37=11.60} \nonumber \]
Revisar la obra. Un chequeo de nuestra aritmética lo demuestra\(K_b = 6.3 \times 10^{−5}\).
- Mostrar que el cálculo en el Paso 2 de este ejemplo da una x de 4.3 × 10 −3 y el cálculo en el Paso 3 muestra K b = 6.3 × 10 −5.
- Encuentra la concentración de ion hidróxido en una solución 0.0325- M de amoníaco, una base débil con un K b de 1.76 × 10 −5. Calcular el porcentaje de ionización de amoníaco, la fracción ionizada × 100, o\(\ce{\dfrac{[NH4+]}{[NH3]}}×100 \%\)
- Contestar a
-
\(7.56 × 10^{−4}\, M\), 2.33%
- Respuesta b
-
2.33%
Algunos ácidos débiles y bases débiles se ionizan hasta tal punto que la suposición simplificadora de que x es pequeña en relación con la concentración inicial del ácido o base es inapropiada. A medida que resolvamos para las concentraciones de equilibrio en tales casos, veremos que no podemos descuidar el cambio en la concentración inicial del ácido o base, y debemos resolver las ecuaciones de equilibrio usando la ecuación cuadrática.
El bisulfato de sodio, NaHSO 4, se utiliza en algunos limpiadores domésticos porque contiene el\(\ce{HSO4-}\) ion, un ácido débil. ¿Cuál es el pH de una solución 0.50- M de\(\ce{HSO4-}\)?
\[\ce{HSO4-}(aq)+\ce{H2O}(l)⇌\ce{H3O+}(aq)+\ce{SO4^2-}(aq) \hspace{20px} K_\ce{a}=1.2×10^{−2} \nonumber \]
Soluti en
Necesitamos determinar la concentración de equilibrio del ion hidronio que resulta de la ionización de\(\ce{HSO4-}\) manera que podamos usar\(\ce{[H3O+]}\) para determinar el pH. Como en los ejemplos anteriores, podemos acercarnos a la solución por los siguientes pasos:

1. Determinar\(x\) y concentraciones de equilibrio. Esta tabla muestra los cambios y concentraciones:

2. Resolver para\(x\) y las concentraciones.
A medida que comencemos a resolver para\(x\), encontraremos que esto es más complicado que en ejemplos anteriores. A medida que discutimos estas complicaciones no debemos perder de vista el hecho de que sigue siendo el propósito de este paso determinar el valor de\(x\).
En equilibrio:
\[K_\ce{a}=1.2×10^{−2}=\ce{\dfrac{[H3O+][SO4^2- ]}{[HSO4- ]}}=\dfrac{(x)(x)}{0.50−x} \nonumber \]
Si asumimos que x es pequeño y aproximado (0.50 − x) como 0.50, encontramos:
\[x=7.7×10^{−2} \nonumber \]
Cuando comprobamos la suposición, confirmamos:
\[\dfrac{x}{\mathrm{[HSO_4^- ]_i}} \overset{?}{\le} 0.05 \nonumber \]
que para este sistema es
\[\dfrac{x}{0.50}=\dfrac{7.7×10^{−2}}{0.50}=0.15(15\%) \nonumber \]
El valor de no\(x\) es inferior al 5% de 0.50, por lo que el supuesto no es válido. Necesitamos la fórmula cuadrática para encontrar\(x\).
La ecuación:
\[K_\ce{a}=1.2×10^{−2}=\dfrac{(x)(x)}{0.50−x}\nonumber \]
da
\[6.0×10^{−3}−1.2×10^{−2}x=x^{2+} \nonumber \]
o
\[x^{2+}+1.2×10^{−2}x−6.0×10^{−3}=0 \nonumber \]
Esta ecuación se puede resolver usando la fórmula cuadrática. Para una ecuación de la forma
\[ax^{2+} + bx + c=0, \nonumber \]
\(x\)viene dada por la ecuación cuadrática:
\[x=\dfrac{−b±\sqrt{b^{2+}−4ac}}{2a} \nonumber \]
En este problema,\(a = 1\),\(b = 1.2 × 10^{−3}\), y\(c = −6.0 × 10^{−3}\).
Resolver para x da una raíz negativa (que no puede ser correcta ya que la concentración no puede ser negativa) y una raíz positiva:
\[x=7.2×10^{−2} \nonumber \]
Ahora determine la concentración de iones hidronio y el pH:
\[\begin{align*} \ce{[H3O+]} &=~0+x=0+7.2×10^{−2}\:M \\[4pt] &=7.2×10^{−2}\:M \end{align*} \nonumber \]
El pH de esta solución es:
\[\mathrm{pH=−log[H_3O^+]=−log7.2×10^{−2}=1.14} \nonumber \]
- Demostrar que la fórmula cuadrática da\(x = 7.2 × 10^{−2}\).
- Calcular el pH en una solución 0.010- M de cafeína, una base débil:
\[\ce{C8H10N4O2}(aq)+\ce{H2O}(l)⇌\ce{C8H10N4O2H+}(aq)+\ce{OH-}(aq) \hspace{20px} K_\ce{b}=2.5×10^{−4} \nonumber \]
- Pista
-
Será necesario convertir [OH −] a\(\ce{[H3O+]}\) o PoH a pH hacia el final del cálculo.
- Contestar
-
pH 11.16
Las Fortalezas Relativas de los Ácidos Fuertes y Bases
Los ácidos fuertes, como\(\ce{HCl}\)\(\ce{HBr}\), y\(\ce{HI}\), todos exhiben la misma fuerza en el agua. La molécula de agua es una base tan fuerte en comparación con las bases conjugadas Cl −, Br − e I − que la ionización de estos ácidos fuertes es esencialmente completa en soluciones acuosas. En disolventes menos básicos que el agua\(\ce{HCl}\), encontramos\(\ce{HBr}\), y\(\ce{HI}\) difieren notablemente en su tendencia a ceder un protón al disolvente. Por ejemplo, cuando se disuelve en etanol (una base más débil que el agua), el grado de ionización aumenta en el orden\(\ce{HCl < HBr < HI}\), y así\(\ce{HI}\) se demuestra que es el más fuerte de estos ácidos. La incapacidad para discernir las diferencias de fuerza entre los ácidos fuertes disueltos en el agua se conoce como el efecto nivelador del agua.
El agua también ejerce un efecto nivelador sobre las fortalezas de bases fuertes. Por ejemplo, el ion óxido, O 2-, y el ion amida\(\ce{NH2-}\), son bases tan fuertes que reaccionan completamente con el agua:
\[\ce{O^2-}(aq)+\ce{H2O}(l)⟶\ce{OH-}(aq)+\ce{OH-}(aq) \nonumber \]
\[\ce{NH2-}(aq)+\ce{H2O}(l)⟶\ce{NH3}(aq)+\ce{OH-}(aq) \nonumber \]
Así, O 2− y\(\ce{NH2-}\) parecen tener la misma fuerza base en agua; ambos dan un rendimiento del 100% de ión hidróxido.
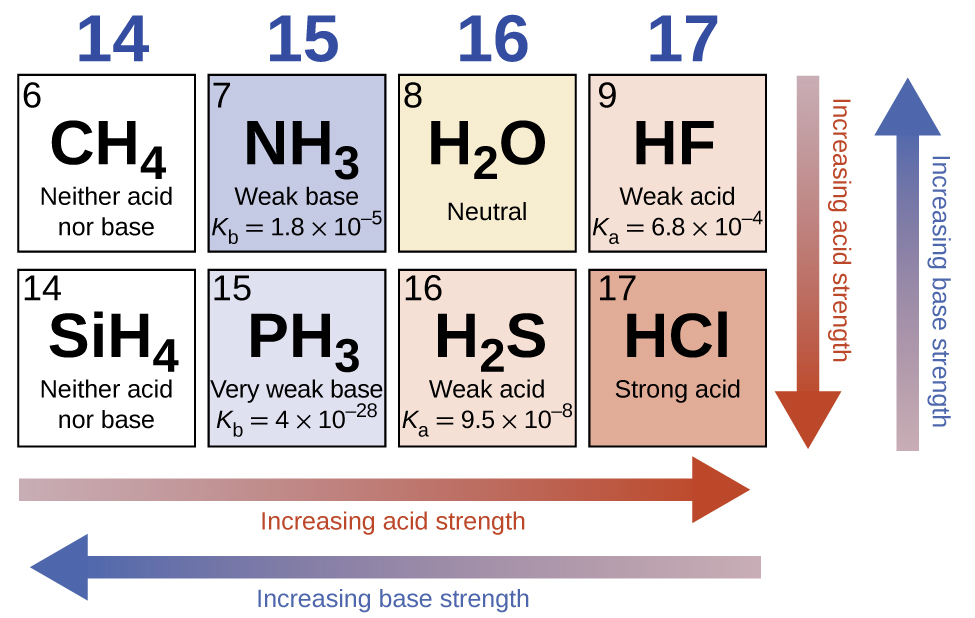
En ausencia de cualquier efecto nivelador, la fuerza ácida de los compuestos binarios de hidrógeno con no metales (A) aumenta a medida que la fuerza del enlace H-A disminuye en un grupo en la tabla periódica. Para el grupo 17, el orden de aumento de la acidez es\(\ce{HF < HCl < HBr < HI}\). Asimismo, para el grupo 16, el orden de aumento de la fuerza ácida es H 2 O < H 2 S < H 2 Se < H 2 Te. A lo largo de una fila en la tabla periódica, la fuerza ácida de los compuestos binarios de hidrógeno aumenta al aumentar la electronegatividad del átomo no metálico debido a que aumenta la polaridad del enlace H-A. Así, el orden de aumento de la acidez (para la eliminación de un protón) a través de la segunda fila es\(\ce{CH4 < NH3 < H2O < HF}\); a través de la tercera fila, es\(\ce{SiH4 < PH3 < H2S < HCl}\) (ver Figura\(\PageIndex{6}\)).
Los compuestos que contienen oxígeno y uno o más grupos hidroxilo (OH) pueden ser ácidos, básicos o anfóteros, dependiendo de la posición en la tabla periódica del átomo central E, el átomo unido al grupo hidroxilo. Dichos compuestos tienen la fórmula general O n E (OH) m, e incluyen ácido sulfúrico\(\ce{O2S(OH)2}\), ácido sulfuroso\(\ce{OS(OH)2}\), ácido nítrico\(\ce{O2NOH}\), ácido perclórico\(\ce{O3ClOH}\), hidróxido de aluminio\(\ce{Al(OH)3}\),\(\ce{Ca(OH)2}\) hidróxido de calcio e hidróxido de potasio,\(\ce{KOH}\):
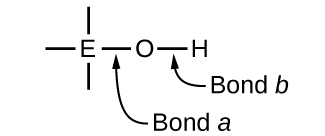
Si el átomo central, E, tiene una electronegatividad baja, su atracción por los electrones es baja. Existe poca tendencia para que el átomo central forme un fuerte enlace covalente con el átomo de oxígeno, y el enlace a entre el elemento y el oxígeno se rompe más fácilmente que el enlace b entre oxígeno e hidrógeno. De ahí que el enlace a sea iónico, los iones hidróxido se liberan a la solución y el material se comporta como una base, este es el caso con Ca (OH) 2 y KOH. La menor electronegatividad es característica de los elementos más metálicos; de ahí que los elementos metálicos formen hidróxidos iónicos que son por definición compuestos básicos.
Si, por otro lado, el átomo E tiene una electronegatividad relativamente alta, atrae fuertemente a los electrones que comparte con el átomo de oxígeno, haciendo del enlace un enlace relativamente fuertemente covalente. El enlace oxígeno-hidrógeno, el enlace b, se debilita debido a que los electrones se desplazan hacia E. El enlace b es polar y libera fácilmente iones de hidrógeno a la solución, por lo que el material se comporta como un ácido. Las altas electronegatividades son características de los elementos más no metálicos. Así, los elementos no metálicos forman compuestos covalentes que contienen grupos -OH ácidos que se denominan oxiácidos.
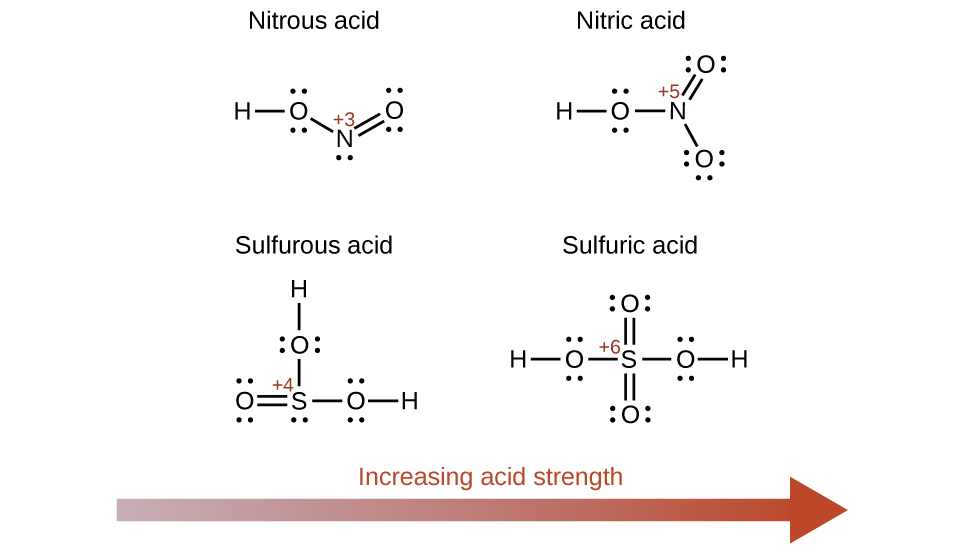
Al aumentar el número de oxidación del átomo central E también se incrementa la acidez de un oxiácido porque esto aumenta la atracción de E por los electrones que comparte con el oxígeno y con ello debilita el enlace O-H. El ácido sulfúrico, H 2 SO 4, o O 2 S (OH) 2 (con un número de oxidación de azufre de +6), es más ácido que el ácido sulfuroso, H 2 SO 3, u OS (OH) 2 (con un número de oxidación de azufre de +4). Asimismo, el ácido nítrico, HNO 3, o O 2 NOH (número de oxidación N = +5), es más ácido que el ácido nitroso, HNO 2, u ONOH (número de oxidación N = +3). En cada uno de estos pares, el número de oxidación del átomo central es mayor para el ácido más fuerte (Figura\(\PageIndex{7}\)).
Los compuestos hidroxi de elementos con electronegatividades intermedias y números de oxidación relativamente altos (por ejemplo, elementos cercanos a la línea diagonal que separa los metales de los no metales en la tabla periódica) suelen ser anfóteros. Esto significa que los compuestos hidroxi actúan como ácidos cuando reaccionan con bases fuertes y como bases cuando reaccionan con ácidos fuertes. El anfoterismo del hidróxido de aluminio, que comúnmente existe como hidrato\(\ce{Al(H2O)3(OH)3}\), se refleja en su solubilidad tanto en ácidos fuertes como en bases fuertes. En bases fuertes, el hidróxido de aluminio hidratado relativamente insoluble\(\ce{Al(H2O)3(OH)3}\),, se convierte en el ion soluble,\(\ce{[Al(H2O)2(OH)4]-}\), por reacción con ion hidróxido:
\[[\ce{Al(H2O)3(OH)3}](aq)+\ce{OH-}(aq)⇌\ce{H2O}(l)+\ce{[Al(H2O)2(OH)4]-}(aq) \nonumber \]
En esta reacción, se transfiere un protón de una de las moléculas H 2 O unidas a aluminio a un ion hidróxido en solución. El\(\ce{Al(H2O)3(OH)3}\) compuesto actúa así como un ácido bajo estas condiciones. Por otro lado, cuando se disuelve en ácidos fuertes, se convierte en el ion soluble\(\ce{[Al(H2O)6]^3+}\) por reacción con ion hidronio:
\[\ce{3H3O+}(aq)+\ce{Al(H2O)3(OH)3}(aq)⇌\ce{Al(H2O)6^3+}(aq)+\ce{3H2O}(l) \nonumber \]
En este caso, los protones se transfieren de iones hidronio en solución a\(\ce{Al(H2O)3(OH)3}\), y el compuesto funciona como base.
Resumen
Las fuerzas de los ácidos y bases de Brønsted-Lowry en soluciones acuosas se pueden determinar por sus constantes de ionización ácida o básica. Los ácidos más fuertes forman bases conjugadas más débiles y los ácidos más débiles forman bases conjugadas más fuertes. Así, los ácidos fuertes se ionizan completamente en solución acuosa debido a que sus bases conjugadas son bases más débiles que el agua. Los ácidos débiles solo se ionizan parcialmente porque sus bases conjugadas son lo suficientemente fuertes como para competir exitosamente con el agua por la posesión de protones. Las bases fuertes reaccionan con el agua para formar cuantitativamente iones hidróxido. Las bases débiles dan solo pequeñas cantidades de ión hidróxido. Las fuerzas de los ácidos binarios aumentan de izquierda a derecha a lo largo de un periodo de la tabla periódica (CH 4 < NH 3 < H 2 O < HF), y aumentan a la baja un grupo (HF < HCl < HBr < HI). Las fuerzas de los oxiácidos que contienen el mismo elemento central aumentan a medida que aumenta el número de oxidación del elemento (H 2 SO 3 < H 2 SO 4). Las fuerzas de los oxiácidos también aumentan a medida que aumenta la electronegatividad del elemento central [H 2 SeO 4 < H 2 SO 4].
Ecuaciones Clave
- \(K_\ce{a}=\ce{\dfrac{[H3O+][A- ]}{[HA]}}\)
- \(K_\ce{b}=\ce{\dfrac{[HB+][OH- ]}{[B]}}\)
- \(K_a \times K_b = 1.0 \times 10^{−14} = K_w \,(\text{at room temperature})\)
- \(\textrm{Percent ionization}=\ce{\dfrac{[H3O+]_{eq}}{[HA]_0}}×100\)
Glosario
- constante de ionización ácida (K a)
- constante de equilibrio para la ionización de un ácido débil
- constante de ionización de base (K b)
- constante de equilibrio para la ionización de una base débil
- efecto nivelador del agua
- cualquier ácido más fuerte que\(\ce{H3O+}\), o cualquier base más fuerte que OH − reaccionará con agua para formar\(\ce{H3O+}\), u OH −, respectivamente; el agua actúa como base para hacer que todos los ácidos fuertes parezcan igualmente fuertes, y actúa como un ácido para hacer que todas las bases fuertes parezcan igualmente fuertes
- oxiácido
- compuesto que contiene un no metal y uno o más grupos hidroxilo
- porcentaje de ionización
- relación de la concentración del ácido ionizado a la concentración inicial de ácido, multiplicado por 100


