19.1: Propiedades de los Metales de Transición y sus Compuestos
- Page ID
- 75644
- Esbozar el enfoque general para el aislamiento de metales de transición de fuentes naturales
- Describir las propiedades físicas y químicas típicas de los metales de transición
- Identificar clases de compuestos simples para metales de transición y describir sus propiedades químicas
Tenemos contacto diario con muchos metales de transición. El hierro ocurre en todas partes, desde los anillos de tu cuaderno de espiral y los cubiertos de tu cocina hasta automóviles, barcos, edificios y en la hemoglobina en tu sangre. El titanio es útil en la fabricación de productos livianos y duraderos como cuadros de bicicletas, caderas artificiales y joyas. El cromo es útil como revestimiento protector en accesorios de plomería y detalles automotrices.
Los metales de transición se definen como aquellos elementos que tienen (o forman fácilmente) orbitales d parcialmente llenos. Como se muestra en la Figura\(\PageIndex{2}\), los elementos d -bloque en los grupos 3—11 son elementos de transición. Los elementos del bloque f, también llamados metales de transición internos (los lantánidos y actínidos), también cumplen con este criterio porque el orbital d está parcialmente ocupado antes de los orbitales f. Los orbitales d se llenan con la familia del cobre (grupo 11); por esta razón, la siguiente familia (grupo 12) técnicamente no son elementos de transición. Sin embargo, los elementos del grupo 12 muestran algunas de las mismas propiedades químicas y son comúnmente incluidos en discusiones sobre metales de transición. Algunos químicos sí tratan a los elementos del grupo 12 como metales de transición.

Los elementos del bloque d se dividen en la primera serie de transición (los elementos Sc a Cu), la segunda serie de transición (los elementos Y a Ag) y la tercera serie de transición (el elemento La y los elementos Hf a Au). Actinium, Ac, es el primer miembro de la cuarta serie de transición, que también incluye Rf a Rg.
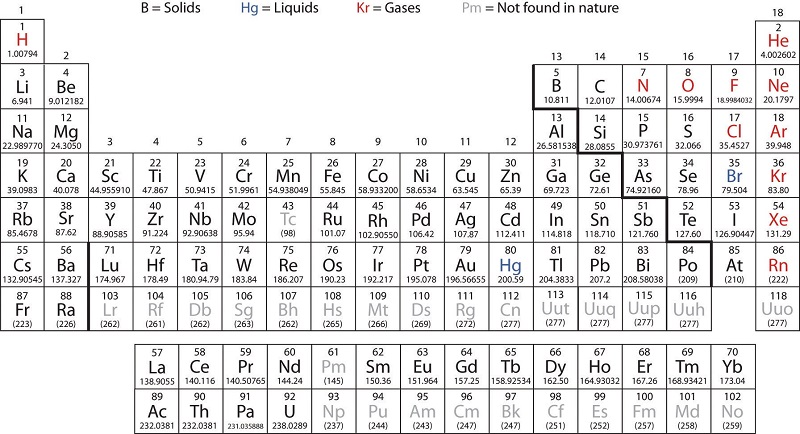
Los elementos del bloque f son los elementos Ce a Lu, que constituyen la serie lantánido (o serie lantanoide), y los elementos Th a Lr, que constituyen la serie de actínidos (o series actinoides). Debido a que el lantano se comporta muy parecido a los elementos lantánidos, se le considera un elemento lantánido, aunque su configuración electrónica lo convierte en el primer miembro de la tercera serie de transición. De igual manera, el comportamiento del actinio significa que es parte de la serie de actínidos, aunque su configuración electrónica lo convierte en el primer miembro de la cuarta serie de transición.
Revisar cómo escribir configuraciones electrónicas, abordadas en el capítulo sobre estructura electrónica y propiedades periódicas de los elementos. Recordemos que para los metales de transición y transición interna, es necesario eliminar los electrones s antes que los electrones d o f. Luego, para cada ion, dar la configuración electrónica:
- cerio (III)
- plomo (II)
- Ti 2 +
- Am 3 +
- Pd 2 +
Para los ejemplos que son metales de transición, determinar a qué series pertenecen.
Solución
Para los iones, los electrones de valencia s se pierden antes que los electrones d o f.
- Ce 3 + [Xe] 4 f 1; Ce 3 + es un elemento de transición interior en la serie de lantánidos.
- Pb 2 + [Xe] 6 s 2 5 d 10 4 f 14; los electrones se pierden del orbital p. Este es un elemento del grupo principal.
- titanio (II) [Ar] 3 d 2; primera serie de transición
- americio (III) [Rn] 5 f 6; actínido
- paladio (II) [Kr] 4 d 8; segunda serie de transición
Comprueba tu aprendizaje Da un ejemplo de un ion de la primera serie de transición sin d electrones.
- Responder
-
V 5+ es una posibilidad. Otros ejemplos incluyen Sc 3 +, Ti 4 +, Cr 6 + y Mn 7 +.
Los lantánidos (elementos 57—71) son bastante abundantes en la corteza terrestre, a pesar de su caracterización histórica como elementos de tierras raras. El tulio, el lantanoide natural más raro, es más común en la corteza terrestre que la plata (4.5 × 10 −5% versus 0.79 × 10 −5% en masa). Hay 17 elementos de tierras raras, que consisten en los 15 lantanoides más el escandio y el itrio. Se les llama raros porque alguna vez fueron difíciles de extraer económicamente, por lo que era raro tener una muestra pura; debido a propiedades químicas similares, es difícil separar cualquiera de los lantánidos de los demás. Sin embargo, los métodos de separación más nuevos, como las resinas de intercambio iónico similares a las que se encuentran en los ablandadores de agua domésticos, hacen que la separación de estos elementos sea más fácil y económica. La mayoría de los minerales que contienen estos elementos tienen bajas concentraciones de todos los elementos de tierras raras mezclados entre sí.
Las aplicaciones comerciales de los lantánidos están creciendo rápidamente. Por ejemplo, el europio es importante en las pantallas planas que se encuentran en monitores de computadora, teléfonos celulares y televisores. El neodimio es útil en discos duros portátiles y en los procesos que convierten el petróleo crudo en gasolina (Figura\(\PageIndex{3}\)). El holmio se encuentra en equipos dentales y médicos. Además, muchas tecnologías de energía alternativa dependen en gran medida de los lantanoides. El neodimio y el disprosio son componentes clave de los motores de vehículos híbridos y los imanes utilizados en las turbinas eólicas.

A medida que la demanda de materiales lantánidos ha aumentado más rápido que la oferta, los precios también han aumentado. En 2008, el disprosio costó $110/kg; para 2014, el precio había aumentado a $470/kg. Aumentar el suministro de elementos lantanoides es uno de los desafíos más significativos que enfrentan las industrias que dependen de las propiedades ópticas y magnéticas de estos materiales.
Los elementos de transición tienen muchas propiedades en común con otros metales. Casi todos son sólidos duros y de alto punto de fusión que conducen bien el calor y la electricidad. Ellos forman fácilmente aleaciones y pierden electrones para formar cationes estables. Además, los metales de transición forman una amplia variedad de compuestos de coordinación estables, en los que el átomo o ion metálico central actúa como un ácido de Lewis y acepta uno o más pares de electrones. Muchas moléculas e iones diferentes pueden donar pares solitarios al centro metálico, sirviendo como bases de Lewis. En este capítulo, nos centraremos principalmente en el comportamiento químico de los elementos de la primera serie de transición.
Propiedades de los Elementos de Transición
Los metales de transición demuestran una amplia gama de comportamientos químicos. Como se puede observar a partir de sus potenciales de reducción (Cuadro P1), algunos metales de transición son agentes reductores fuertes, mientras que otros tienen una reactividad muy baja. Por ejemplo, todos los lantánidos forman cationes acuosos estables 3+. La fuerza impulsora para tales oxidaciones es similar a la de los metales alcalinotérreos como Be o Mg, formando Be 2 + y Mg 2 +. Por otro lado, materiales como el platino y el oro tienen potenciales de reducción mucho mayores. Su capacidad para resistir la oxidación los convierte en materiales útiles para la construcción de circuitos y joyas.
Los iones de los elementos más ligeros del bloque d, como Cr 3 +, Fe 3 + y Co 2 +, forman iones hidratados coloridos que son estables en el agua. Sin embargo, los iones en el periodo justo por debajo de estos (Mo 3 +, Ru 3 + e Ir 2 +) son inestables y reaccionan fácilmente con el oxígeno del aire. La mayoría de los iones simples y estables al agua formados por los elementos más pesados del bloque d son oxianiones como\(\ce{MoO4^2-}\) y\(\ce{ReO4-}\).
El rutenio, el osmio, el rodio, el iridio, el paladio y el platino son los metales del platino. Con dificultad, forman cationes simples que son estables en el agua y, a diferencia de los elementos anteriores en la segunda y tercera serie de transición, no forman oxianiones estables.
Tanto los elementos del bloque d y f reaccionan con los no metales para formar compuestos binarios; a menudo se requiere calentamiento. Estos elementos reaccionan con halógenos para formar una variedad de haluros que varían en estado de oxidación de 1+ a 6+. Al calentar, el oxígeno reacciona con todos los elementos de transición excepto paladio, platino, plata y oro. Los óxidos de estos últimos metales se pueden formar usando otros reactivos, pero se descomponen al calentarse. Los elementos del bloque f, los elementos del grupo 3, y los elementos de la primera serie de transición excepto el cobre reaccionan con soluciones acuosas de ácidos, formando gas hidrógeno y soluciones de las sales correspondientes.
Los metales de transición pueden formar compuestos con una amplia gama de estados de oxidación. Algunos de los estados de oxidación observados de los elementos de la primera serie de transición se muestran en la Figura\(\PageIndex{4}\). A medida que nos movemos de izquierda a derecha a través de la primera serie de transición, vemos que el número de estados de oxidación comunes aumenta al principio hasta un máximo hacia el centro de la tabla, luego disminuye. Los valores en la tabla son valores típicos; hay otros valores conocidos, y es posible sintetizar nuevas adiciones. Por ejemplo, en 2014, los investigadores lograron sintetizar un nuevo estado de oxidación del iridio (9+).
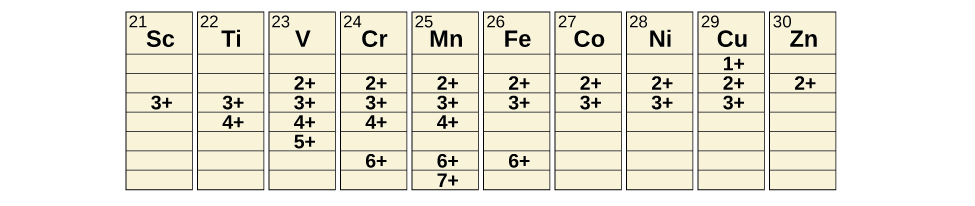
Para los elementos escandio a través del manganeso (la primera mitad de la primera serie de transición), el estado de oxidación más alto corresponde a la pérdida de todos los electrones tanto en los orbitales s como d de sus conchas de valencia. El ion titanio (IV), por ejemplo, se forma cuando el átomo de titanio pierde sus dos electrones de 3 d y dos de 4 s. Estos estados de oxidación más altos son las formas más estables de escandio, titanio y vanadio. Sin embargo, no es posible continuar eliminando todos los electrones de valencia de los metales a medida que continuamos a través de la serie. Se sabe que el hierro forma estados de oxidación de 2+ a 6+, siendo el hierro (II) y el hierro (III) los más comunes. La mayoría de los elementos de la primera serie de transición forman iones con una carga de 2+ o 3+ que son estables en el agua, aunque los de los primeros miembros de la serie pueden ser fácilmente oxidados por el aire.
Los elementos de la segunda y tercera serie de transición generalmente son más estables en estados de oxidación más altos que los elementos de la primera serie. En general, el radio atómico aumenta hacia abajo un grupo, lo que lleva a que los iones de la segunda y tercera serie sean mayores que los de la primera serie. Eliminar electrones de los orbitales que se encuentran más lejos del núcleo es más fácil que eliminar electrones cercanos al núcleo. Por ejemplo, el molibdeno y el tungsteno, miembros del grupo 6, están limitados principalmente a un estado de oxidación de 6+ en solución acuosa. El cromo, el miembro más ligero del grupo, forma iones Cr 3 + estables en agua y, en ausencia de aire, iones Cr 2 + menos estables. El sulfuro con mayor estado de oxidación para el cromo es Cr 2 S 3, el cual contiene el ion Cr 3 +. El molibdeno y el tungsteno forman sulfuros en los que los metales presentan estados de oxidación de 4+ y 6+.
¿Cuál es el agente oxidante más fuerte en solución ácida: ion dicromato, que contiene cromo (VI), ion permanganato, que contiene manganeso (VII), o dióxido de titanio, que contiene titanio (IV)?
Solución
Primero, necesitamos buscar las medias reacciones de reducción (Cuadro P1) para cada óxido en el estado de oxidación especificado:
\[\ce{Cr2O7^2- + 14H+ + 6e- ⟶ 2Cr^3+ + 7H2O} \hspace{20px} \mathrm{+1.33\: V} \nonumber \]
\[\ce{MnO4- + 8H+ + 5e- ⟶ Mn^2+ + H2O} \hspace{20px} \mathrm{+1.51\: V} \nonumber \]
\[\ce{TiO2 + 4H+ + 2e- ⟶ Ti^2+ + 2H2O} \hspace{20px} \mathrm{−0.50\: V} \nonumber \]
Un mayor potencial de reducción significa que es más fácil reducir el reactivo. El permanganato, con el mayor potencial de reducción, es el oxidante más fuerte bajo estas condiciones. El dicromato es el siguiente, seguido del dióxido de titanio como el agente oxidante más débil (el más difícil de reducir) de este conjunto.
Predecir qué reacción (si la hay) ocurrirá entre HCl y Co (s), y entre HBr y Pt (s). Deberá utilizar los potenciales de reducción estándar de (Cuadro P1).
- Responder
-
\(\ce{Co}(s)+\ce{2HCl}⟶\ce{H2}+\ce{CoCl2}(aq)\); ninguna reacción porque Pt (s) no será oxidado por H +
Preparación de los Elementos de Transición
Las civilizaciones antiguas conocían el hierro, el cobre, la plata y el oro. Los períodos de tiempo en la historia humana conocidos como la Edad del Bronce y la Edad del Hierro marcan los avances en los que las sociedades aprendieron a aislar ciertos metales y utilizarlos para fabricar herramientas y bienes. Los minerales naturales de cobre, plata y oro pueden contener altas concentraciones de estos metales en forma elemental (Figura\(\PageIndex{5}\)). El hierro, por otro lado, se presenta en la tierra casi exclusivamente en formas oxidadas, como la roya (Fe 2 O 3). Los primeros implementos de hierro conocidos fueron hechos de meteoritos de hierro. Los artefactos de hierro sobrevivientes que datan de aproximadamente 4000 a 2500 aC son raros, pero todos los ejemplos conocidos contienen aleaciones específicas de hierro y níquel que ocurren solo en objetos extraterrestres, no en la tierra. Pasaron miles de años de avances tecnológicos antes de que las civilizaciones desarrollaran la fundición de hierro, la capacidad de extraer un elemento puro de sus minerales naturales y que las herramientas de hierro se volvieran comunes.

Generalmente, los elementos de transición se extraen de minerales que se encuentran en una variedad de minerales. Sin embargo, la facilidad de su recuperación varía ampliamente, dependiendo de la concentración del elemento en el mineral, la identidad de los demás elementos presentes y la dificultad de reducir el elemento al metal libre.
En general, no es difícil reducir los iones de los elementos del bloque d al elemento libre. El carbono es un agente reductor suficientemente fuerte en la mayoría de los casos. Sin embargo, al igual que los iones de los metales del grupo principal más activo, los iones de los elementos del bloque f deben aislarse por electrólisis o por reducción con un metal activo como el calcio.
Discutiremos los procesos utilizados para el aislamiento de hierro, cobre y plata, ya que estos tres procesos ilustran los principales medios para aislar la mayoría de los metales del bloque d. En general, cada uno de estos procesos implica tres etapas principales: tratamiento preliminar, fundición y refinación.
- Tratamiento preliminar. En general, existe un tratamiento inicial de los minerales para hacerlos adecuados para la extracción de los metales. Esto generalmente implica triturar o moler el mineral, concentrar los componentes que contienen metal y, a veces, tratar estas sustancias químicamente para convertirlas en compuestos que son más fáciles de reducir al metal.
- Fundicion. El siguiente paso es la extracción del metal en estado fundido, un proceso llamado fundición, que incluye la reducción del compuesto metálico al metal. Las impurezas se pueden eliminar mediante la adición de un compuesto que forma una escoria, una sustancia con un bajo punto de fusión que se puede separar fácilmente del metal fundido.
- Refinación. El paso final en la recuperación de un metal es refinar el metal. Los metales de bajo punto de ebullición como el zinc y el mercurio se pueden refinar por destilación. Cuando se funden sobre una mesa inclinada, los metales de bajo punto de fusión como el estaño fluyen lejos de las impurezas de mayor fusión La electrólisis es otro método común para refinar metales.
Aislamiento de Hierro
La aplicación temprana del hierro a la fabricación de herramientas y armas fue posible debido a la amplia distribución de los minerales de hierro y a la facilidad con que los compuestos de hierro en los minerales podían ser reducidos por el carbono. Durante mucho tiempo, el carbón fue la forma de carbono utilizada en el proceso de reducción. La producción y el uso del hierro se generalizaron mucho más alrededor de 1620, cuando se introdujo el coque como agente reductor. El coque es una forma de carbono que se forma calentando carbón en ausencia de aire para eliminar impurezas.
El primer paso en la metalurgia del hierro suele ser asar el mineral (calentar el mineral al aire) para eliminar el agua, descomponer los carbonatos en óxidos y convertir los sulfuros en óxidos. Luego, los óxidos se reducen en un alto horno de 80 a 100 pies de altura y aproximadamente 25 pies de diámetro (Figura\(\PageIndex{6}\)) en el que el mineral tostado, el coque y la piedra caliza (CaCo impuro 3) se introducen continuamente en la parte superior. El hierro fundido y la escoria se retiran en el fondo. Todo el stock en un horno puede pesar varios cientos de toneladas.

Cerca del fondo de un horno hay boquillas a través de las cuales se sopla aire precalentado al interior del horno. Tan pronto como entra el aire, el coque en la región de las boquillas se oxida a dióxido de carbono con la liberación de una gran cantidad de calor. El dióxido de carbono caliente pasa hacia arriba a través de la capa superpuesta de coque candente, donde se reduce a monóxido de carbono:
\[\ce{CO2}(g)+\ce{C}(s)⟶\ce{2CO}(g) \nonumber \]
El monóxido de carbono sirve como agente reductor en las regiones superiores del horno. Las reacciones individuales se indican en la Figura\(\PageIndex{6}\).
Los óxidos de hierro se reducen en la región superior del horno. En la región media, la piedra caliza (carbonato de calcio) se descompone y el óxido de calcio resultante se combina con sílice y silicatos en el mineral para formar escoria. La escoria es principalmente silicato de calcio y contiene la mayoría de los componentes comercialmente poco importantes del mineral:
\[\ce{CaO}(s)+\ce{SiO2}(s)⟶\ce{CaSiO3}(l) \nonumber \]
Justo debajo de la mitad del horno, la temperatura es lo suficientemente alta como para fundir tanto el hierro como la escoria. Se acumulan en capas en el fondo del horno; la escoria menos densa flota sobre el hierro y lo protege de la oxidación. Varias veces al día, la escoria y el hierro fundido son retirados del horno. El hierro se transfiere a máquinas de fundición o a una planta de fabricación de acero (Figura\(\PageIndex{7}\)).

Gran parte del hierro producido se refina y se convierte en acero. El acero está hecho de hierro eliminando impurezas y agregando sustancias como manganeso, cromo, níquel, tungsteno, molibdeno y vanadio para producir aleaciones con propiedades que hacen que el material sea adecuado para usos específicos. La mayoría de los aceros también contienen porcentajes pequeños pero definidos de carbono (0.04% — 2.5%). Sin embargo, una gran parte del carbono contenido en el hierro debe ser removido en la fabricación del acero; de lo contrario, el exceso de carbono haría que el hierro fuera quebradizo.
Aislamiento de Cobre
Los minerales más importantes del cobre contienen sulfuros de cobre (como covellita, CuS), aunque a veces se encuentran óxidos de cobre (como tenorita, CuO) e hidroxicarboxatos de cobre [como malaquita, Cu 2 (OH) 2 CO 3]. En la producción de cobre metálico, el mineral de sulfuro concentrado se tuesta para eliminar parte del azufre como dióxido de azufre. La mezcla restante, que consiste en Cu 2 S, FeS, FeO y SiO 2, se mezcla con piedra caliza, que sirve como fundente (un material que ayuda en la eliminación de impurezas), y se calienta. La escoria fundida se forma a medida que el hierro y la sílice se eliminan mediante reacciones ácido-base de Lewis:
\[\ce{CaCO3}(s)+\ce{SiO2}(s)⟶\ce{CaSiO3}(l)+\ce{CO2}(g) \nonumber \]
\[\ce{FeO}(s)+\ce{SiO2}(s)⟶\ce{FeSiO3}(l) \nonumber \]
En estas reacciones, el dióxido de silicio se comporta como un ácido de Lewis, que acepta un par de electrones de la base de Lewis (el ion óxido).
La reducción del Cu 2 S que queda después de la fundición se logra soplando aire a través del material fundido. El aire convierte parte del Cu 2 S en Cu 2 O. Tan pronto como se forma el óxido de cobre (I), se reduce por el sulfuro de cobre (I) restante a cobre metálico:
\[\ce{2Cu2S}(l)+\ce{3O2}(g)⟶\ce{2Cu2O}(l)+\ce{2SO2}(g) \nonumber \]
\[\ce{2Cu2O}(l)+\ce{Cu2S}(l)⟶\ce{6Cu}(l)+\ce{SO2}(g) \nonumber \]
El cobre obtenido de esta manera se llama cobre blister por su aspecto característico, que se debe a las ampollas de aire que contiene (Figura\(\PageIndex{8}\)). Este cobre impuro se funde en placas grandes, las cuales se utilizan como ánodos en el refinamiento electrolítico del metal (que se describe en el capítulo sobre electroquímica).

Aislamiento de Plata
La plata a veces se presenta en pepitas grandes (Figura\(\PageIndex{9}\)) pero con mayor frecuencia en venas y depósitos relacionados. En un momento, el paneo fue un método efectivo para aislar pepitas de plata y oro. Debido a su baja reactividad, estos metales, y algunos otros, se presentan en depósitos como pepitas. El descubrimiento del platino se debió a que exploradores españoles en Centroamérica confundieron pepitas de platino con plata. Cuando el metal no está en forma de pepitas, a menudo es útil emplear un proceso llamado hidrometalurgia para separar la plata de sus minerales.

La hidrología implica la separación de un metal de una mezcla convirtiéndolo primero en iones solubles y luego extrayéndolos y reduciéndolos para precipitar el metal puro. En presencia de aire, los cianuros de metales alcalinos forman fácilmente el ion dicianoargentato (I) soluble\(\ce{[Ag(CN)2]-}\), a partir de metal plata o compuestos que contienen plata como Ag 2 S y AgCl. Las ecuaciones representativas son:
\[\ce{4Ag}(s)+\ce{8CN-}(aq)+\ce{O2}(g)+\ce{2H2O}(l)⟶\ce{4[Ag(CN)2]-}(aq)+\ce{4OH-}(aq) \nonumber \]
\[\ce{2Ag2S}(s)+\ce{8CN-}(aq)+\ce{O2}(g)+\ce{2H2O}(l)⟶\ce{4[Ag(CN)2]-}(aq)+\ce{2S}(s)+\ce{4OH-}(aq) \nonumber \]
\[\ce{AgCl}(s)+\ce{2CN-}(aq)⟶\ce{[Ag(CN)2]-}(aq)+\ce{Cl-}(aq) \nonumber \]
La plata se precipita de la solución de cianuro mediante la adición de iones de zinc o hierro (II), que sirve como agente reductor:
\[\ce{2[Ag(CN)2]-}(aq)+\ce{Zn}(s)⟶\ce{2Ag}(s)+\ce{[Zn(CN)4]^2-}(aq) \nonumber \]
Uno de los pasos para refinar la plata consiste en convertir la plata en iones dicianoargenato (I):
\[\ce{4Ag}(s)+\ce{8CN-}(aq)+\ce{O2}(g)+\ce{2H2O}(l)⟶\ce{4[Ag(CN)2]-}(aq)+\ce{4OH-}(aq) \nonumber \]
Explicar por qué el oxígeno debe estar presente para llevar a cabo la reacción. ¿Por qué la reacción no ocurre como:
\[\ce{4Ag}(s)+\ce{8CN-}(aq)⟶\ce{4[Ag(CN)2]-}(aq)? \nonumber \]
Así lution
Las cargas, así como los átomos, deben equilibrarse en las reacciones. El átomo de plata está siendo oxidado desde el estado de oxidación 0 al estado 1+. Siempre que algo pierde electrones, algo también debe ganar electrones (reducirse) para equilibrar la ecuación. El oxígeno es un buen agente oxidante para estas reacciones porque puede ganar electrones para pasar del estado de oxidación 0 al estado 2 −.
Durante la refinación del hierro, el carbono debe estar presente en el alto horno. ¿Por qué es necesario el carbono para convertir el óxido de hierro en hierro?
- Responder
-
El carbono se convierte en CO, que es el agente reductor que acepta electrones para que el hierro (III) pueda reducirse a hierro (0).
Compuestos de metales de transición
La unión en los compuestos simples de los elementos de transición varía de iónica a covalente. En sus estados de oxidación inferiores, los elementos de transición forman compuestos iónicos; en sus estados de oxidación superiores, forman compuestos covalentes o iones poliatómicos. La variación en los estados de oxidación exhibidos por los elementos de transición da a estos compuestos una química de oxidación-reducción basada en metales. Sigue la química de varias clases de compuestos que contienen elementos de la serie de transición.
Halidos
Los haluros anhidros de cada uno de los elementos de transición se pueden preparar mediante la reacción directa del metal con halógenos. Por ejemplo:
\[\ce{2Fe}(s)+\ce{3Cl2}(g)⟶\ce{2FeCl3}(s) \nonumber \]
El calentamiento de un haluro metálico con metal adicional se puede usar para formar un haluro del metal con un estado de oxidación más bajo:
\[\ce{Fe}(s)+\ce{2FeCl3}(s)⟶\ce{3FeCl2}(s) \nonumber \]
La estequiometría del haluro metálico que resulta de la reacción del metal con un halógeno está determinada por las cantidades relativas de metal y halógeno y por la fuerza del halógeno como agente oxidante. Generalmente, el flúor forma metales que contienen flúor en sus estados de oxidación más altos. Los otros halógenos pueden no formar compuestos análogos.
En general, la preparación de soluciones acuosas estables de los haluros de los metales de la primera serie de transición es mediante la adición de un ácido hidrohalogenado a carbonatos, hidróxidos, óxidos u otros compuestos que contienen aniones básicos. Las reacciones de muestra son:
\[\ce{NiCO3}(s)+\ce{2HF}(aq)⟶\ce{NiF2}(aq)+\ce{H2O}(l)+\ce{CO2}(g) \nonumber \]
\[\ce{Co(OH)2}(s)+\ce{2HBr}(aq)⟶\ce{CoBr2}(aq)+\ce{2H2O}(l) \nonumber \]
La mayoría de los metales de la primera serie de transición también se disuelven en ácidos, formando una solución de la sal y el gas hidrógeno. Por ejemplo:
\[\ce{Cr}(s)+\ce{2HCl}(aq)⟶\ce{CrCl2}(aq)+\ce{H2}(g) \nonumber \]
La polaridad de los enlaces con los metales de transición varía en función no solo de las electronegatividades de los átomos involucrados sino también en el estado de oxidación del metal de transición. Recuerde que la polaridad de los enlaces es un espectro continuo con electrones que se comparten uniformemente (enlaces covalentes) en un extremo y los electrones se transfieren completamente (enlaces iónicos) en el otro. Ningún enlace es nunca 100% iónico, y el grado en que los electrones se distribuyen uniformemente determina muchas propiedades del compuesto. Los haluros de metales de transición con bajos índices de oxidación forman más enlaces iónicos. Por ejemplo, el cloruro de titanio (II) y el cloruro de titanio (III) (TiCl 2 y TiCl 3) tienen altos puntos de fusión que son característicos de los compuestos iónicos, pero el cloruro de titanio (IV) (TiCl 4) es un líquido volátil, consistente con tener enlaces covalentes titanio-cloro. Todos los haluros de los elementos del bloque d más pesados tienen características covalentes significativas.
El comportamiento covalente de los metales de transición con estados de oxidación más altos se ejemplifica por la reacción de los tetrahaluros metálicos con agua. Al igual que el tetracloruro de silicio covalente, tanto los tetrahaluros de titanio como de vanadio reaccionan con agua para dar soluciones que contienen los correspondientes ácidos hidrohalogenados y los óxidos metálicos:
\[\ce{SiCl4}(l)+\ce{2H2O}(l)⟶\ce{SiO2}(s)+\ce{4HCl}(aq) \nonumber \]
\[\ce{TiCl4}(l)+\ce{2H2O}(l)⟶\ce{TiO2}(s)+\ce{4HCl}(aq) \nonumber \]
Óxidos
Al igual que con los haluros, la naturaleza de la unión en los óxidos de los elementos de transición está determinada por el estado de oxidación del metal. Los óxidos con estados de oxidación bajos tienden a ser más iónicos, mientras que aquellos con estados de oxidación más altos son más covalentes. Estas variaciones en la unión se deben a que las electronegatividades de los elementos no son valores fijos. La electronegatividad de un elemento aumenta con el aumento del estado de oxidación. Los metales de transición en estados de baja oxidación tienen valores de electronegatividad más bajos que el oxígeno; por lo tanto, estos óxidos metálicos son iónicos. Los metales de transición en estados de oxidación muy altos tienen valores de electronegatividad cercanos a los del oxígeno, lo que lleva a que estos óxidos sean covalentes.
Los óxidos de la primera serie de transición se pueden preparar calentando los metales en el aire. Estos óxidos son Sc 2 O 3, TiO 2, V 2 O 5, Cr 2 O 3, Mn 3 O 4, Fe 3 O 4, Co 3 O 4, NiO y CuO.
Alternativamente, estos óxidos y otros óxidos (con los metales en diferentes estados de oxidación) se pueden producir calentando los correspondientes hidróxidos, carbonatos u oxalatos en una atmósfera inerte. El óxido de hierro (II) se puede preparar calentando oxalato de hierro (II), y el óxido de cobalto (II) se produce calentando hidróxido de cobalto (II):
\[\ce{FeC2O4}(s)⟶\ce{FeO}(s)+\ce{CO}(g)+\ce{CO2}(g) \nonumber \]
\[\ce{Co(OH)2}(s)⟶\ce{CoO}(s)+\ce{H2O}(g) \nonumber \]
A excepción de CrO 3 y Mn 2 O 7, los óxidos de metales de transición no son solubles en agua. Pueden reaccionar con ácidos y, en algunos casos, con bases. En general, los óxidos de metales de transición con los estados de oxidación más bajos son básicos (y reaccionan con ácidos), los intermedios son anfóteros y los estados de oxidación más altos son principalmente ácidos. Los óxidos metálicos básicos en un estado de oxidación bajo reaccionan con ácidos acuosos para formar soluciones de sales y agua. Los ejemplos incluyen la reacción de protones aceptores de óxido de cobalto (II) del ácido nítrico, y protones aceptores de óxido de escandio (III) del ácido clorhídrico:
\[\ce{CoO}(s)+\ce{2HNO3}(aq)⟶\ce{Co(NO3)2}(aq)+\ce{H2O}(l) \nonumber \]
\[\ce{Sc2O3}(s)+\ce{6HCl}(aq)⟶\ce{2ScCl3}(aq)+\ce{3H2O}(l) \nonumber \]
Los óxidos de metales con estados de oxidación de 4+ son anfóteros, y la mayoría no son solubles ni en ácidos ni en bases. El óxido de vanadio (V), el óxido de cromo (VI) y el óxido de manganeso (VII) son ácidos. Reaccionan con soluciones de hidróxidos para formar sales de los oxianiones\(\ce{VO4^3-}\),\(\ce{CrO4^2-}\), y\(\ce{MnO4-}\). Por ejemplo, la ecuación iónica completa para la reacción del óxido de cromo (VI) con una base fuerte viene dada por:
\[\ce{CrO3}(s)+\ce{2Na+}(aq)+\ce{2OH-}(aq)⟶\ce{2Na+}(aq)+\ce{CrO4^2-}(aq)+\ce{H2O}(l) \nonumber \]
El óxido de cromo (VI) y el óxido de manganeso (VII) reaccionan con el agua para formar los ácidos H 2 CrO 4 y HMnO 4, respectivamente.
Hidróxidos
Cuando se agrega un hidróxido soluble a una solución acuosa de una sal de un metal de transición de la primera serie de transición, se forma un precipitado gelatinoso. Por ejemplo, agregar una solución de hidróxido de sodio a una solución de sulfato de cobalto produce un precipitado gelatinoso rosado o azul de hidróxido de cobalto (II). La ecuación iónica neta es:
\[\ce{Co^2+}(aq)+\ce{2OH-}(aq)⟶\ce{Co(OH)2}(s) \nonumber \]
En este y muchos otros casos, estos precipitados son hidróxidos que contienen el ion de metal de transición, iones hidróxido y agua coordinados con el metal de transición. En otros casos, los precipitados son óxidos hidratados compuestos por el ión metálico, iones óxido y agua de hidratación:
\[\ce{4Fe^3+}(aq)+\ce{6OH-}(aq)+\ce{nH2O}(l)⟶\ce{2Fe2O3⋅(n + 3)H2O}(s) \nonumber \]
Estas sustancias no contienen iones hidróxido. Sin embargo, tanto los hidróxidos como los óxidos hidratados reaccionan con ácidos para formar sales y agua. Al precipitar un metal de la solución, es necesario evitar un exceso de ion hidróxido, ya que esto puede conducir a la formación de iones complejos como se discutirá más adelante en este capítulo. Los hidróxidos metálicos precipitados se pueden separar para su posterior procesamiento o para la eliminación de desechos.
Carbonatos
Muchos de los elementos de la primera serie de transición forman carbonatos insolubles. Es posible preparar estos carbonatos mediante la adición de una sal de carbonato soluble a una solución de una sal de metal de transición. Por ejemplo, el carbonato de níquel se puede preparar a partir de soluciones de nitrato de níquel y carbonato de sodio de acuerdo con la siguiente ecuación iónica neta:
\[\ce{Ni^2+}(aq)+\ce{CO3^2-}⟶\ce{NiCO3}(s) \nonumber \]
Las reacciones de los carbonatos de metales de transición son similares a las de los carbonatos metálicos activos. Reaccionan con ácidos para formar sales de metales, dióxido de carbono y agua. Al calentarse, se descomponen, formando los óxidos de metales de transición.
Otras Sales
En muchos aspectos, el comportamiento químico de los elementos de la primera serie de transición es muy similar al del grupo principal de metales. En particular, se pueden utilizar los mismos tipos de reacciones que se utilizan para preparar sales del grupo principal metales para preparar sales iónicas simples de estos elementos.
Se pueden preparar diversas sales a partir de metales que son más activos que el hidrógeno por reacción con los ácidos correspondientes: El metal escandio reacciona con ácido bromhídrico para formar una solución de bromuro de escandio:
\[\ce{2Sc}(s)+\ce{6HBr}(aq)⟶\ce{2ScBr3}(aq)+\ce{3H2}(g) \nonumber \]
Los compuestos comunes que acabamos de discutir también pueden ser utilizados para preparar sales. Las reacciones involucradas incluyen las reacciones de óxidos, hidróxidos o carbonatos con ácidos. Por ejemplo:
\[\ce{Ni(OH)2}(s)+\ce{2H3O+}(aq)+\ce{2ClO4-}(aq)⟶\ce{Ni^2+}(aq)+\ce{2ClO4-}(aq)+\ce{4H2O}(l) \nonumber \]
Se pueden usar reacciones de sustitución que implican sales solubles para preparar sales insolubles. Por ejemplo:
\[\ce{Ba^2+}(aq)+\ce{2Cl-}(aq)+\ce{2K+}(aq)+\ce{CrO4^2-}(aq)⟶\ce{BaCrO4}(s)+\ce{2K+}(aq)+\ce{2Cl-}(aq) \nonumber \]
En nuestra discusión sobre los óxidos en esta sección, hemos visto que las reacciones de los óxidos covalentes de los elementos de transición con hidróxidos forman sales que contienen oxianiones de los elementos de transición.
Superconductores de Alta Temperatura
Un superconductor es una sustancia que conduce electricidad sin resistencia. Esta falta de resistencia hace que no haya pérdida de energía durante la transmisión de la electricidad. Esto conduciría a una reducción significativa en el costo de la electricidad.
Los materiales superconductores comerciales más utilizados actualmente, como NbTi y Nb 3 Sn, no se vuelven superconductores hasta que se enfrían por debajo de 23 K (−250 °C). Esto requiere el uso de helio líquido, que tiene una temperatura de ebullición de 4 K y es caro y difícil de manejar. El costo del helio líquido ha disuadido la aplicación generalizada de superconductores.
Uno de los descubrimientos científicos más emocionantes de la década de 1980 fue la caracterización de compuestos que exhiben superconductividad a temperaturas superiores a 90 K. (Comparado con el helio líquido, 90 K es una temperatura alta). Entre los materiales superconductores de alta temperatura son los óxidos que contienen itrio (o uno de varios elementos de tierras raras), bario y cobre en una proporción 1:2:3. La fórmula del compuesto iónico de itrio es YbA 2 Cu 3 O 7.
Los nuevos materiales se vuelven superconductores a temperaturas cercanas a los 90 K (Figura\(\PageIndex{10}\)), temperaturas que se pueden alcanzar enfriando con nitrógeno líquido (temperatura de ebullición de 77 K). No solo los materiales refrigerados con nitrógeno líquido son más fáciles de manejar, sino que los costos de enfriamiento también son aproximadamente 1000 veces más bajos que para el helio líquido.
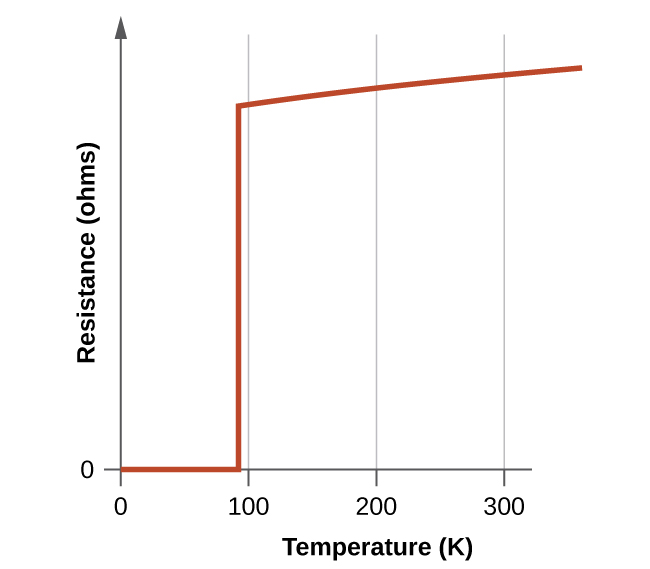
Aunque la naturaleza frágil y frágil de estos materiales actualmente obstaculiza sus aplicaciones comerciales, tienen un tremendo potencial que los investigadores están trabajando duro para mejorar sus procesos para ayudar a realizar. Las líneas de transmisión superconductoras transportarían corriente por cientos de millas sin pérdida de energía debido a la resistencia en los cables. Esto podría permitir que las estaciones generadoras se ubicaran en zonas alejadas de los centros de población y cerca de los recursos naturales necesarios para la producción de energía. El primer proyecto que demuestra la viabilidad de la transmisión de energía superconductora de alta temperatura se estableció en Nueva York en 2008.

Los investigadores también están trabajando en el uso de esta tecnología para desarrollar otras aplicaciones, como microchips más pequeños y potentes. Además, los superconductores de alta temperatura se pueden utilizar para generar campos magnéticos para aplicaciones como dispositivos médicos, trenes de levitación magnética y campos de contención para reactores de fusión nuclear (Figura\(\PageIndex{11}\)).
Resumen
Los metales de transición son elementos con orbitales d parcialmente llenos, ubicados en el bloque d de la tabla periódica. La reactividad de los elementos de transición varía ampliamente desde metales muy activos como el escandio y el hierro hasta elementos casi inertes, como los metales platino. El tipo de química utilizada en el aislamiento de los elementos de sus minerales depende de la concentración del elemento en su mineral y de la dificultad de reducir los iones de los elementos a los metales. Los metales que son más activos son más difíciles de reducir.
Los metales de transición presentan un comportamiento químico típico de los metales. Por ejemplo, se oxidan al aire al calentarse y reaccionan con halógenos elementales para formar haluros. Aquellos elementos que se encuentran por encima del hidrógeno en la serie de actividades reaccionan con ácidos, produciendo sales e hidrógeno gaseoso. Los óxidos, hidróxidos y carbonatos de compuestos de metales de transición en estados de baja oxidación son básicos. Los haluros y otras sales son generalmente estables en el agua, aunque en algunos casos se debe excluir el oxígeno. La mayoría de los metales de transición forman una variedad de estados de oxidación estables, lo que les permite demostrar una amplia gama de reactividad química.
Glosario
- serie de actínidos
- (también, serie actinoide) actinio y los elementos en la segunda fila o el bloque f, números atómicos 89—103
- compuesto de coordinación
- compuesto estable en el que el átomo o ion metálico central actúa como un ácido de Lewis y acepta uno o más pares de electrones
- d -bloque elemento
- uno de los elementos en los grupos 3—11 con electrones de valencia en d orbitales
- f -elemento de bloque
- (también, elemento de transición interior) uno de los elementos con números atómicos 58—71 o 90—103 que tienen electrones de valencia en f orbitales; frecuentemente se muestran desfasados debajo de la tabla periódica
- primera serie de transición
- elementos de transición en el cuarto período de la tabla periódica (primera fila del bloque d), números atómicos 21—29
- cuarta serie de transición
- elementos de transición en el séptimo período de la tabla periódica (cuarta fila del bloque d), números atómicos 89 y 104—111
- hidrometalurgia
- proceso en el que un metal se separa de una mezcla convirtiéndolo primero en iones solubles, extrayendo los iones y luego reduciendo los iones para precipitar el metal puro
- serie lantánido
- (también, serie lantanoide) lantano y los elementos en la primera fila o el bloque f, números atómicos 57—71
- metales de platino
- grupo de seis metales de transición consistentes en rutenio, osmio, rodio, iridio, paladio y platino que tienden a aparecer en los mismos minerales y demuestran propiedades químicas similares
- elemento de tierras raras
- colección de 17 elementos incluyendo lantánidos, escandio e itrio que a menudo ocurren juntos y tienen propiedades químicas similares, dificultando la separación
- segunda serie de transición
- elementos de transición en el quinto período de la tabla periódica (segunda fila del bloque d), números atómicos 39—47
- fundición
- proceso de extracción de un metal puro de un mineral fundido
- acero
- material hecho de hierro mediante la eliminación de impurezas en el hierro y la adición de sustancias que producen aleaciones con propiedades adecuadas para usos específicos
- superconductor
- material que conduce la electricidad sin resistencia
- tercera serie de transición
- elementos de transición en el sexto periodo de la tabla periódica (tercera fila del bloque d), números atómicos 57 y 72—79


