4.18: Soluciones a Problemas Seleccionados
( \newcommand{\kernel}{\mathrm{null}\,}\)
Ejercicio 4.2.1:
a) 10 ppm b) 64 ppm c) 158 ppm
Ejercicio 4.2.2:
a) 63 ppm b) 201 ppm c) 71 ppm
Ejercicio 4.3.1:
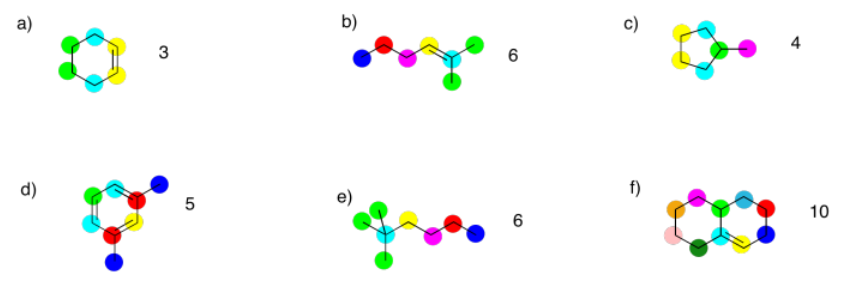
Ejercicio 4.3.2:
- pentano, CH 3 CH 2 CH 2 CH 2 CH 3, o hexano, CH 3 CH 2 CH 2 CH 2 CH 2 CH 2 CH 3
- heptano, CH 3 CH 2 CH 2 CH 2 CH 2 CH 3, u octano, CH 3 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 3
- nonano, CH 3 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 3, o decano, CH 3 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 2 CH 3
Ejercicio 4.4.1:
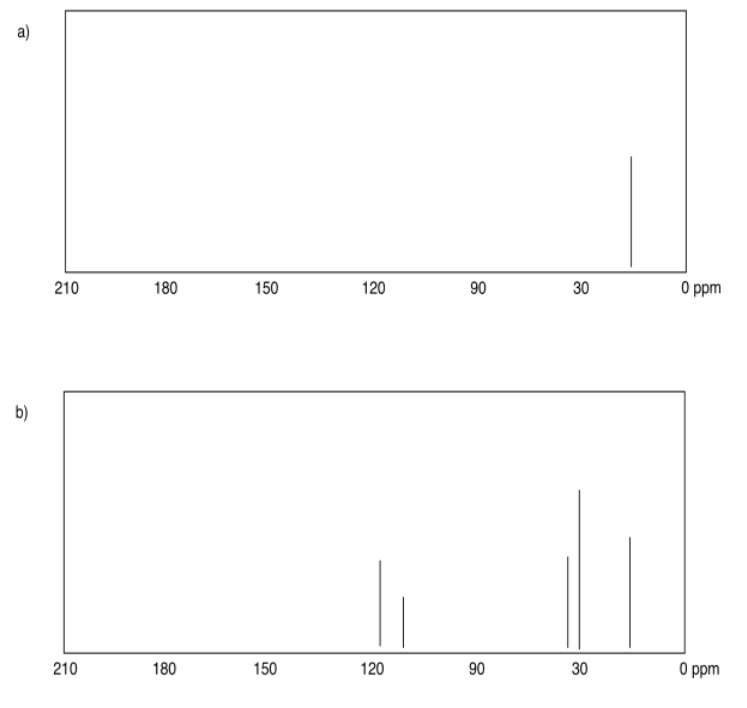
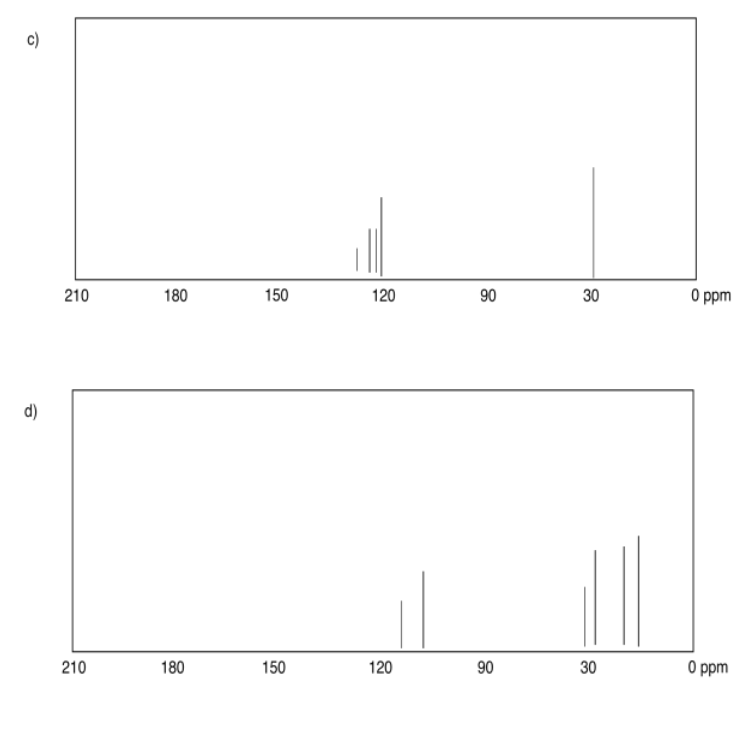
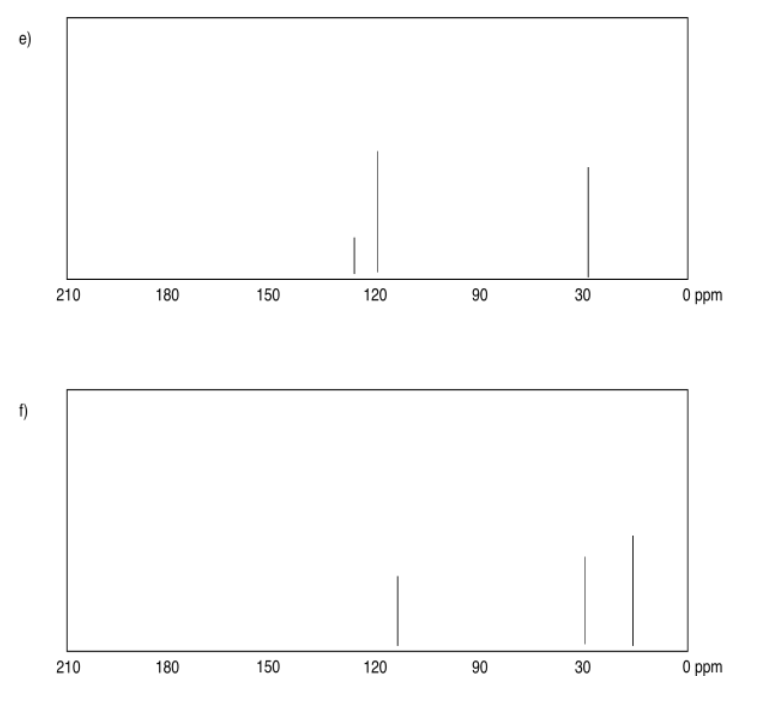
Ejercicio 4.4.2:
a) sp 3 b) sp 2 c) sp 2 d) sp 3 e) sp 3 f) sp 2
Ejercicio 4.5.1:
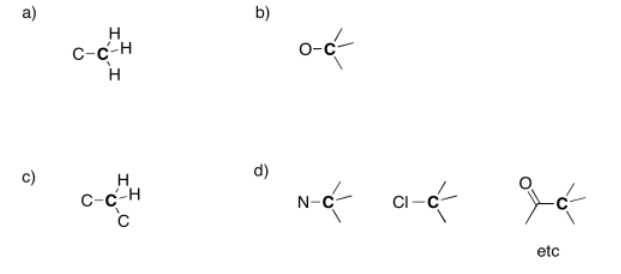
Ejercicio 4.5.2:
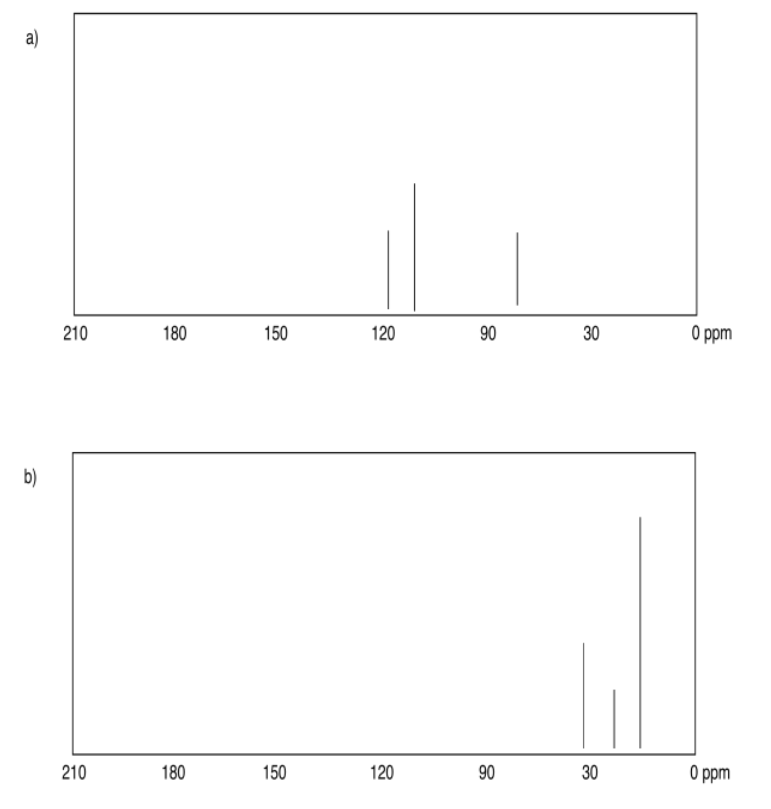
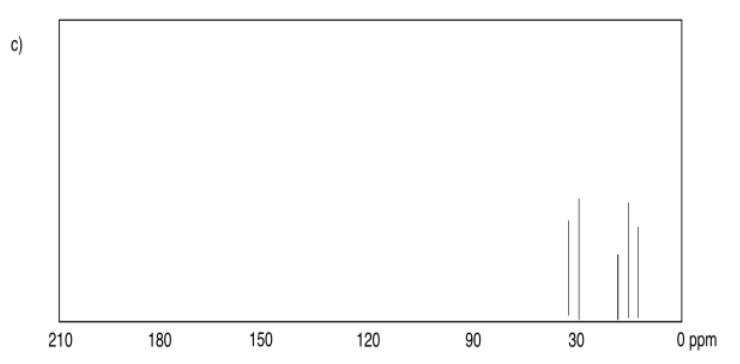
Ejercicio 4.6.1:
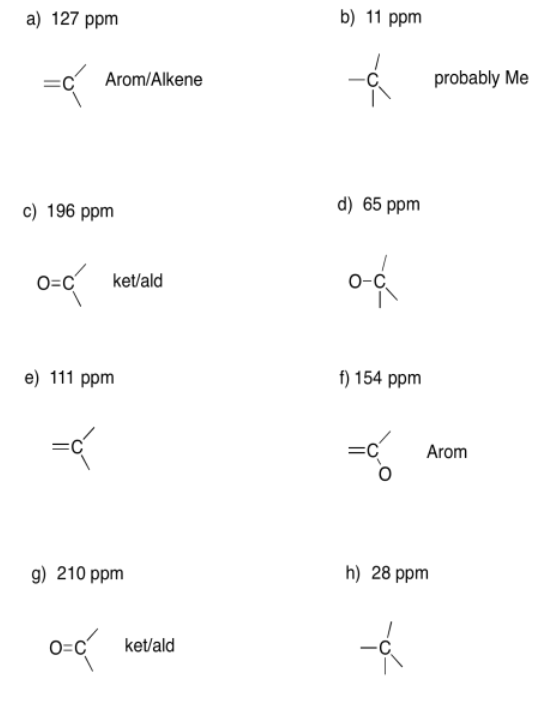

Ejercicio 4.6.2:
a)
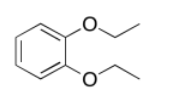
b)
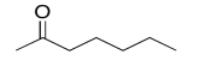
c)
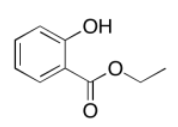
Ejercicio 4.8.1:
a) H-C sp 3 b) H-C sp 3 c) H-C sp 2 d) H-C sp 3 e) H-C sp 2 f) H-C sp 2 g) H-C sp 3
Ejercicio 4.8.2:
a) carbono b) carbono c) nitrógeno d) oxígeno e) carbono f) oxígeno g) nitrógeno
Ejercicio 4.8.3:
a) aromático b) aromático c) alqueno d) alqueno e) alqueno f) aromático
Ejercicio 4.8.4:
a) H-C Ar -C b) H-C Ar -C c) H-C Ar -N d) C=O e) C=O f) H-C Ar -N g) H-C Ar -N
Ejercicio 4.8.5:
- 3.4 ppm: H a 1.5 ppm: H b, H c 0.9 ppm: H d
- 7.4 ppm: H d 6.9 ppm: H b, H c 3.7 ppm: H a
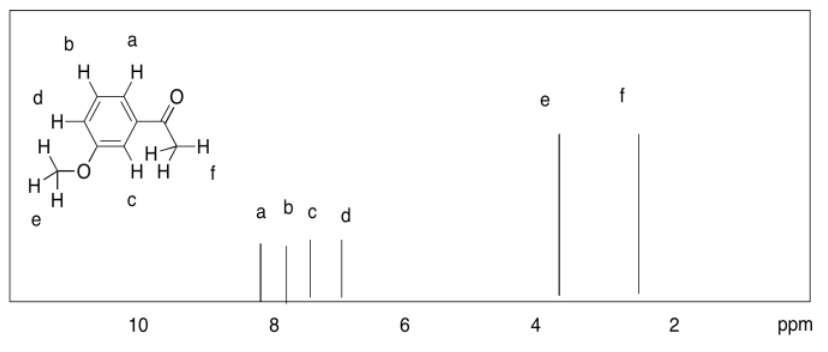
- 10.1 ppm: H a 7.9 ppm: H b 7.6 ppm: H d 7.5 ppm: H c
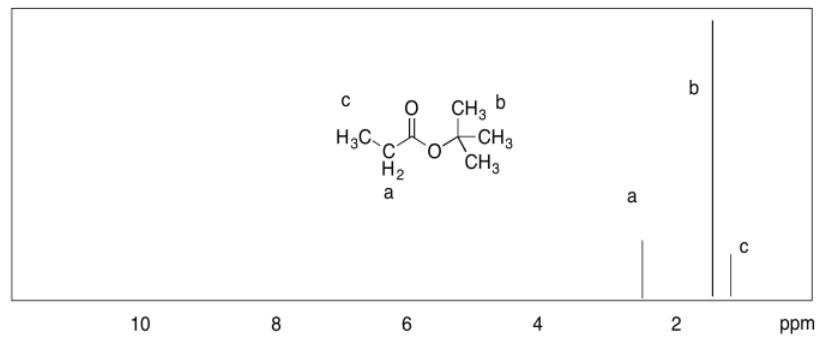
- 7.9 ppm: H b 7.6 ppm: H d 7.4 ppm: H c 2.5 ppm: H a
Ejercicio 4.8.6:
a)
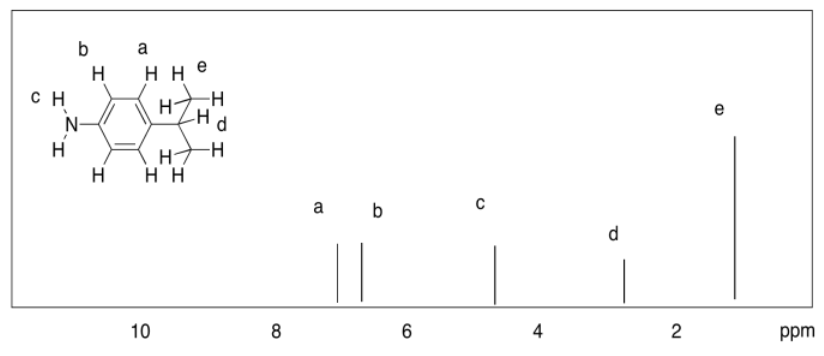
b)
c)
d)
Ejercicio 4.9.1:
- 0.9 ppm, 6H; 1.0 ppm, 6H (relación 1:1)
- 0.9 ppm, 6H; 1.0 ppm, 12H (relación 1:2)
- 0.9 ppm, 6H; 1.0 ppm, 16H (relación 3:8)
- 0.9 ppm, 6H; 1.0 ppm, 10H (relación 3:5)
- 0.9 ppm, 6H; 1.0 ppm, 8H (relación 3:4)
Ejercicio 4.9.2:
a)
b)
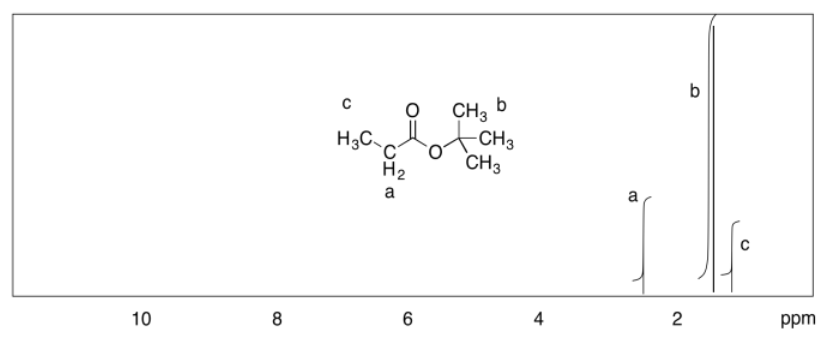
c)
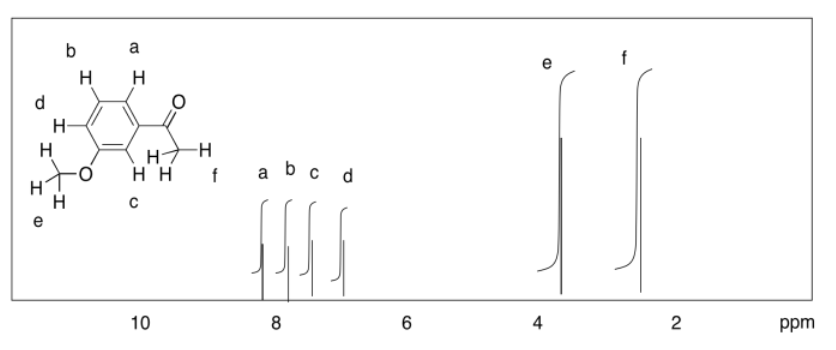
d)
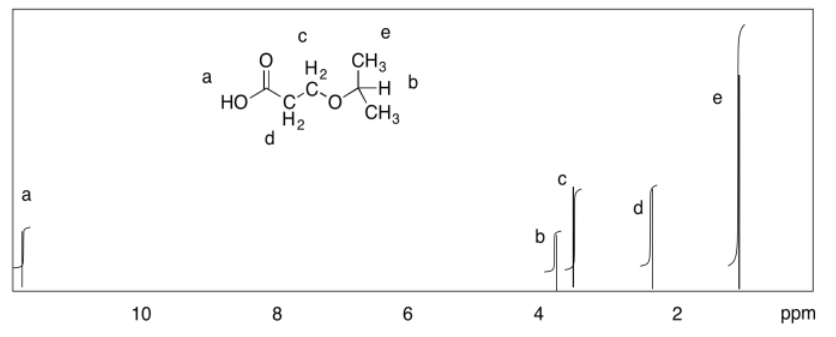
Ejercicio 4.9.3:
a) 5:2:3
Exericse 4.10.1:
(Habrá alguna variación en el turno dependiendo del resto de la estructura; esto es solo una estimación).
a) 3.5 ppm, cuarteto, 2H b) 1.5 ppm, sexteto, 2H c) 2.6 ppm, septeto, 1H
d) 2.3 ppm, quinteto, 1H e) 2.2 ppm, cuarteto, 2H f) 1.7 ppm, nonet, 1H
Ejercicio 4.10.2:
(Habrá alguna variación en el turno dependiendo del resto de la estructura; esto es solo una estimación).
a) 7.8 ppm, doblete, 1H b) 8.4 ppm, singlete, 1H c) 6.7 ppm, singlete, 1H
d) 7.2 ppm, troplete, 1H e) 6.9 ppm, doblete, 1H
Ejercicio 4.10.3:
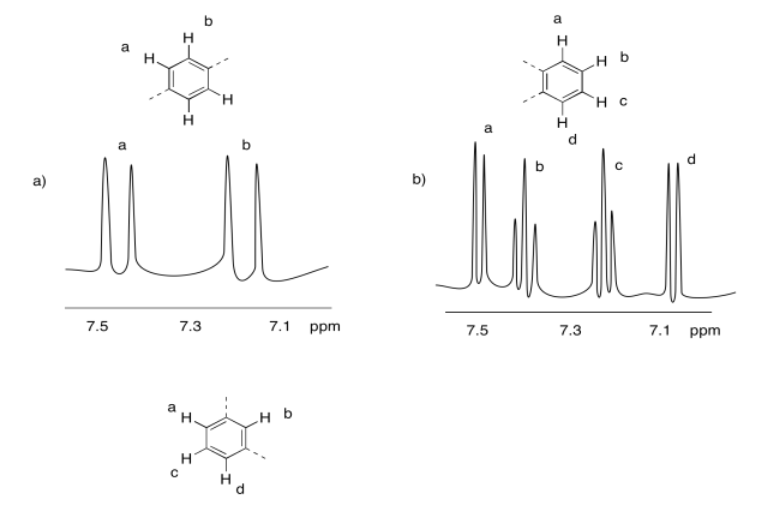
Ejercicio 4.10.4:
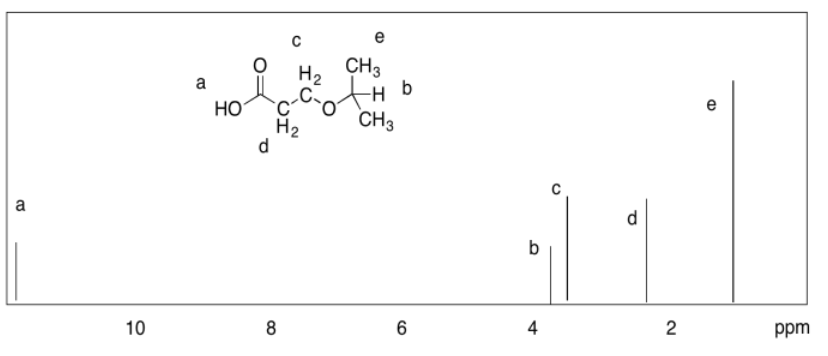
3.4 ppm, doblete: CH-C H 2 -O
2.1 ppm, singlete: O H
1.7 ppm, nonet: (CH 3) 2 C H CH 2
0.9 ppm, doblete: CH (C H 3) 2
Ejercicio 4.10.5:
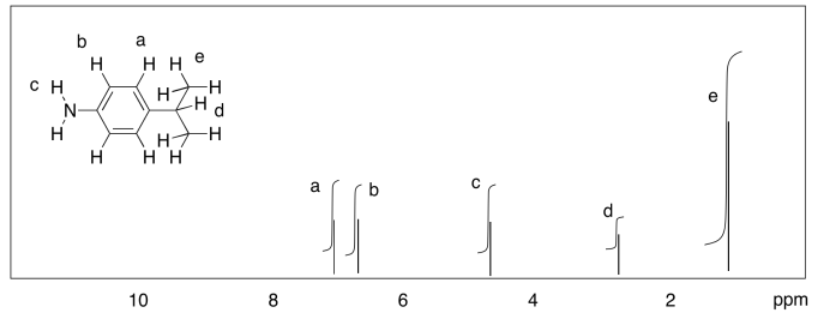
a) Se trata de un espectro simulado. Los picos en f, e y c son singletes. El pico a d es un doblete. Los picos en a & b son desafortunadamente coincidentes, por lo que sus multiplicidades están oscurecidas, pero serían dobletes y trillizos, respectivamente.
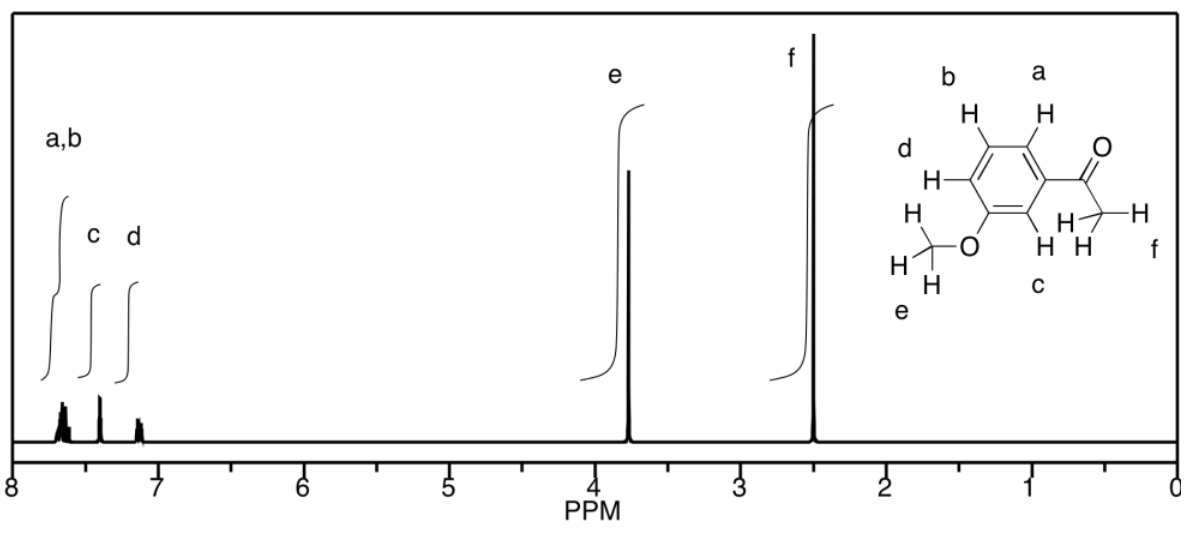
b)
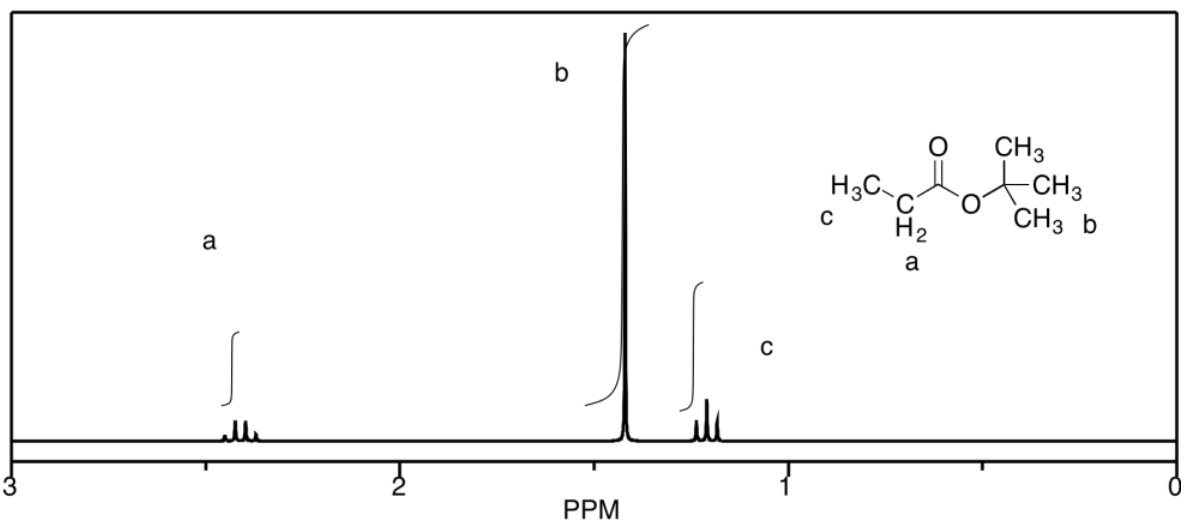
c)
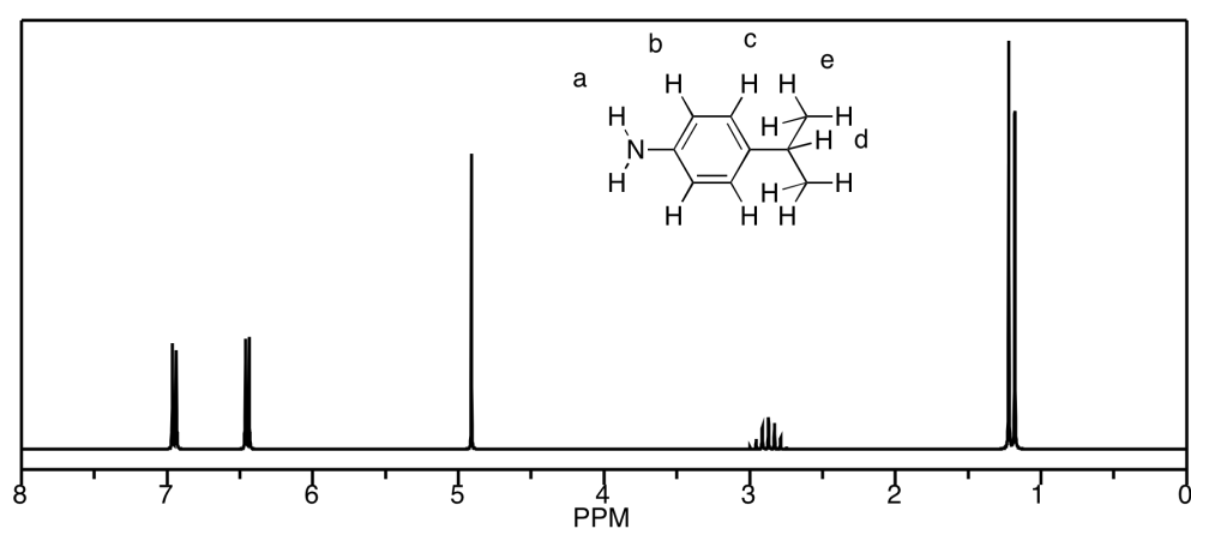
d) Los picos en b y c lamentablemente coinciden, pero serían un septeto y un triplete, respectivamente. De lo contrario, a es un singlete, d es un triplete y e es un doblete.
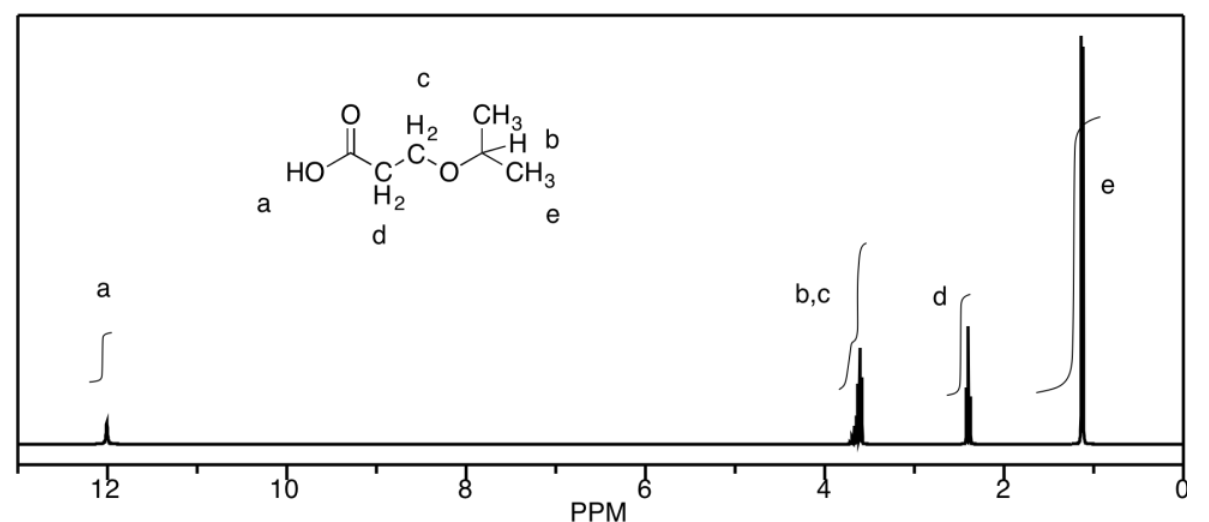
Ejercicio 4.12.1:
Rellenar estructuras parciales para los siguientes picos.
Los picos aromáticos (benceno, etc.) se marcan como “Ar” para distinguirlos de los picos de alqueno que aparecen más arriba (desplazamiento inferior). Además, algunos picos pueden estar en dos posiciones simétricas y están etiquetados con “x2".
a) 10.1 ppm, 1H, triplete, CH 2 -C H =O b) 3.4 ppm, 1H, septeto, O-C H (CH 3) 2
c) 7.3 ppm, 2H, triplete, CH=C H -CH x 2 (Ar) d) 5.4 ppm, 1H, cuarteto, CH 3 -C H =C
e) 1.4 ppm, 2H, sexteto, CH 3 -C H 2 -CH 2 f) 8.0 ppm, 1H, singlete, C=C H-C (Ar)
g) 2.1 ppm, 3H, singlete, C H 3 -C=C o C H 3 -C=O o C H 3 -N; necesita contexto para elegir
h) 6.8 ppm, 2H, doblete, CH=C H -C x 2 (Ar) i) 0.9 ppm, 6H, doblete, CH-C H 3 x 2
Ejercicio 4.12.2:
Identificar los errores en las siguientes estructuras parciales:
a) 3.6 ppm, 2H, triplete, C H 2 -CH 2 el primer carbono debe estar unido a O para tener un desplazamiento a 3.6 ppm
b) 2.1 ppm, 2H, singlete, C H 3 -C=C la integral dice solo 2H, no 3H
c) 7.4 ppm, 2H, doblete, CH=C H 2 -C el desplazamiento implica aromático, por lo que solo puede haber un H por carbono; debe haber simetría
d) 1.8 ppm, 2H, quinteto, C H 2 -CH 4 no puede haber cuatro hidrógenos en un carbono; debe haber algunos hidrógenos en cada lado
e) 7.8 ppm, 1H, triplete, -C H =CH 2 el desplazamiento implica aromático, por lo que solo puede haber un H por carbono; debe ser uno por cada lado
f) 1.7 ppm, 1H, nonet, NH 2-C H (CH 3) 2 un nitrógeno unido desplazaría este hidrógeno más allá de 2 ppm; además, el acoplamiento rara vez se ve a través de O o N, por lo que los dos H vecinos a la izquierda probablemente estén en un carbono
Ejercicio 4.13.1:
a) TBME b) acetona c) THF d) metanol e) acetato de etilo
Ejercicio 4.14.1:
- aparición de CH-O cerca de 3.5 ppm (multiplete, 1H)
- aparición de CH 2 -O cerca de 3.5 ppm (triplete, 2H); desaparición de =CH cerca de 5-6 ppm (mutipletes, 3H total)
- aparición de HC=O cerca de 10 ppm (triplete, 1H); desaparición de =CH cerca de 5-6 ppm (mutipletes, 3H total)
- aparición de HC=O cerca de 10 ppm (triplete, 1H); desaparición de CH 2-O cerca de 3.5 ppm (doblete, 2H)
- aparición de CH 2 -O cerca de 3.5 ppm (triplete, 2H)
- aparición de CH 2 -O cerca de 4 ppm (triplete, 2H)
- aparición de =CH cerca de 5-6 ppm (mutipletes, 2H total); desaparición de HC=O cerca de 10 ppm (triplete, 1H);
- desaparición de =CH cerca de 5-6 ppm (mutipletes, 2H total); aparición de patrón triplet:sextet:triplete entre 1-2 ppm
i) aparición de HC=O cerca de 10 ppm (triplete, 1H); desaparición de CH 2-O cerca de 3.5 ppm (doblete, 2H)
j) aparición de CH-O cerca de 3 ppm (singlete, 3H) y 3.5 ppm (sexteto, 1H); desaparición de =CH cerca de 5-6 ppm (mutipletes, 2H total)
Ejercicio 4.15.1:
a) Estudiante 1: Usemos el pico H 2 C-O de propanoato de etilo a 4 ppm y el acetonitrilo metilo a 2 ppm. La proporción parece ser 2:1, pero representan 2 protones y 3 protones, respectivamente. Eso significa que la relación de moléculas es 2/ 2:1 /3 = 3:1 de propanoato de etilo: acetonitrilo.
estudiante 2: Utilizaremos el pico H 2 C-O de propanoato de etilo a 4 ppm y el pico H 2 C-O de THF a 3.5 ppm. La proporción parece ser 3:2, pero representan 2 protones y 4 protones, respectivamente. Eso significa que la relación de moléculas es 3/ 2:2 /4 = 12:4 = 3:1 propanoato de etilo: THF.
estudiante 3: Observa el pico H 2 cCl 2 de diclorometano a 5 ppm y el pico H 2 C-O de THF a 4 ppm. La relación parece ser 1:2, y ambos representan 2 protones, por lo que la relación de moléculas es 1:2 de diclorometano:propanoato de etilo.
b) Estudiante 1: La muestra es\frac{1}{1 + 3} \times 100 \% = 25 \% acetonitrilo.
estudiante 2: La muestra es\frac{1}{1 + 3} \times 100 \% = 25 \% THF.
estudiante 3: La muestra es\frac{1}{1 + 2} \times 100 \% = 33 \% acetonitrilo.
Ejercicio 4.15.2:
Los mangos de RMN obvios son el protón de aldehído H-C=O a 10 ppm para el benzaldehído y el protón H-C-O adyacente al alcohol a 4.5 ppm para 1-fenilpropanol.
Cada uno de esos picos representa un protón, por lo que la relación integral de 1:2 sugiere una relación de bezaldehído a 1-fenilpropanol de 1:2. Eso se traduce en 33% benzaldehído, 67% 1-fenilpropanol.
Ejercicio 4.15.3:
Los mangos de RMN aquí son el protón de aldehído H-C=O a 10 ppm para el benzaldehído y los protones H 2 C-O adyacentes al alcohol cerca de 5 ppm para el alcohol bencílico.
En este caso, necesitamos corregir los diferentes números de protones representados por cada pico: 1H para el pico de aldehído pero 2H para el de alcohol. Por lo tanto, la relación integral de 1:6 sugiere una relación de bezaldehído a 1-fenilpropanol de 1:3. Eso se traduce en 25% benzaldehído, 75% 1-fenilpropanol.
Ejercicio 4.15.4:
Podríamos usar el pico correspondiente al protón O-CH-C=O por encima de 5 ppm para la unidad de repetición y el pico para el protón CH 2-O en el grupo iniciador/final cerca de 3.5 ppm. La relación integral es de 24:1, pero representan diferentes números de hidrógenos, por lo que la relación de unidad repetida a grupo final es realmente 24/ 1:1 /2, o 48:1. El grado de polimerización es 48.

