16.5: Otros grupos funcionales que contienen oxígeno
- Page ID
- 75012
- Identificar los grupos funcionales aldehído, cetona, ácido, éster y éter.
Existen otros grupos funcionales que contienen átomos de O. Antes de introducirlos, definimos el grupo carbonilo, que se forma cuando un átomo de O y un átomo de C están unidos por un doble enlace:
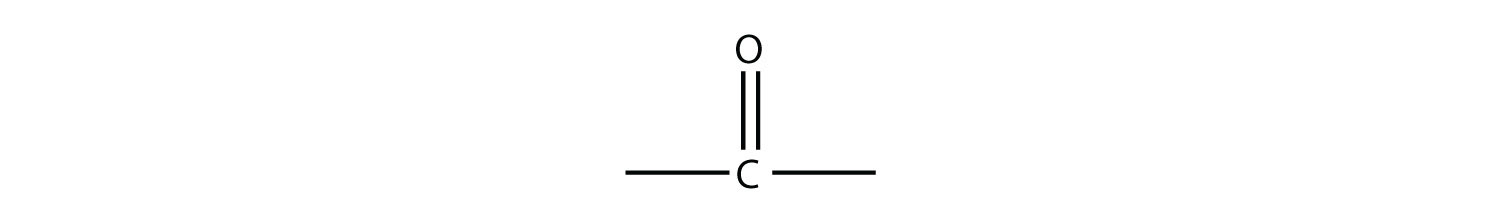
Los otros dos enlaces en el átomo de C están unidos a otros átomos. Son las identidades de estos otros átomos las que definen qué tipo específico de compuesto es una molécula orgánica.
Si se hace un enlace del grupo carbonilo a un átomo de H, entonces la molécula se clasifica como un aldehído (Si hay dos átomos de H, solo hay 1 átomo de C). Al nombrar aldehídos, la cadena principal de átomos de C debe incluir el carbono en el grupo carbonilo, el cual está numerado como posición 1 en la cadena carbonada. Se utiliza el nombre padre del hidrocarburo, pero se agrega el sufijo - al. (No confundir - al con - ol, que es el sufijo que se usa para los alcoholes.) Así que tenemos
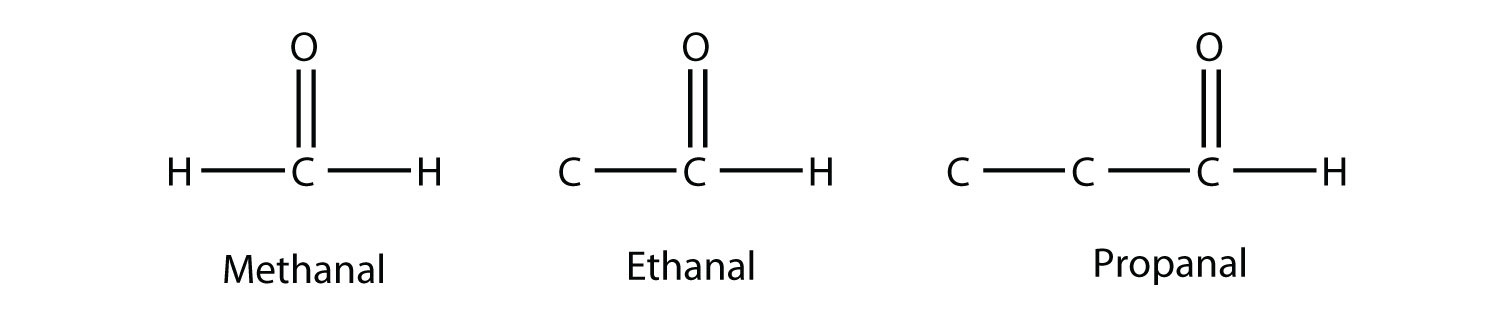
Metanal tiene un nombre común con el que te puede estar familiarizado: formaldehído. Lo principal a tener en cuenta de los aldehídos es que el grupo carbonilo está al final de una cadena carbonada.
Un grupo carbonilo en el medio de una cadena de carbono implica que ambos enlaces restantes del grupo carbonilo se hacen a átomos de C. Este tipo de molécula se llama cetona. A pesar de que los aldehídos y cetonas tienen el mismo grupo carbonilo, tienen diferentes propiedades químicas y físicas y se agrupan adecuadamente como dos tipos diferentes de compuestos. La cetona más pequeña tiene tres átomos de C en ella. Al nombrar una cetona, tomamos el nombre del hidrocarburo padre y cambiamos el sufijo a - uno:
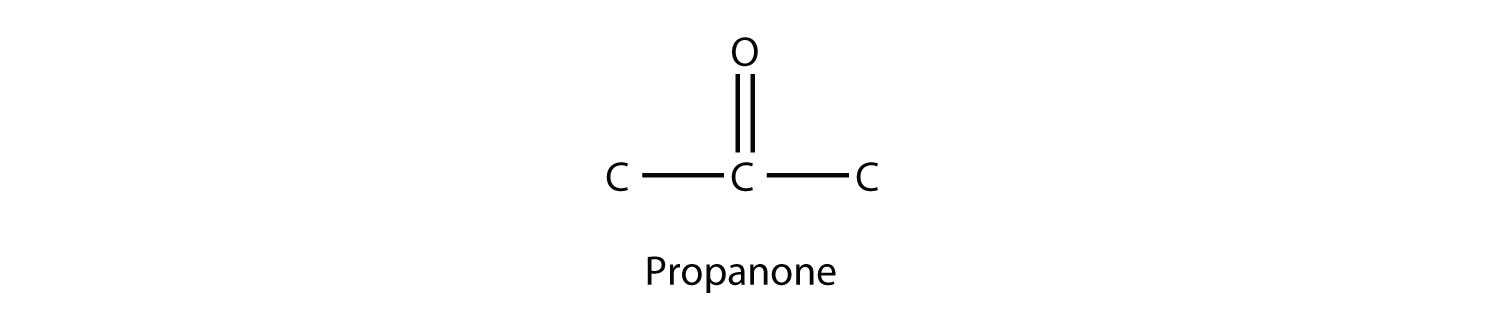
El nombre común para propanona es acetona. Con cetonas más grandes, debemos usar un número para indicar la posición del grupo carbonilo, al igual que un número se usa con alquenos y alquinos:
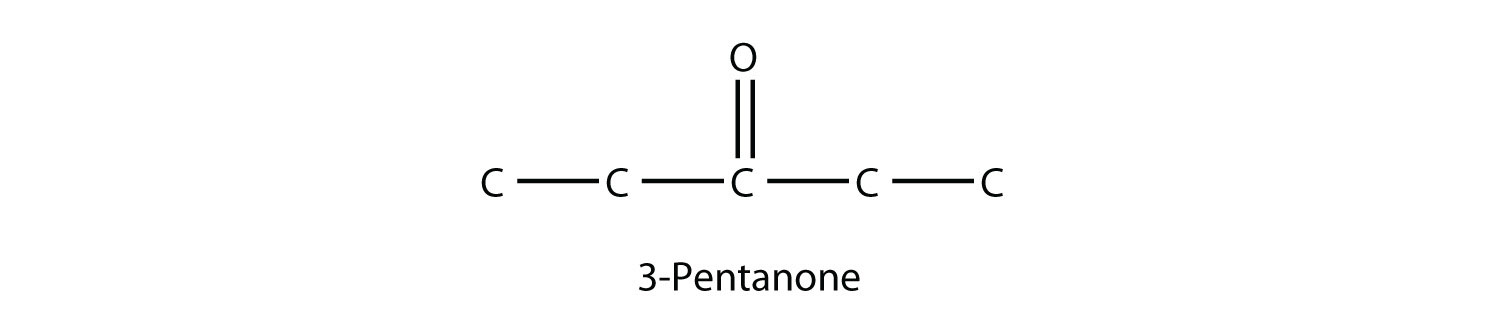
Hay otra manera de nombrar cetonas: nombrar los grupos alquilo que están unidos al grupo carbonilo y agregar la palabra cetona al nombre. Entonces la propanona también se puede llamar dimetil cetona, mientras que la 2-butanona se llama metil etil cetona.
Dibujar la estructura de 2-pentanona.
Solución
Esta molécula tiene cinco átomos de C en una cadena, con el grupo carbonilo en el segundo átomo de C. Su estructura es la siguiente:
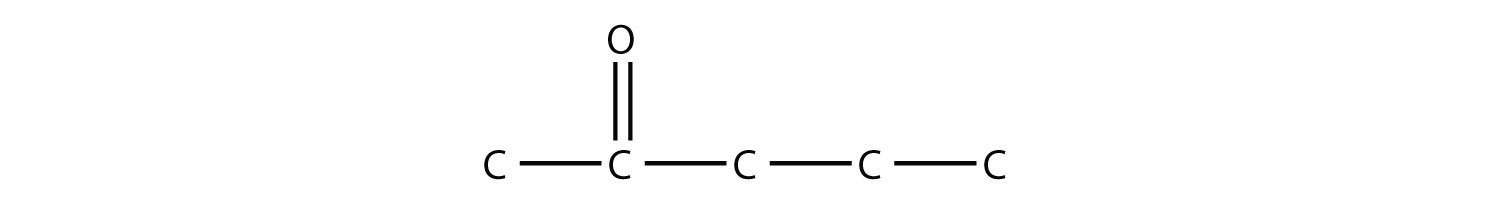
La combinación de un grupo funcional carbonilo y un grupo OH hace que el grupo carboxilo.
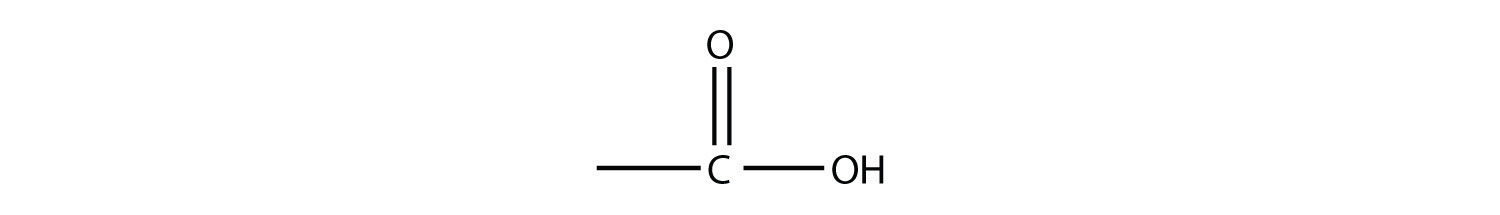
Las moléculas con un grupo carboxilo se denominan ácidos carboxílicos. Al igual que con los aldehídos, el grupo funcional en los ácidos carboxílicos se encuentra al final de una cadena carbonada. También al igual que con los aldehídos, el átomo de C en el grupo funcional se cuenta como uno de los átomos de C que define el nombre de hidrocarburo parental. Para nombrar ácidos carboxílicos, se usa el nombre parental del hidrocarburo, pero se agrega el sufijo - ácido oico:
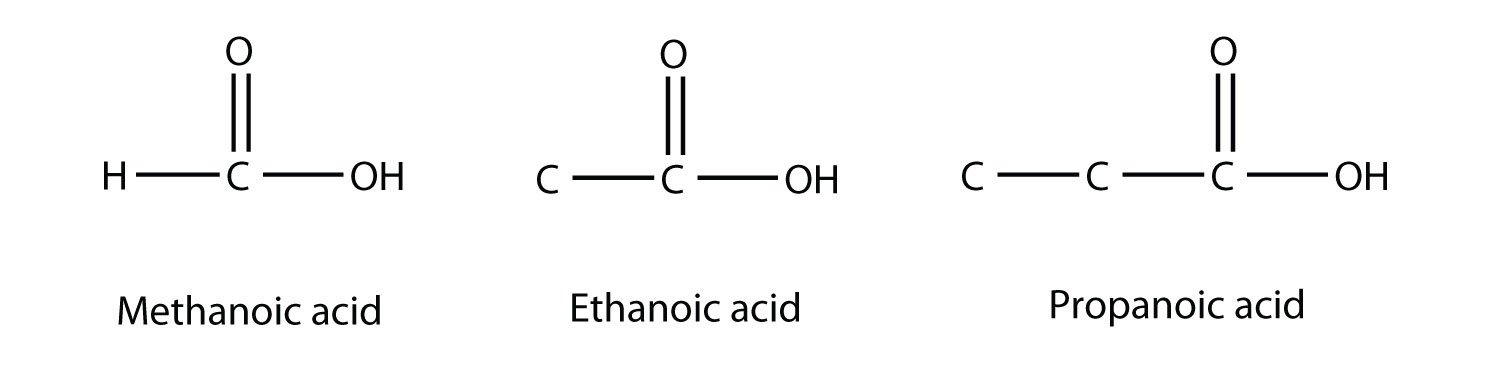
El ácido metanoico y el ácido etanoico también se denominan ácido fórmico y ácido acético, respectivamente. El ácido fórmico es el compuesto que hace picar ciertas picaduras de hormigas, mientras que el ácido acético es el principio activo en el vinagre.
¿Qué tan ácidos son los ácidos carboxílicos? Resulta que no son muy ácidos. Ningún ácido carboxílico está en la lista de ácidos fuertes (Tabla\(\PageIndex{1}\)). Esto significa que todos los ácidos carboxílicos son ácidos débiles. Una solución 1 M de ácido fórmico solo se disocia aproximadamente 1.3% en iones H + e iones formiato, mientras que una solución similar de ácido acético se ioniza en aproximadamente solo 0.4%. Algunos ácidos carboxílicos son más fuertes, por ejemplo, el ácido tricloroacético está aproximadamente 45% disociado en solución acuosa. Pero ningún ácido carboxílico se acerca a la cantidad de disociación del 100% requerida por la definición de un ácido fuerte.
Sin embargo, como su nombre indica, los ácidos carboxílicos actúan como ácidos en presencia de bases. El átomo de H en el grupo carboxilo se desprende como el ion H +, dejando un anión carboxilato:

Los iones carboxilato se nombran por el nombre ácido: el ácido - oico se reemplaza por - oato para nombrar el ion.
Completar la reacción química. ¿Se puede nombrar el ion carboxilato formado?
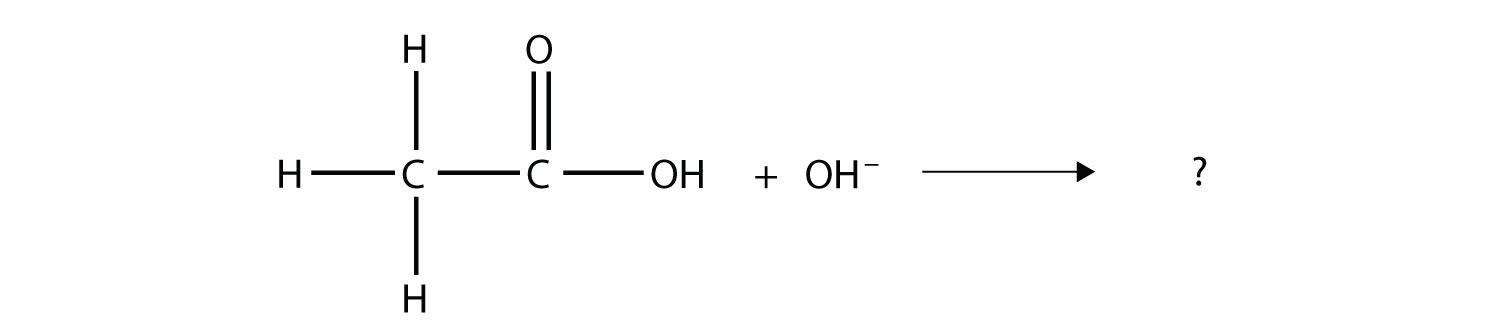
Solución
El ion OH — elimina el átomo de H que forma parte del grupo carboxilo:
El ion carboxilato, que tiene la fórmula estructural condensada CH 3 CO 2 −, es el ion etanoato, pero comúnmente se le llama el ion acetato.
Completar la reacción química. ¿Se puede nombrar el ion carboxilato formado?
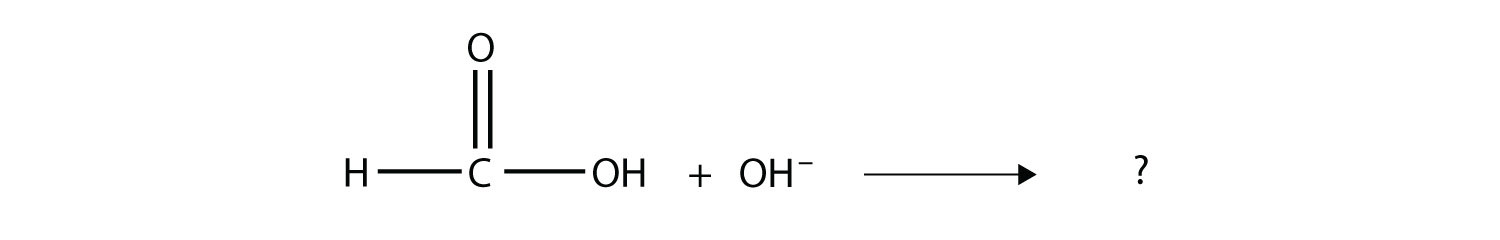
Contestar
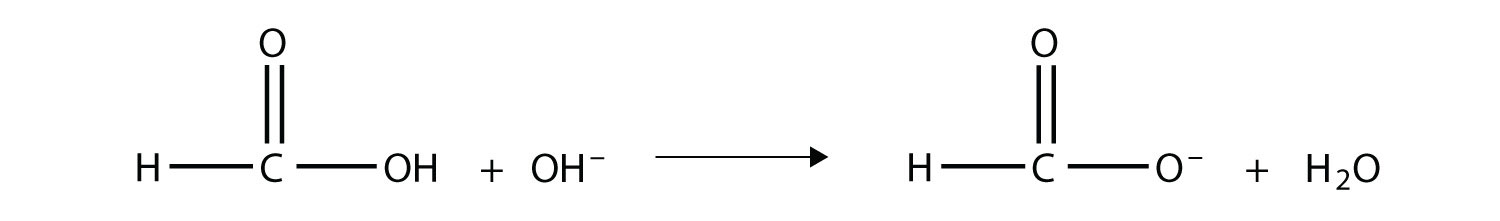
Una reacción a considerar es la de un ácido carboxílico y un alcohol. Cuando se combinan en las condiciones adecuadas, se eliminará una molécula de agua y las piezas restantes se combinarán para formar un nuevo grupo funcional: el grupo funcional éster:
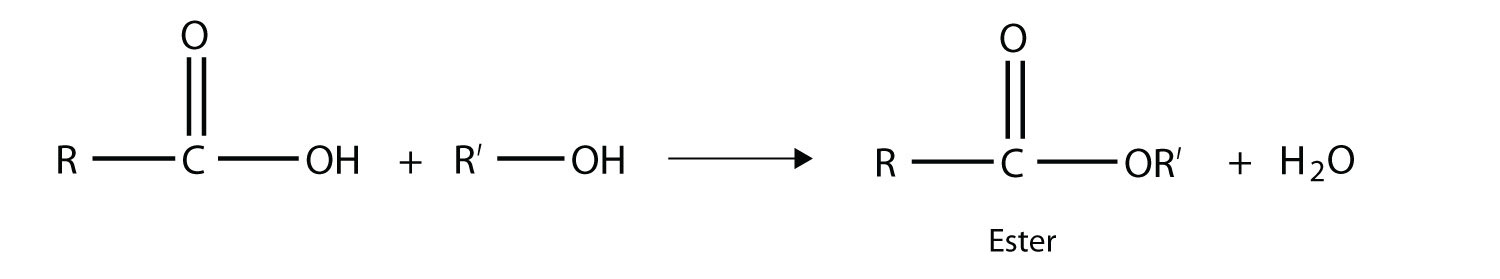
Observe cómo la molécula de ácido aporta un lado alquilo (representado por R), mientras que el alcohol aporta el otro lado (representado por R′). Los ésteres se nombran usando el nombre del grupo alquilo del alcohol más el nombre carboxilato del ácido. Por ejemplo, la molécula
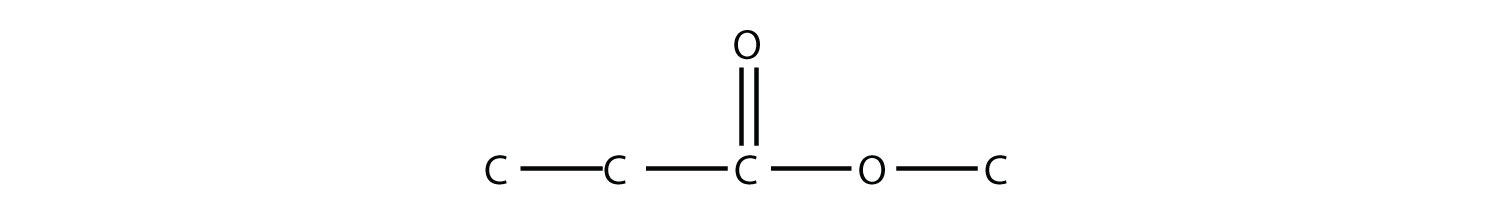
se llama propanoato de metilo.
Los ésteres son compuestos muy interesantes, en parte porque muchos tienen olores y sabores muy agradables. (Recuerda, ¡nunca pruebes nada en el laboratorio de química!) Muchos ésteres ocurren de forma natural y contribuyen al olor de las flores y al sabor de los frutos. Otros ésteres se sintetizan industrialmente y se agregan a los productos alimenticios para mejorar su olor o sabor; es probable que si comes un producto cuyos ingredientes incluyen saborizantes artificiales, esos saborizantes sean ésteres. Estos son algunos ésteres y sus usos, gracias a sus olores, sabores, o ambos:
| Ester | Gusto/Huele a | Ester | Gusto/Huele a |
|---|---|---|---|
| hexanoato de alilo | piña | formiato de isobutilo | frambuesa |
| acetato de bencilo | pera | acetato de isobutilo | pera |
| Butanoato de butilo | piña | fenilacetato de metilo | miel |
| butanoato de etilo | plátano | caprilato de nonilo | naranja |
| hexanoato de etilo | piña | acetato de pentil | manzana |
| heptanoato de etilo | albaricoque | etanoato de propilo | pera |
| pentanoato de etilo | manzana | isobutirato de propilo | ron |
Finalmente, el grupo funcional éter es un átomo de O que está unido a dos grupos orgánicos: R-O-R'
Los dos grupos R pueden ser iguales o diferentes. Nombrar éteres es como la forma alternativa de nombrar cetonas. En este caso, los grupos R se nombran secuencialmente, y se agrega la palabra éter. La molécula CH 3 OCH 3 es dimetil éter, mientras que CH 3 OCH 2 CH 3 es metil etil éter. El éter dietílico, otro éter, alguna vez se utilizó como anestésico, pero su inflamabilidad y toxicidad provocaron que cayera en desfavor. Las moléculas de éter más pequeñas que son líquidos a temperatura ambiente son solventes comunes para reacciones químicas orgánicas.
- Los aldehídos, cetonas, ácidos carboxílicos, ésteres y éteres tienen grupos funcionales que contienen oxígeno.
- Nombrar una similitud entre los grupos funcionales encontrados en aldehídos y cetonas. ¿Se puede nombrar una diferencia entre ellos?
- Explicar cómo se usa un ácido carboxílico para elaborar un éster.
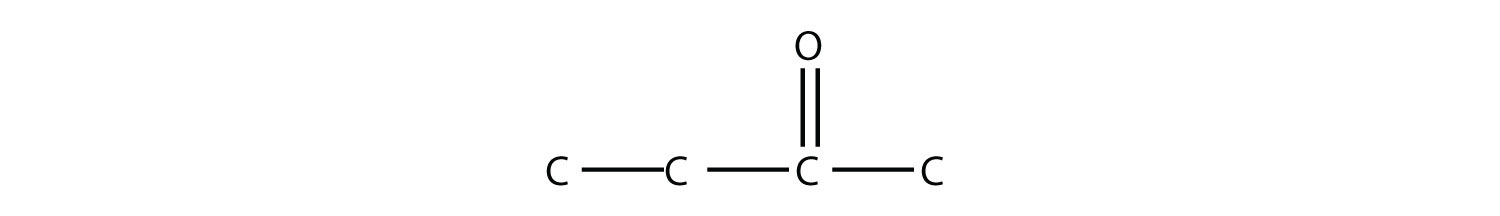
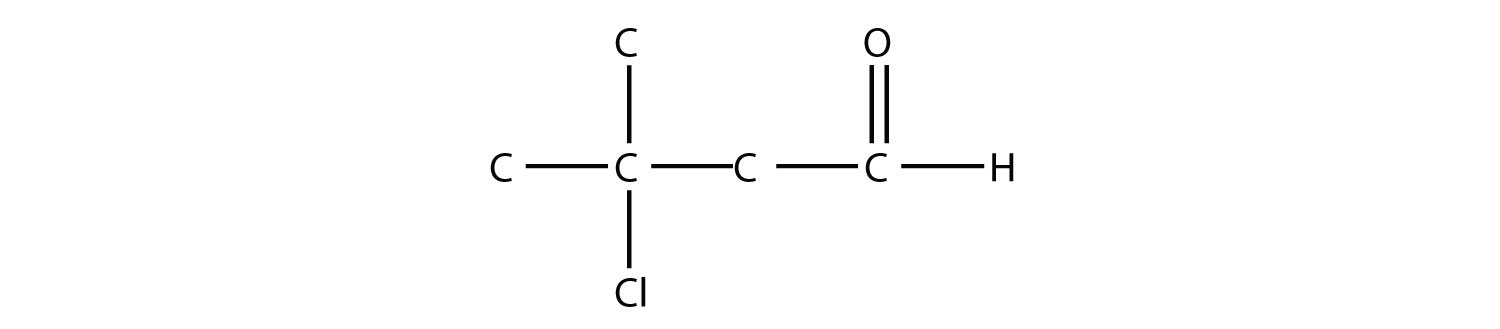
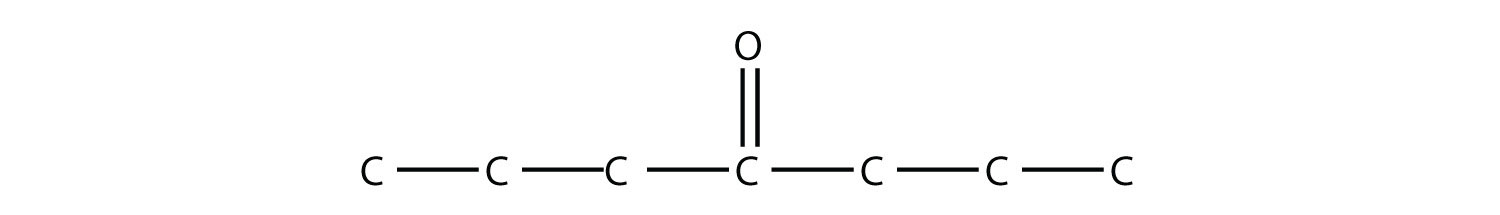
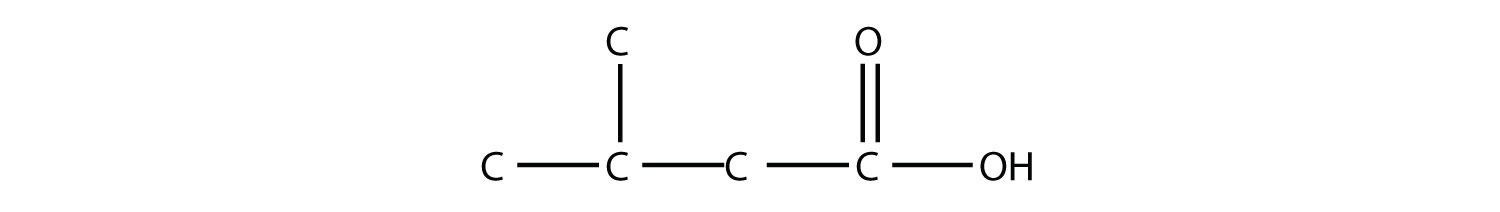
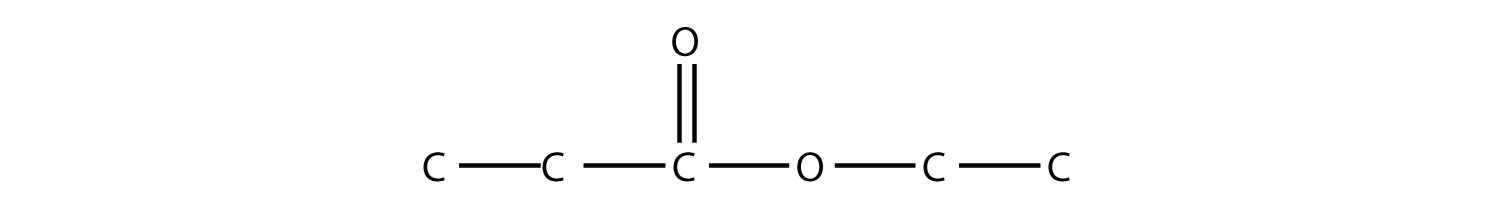
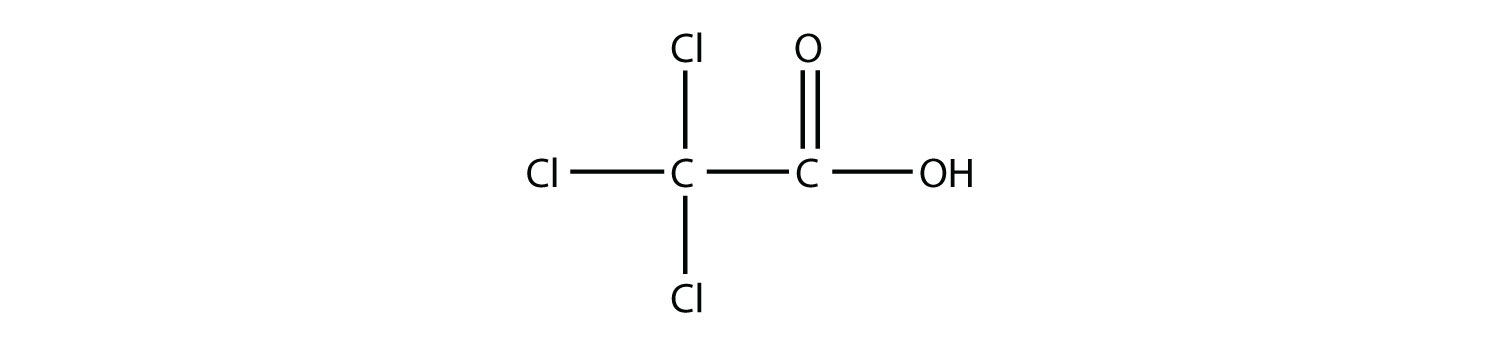
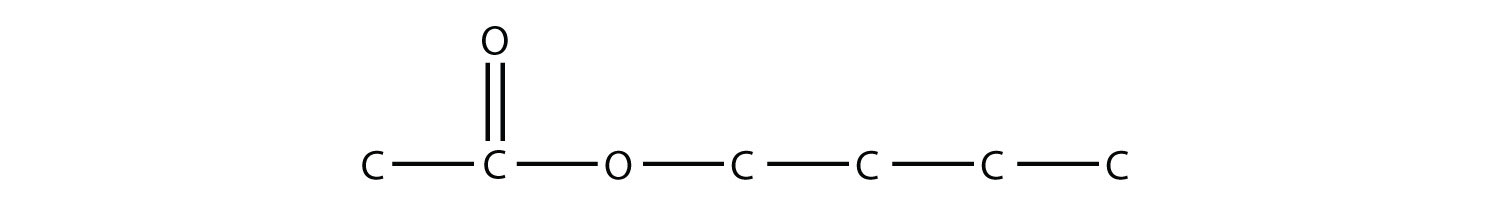
- Nombra cada molécula.
- Nombra cada molécula.
- Nombra cada molécula.
- Nombra cada molécula.
- Nombra la molécula.
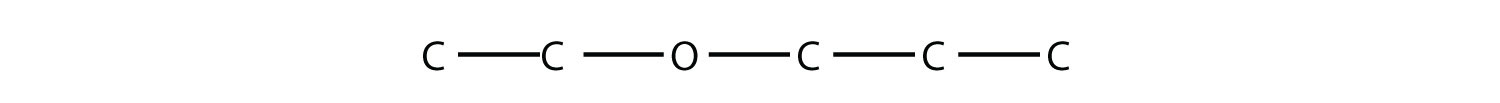
- Nombra la molécula.
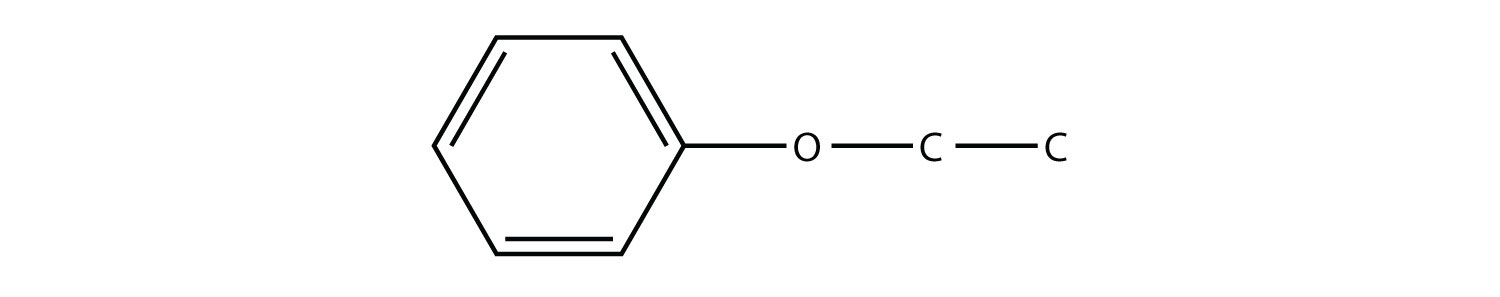
- Dar un nombre alternativo pero aceptable a la molécula en el Ejercicio 3b.
- Dar un nombre alternativo pero aceptable a la molécula en el Ejercicio 4b.
- Completa esta reacción química.
KOH.” style="ancho: 550px; alto: 82px;” width="550px” height="82px” data-cke-saved-src=”/@api /deki/files/96632/Ex_11.png "src=”/@api /deki/files/96632/Ex_11.png "data-quail-id="209">
- Completa esta reacción química.
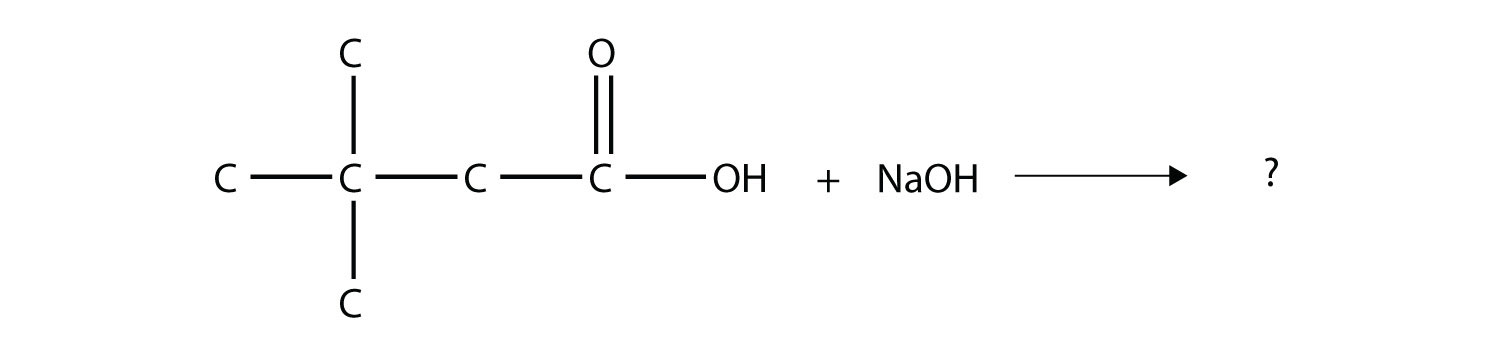
- El fármaco conocido como aspirina tiene esta estructura molecular:
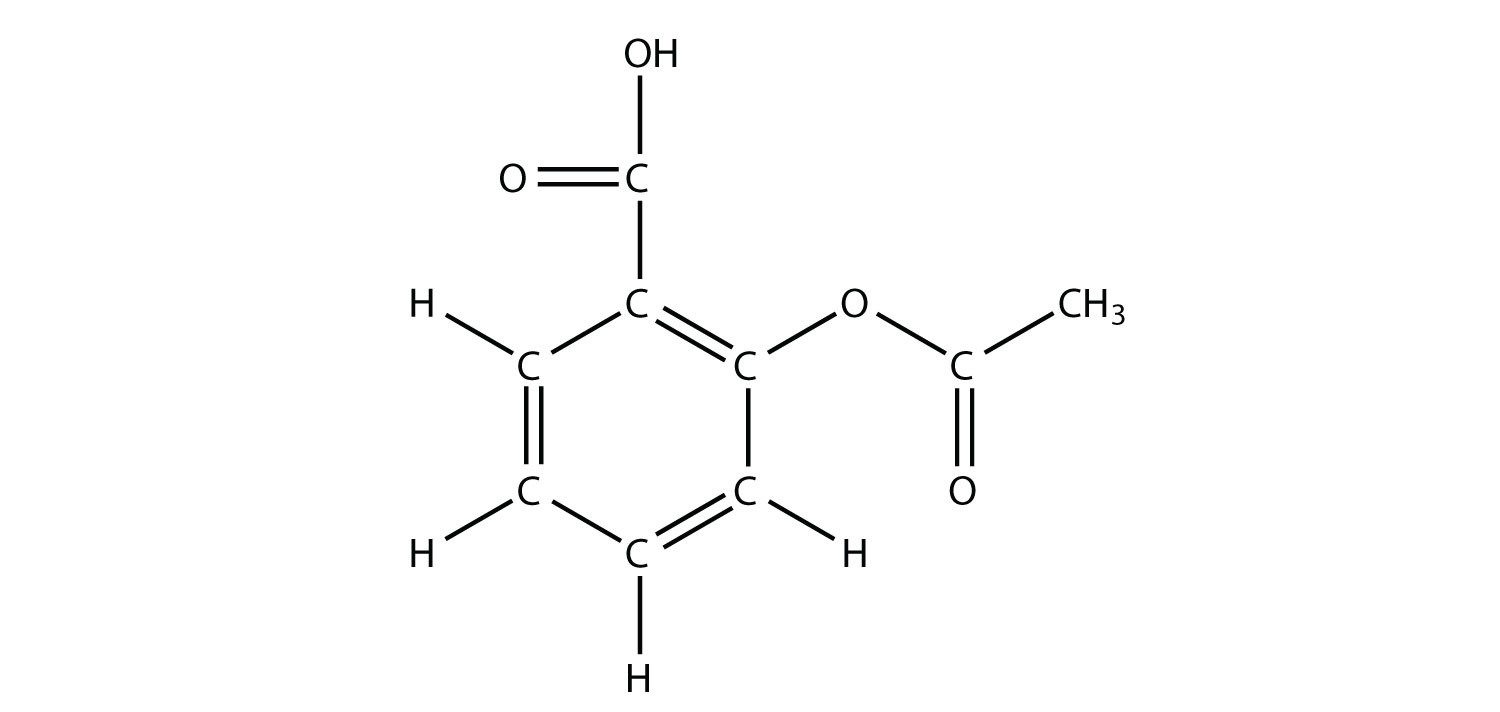 Identificar el (los) grupo (s) funcional (s) en esta molécula.
Identificar el (los) grupo (s) funcional (s) en esta molécula. - El fármaco conocido como naproxeno sódico es la sal sódica de esta molécula:
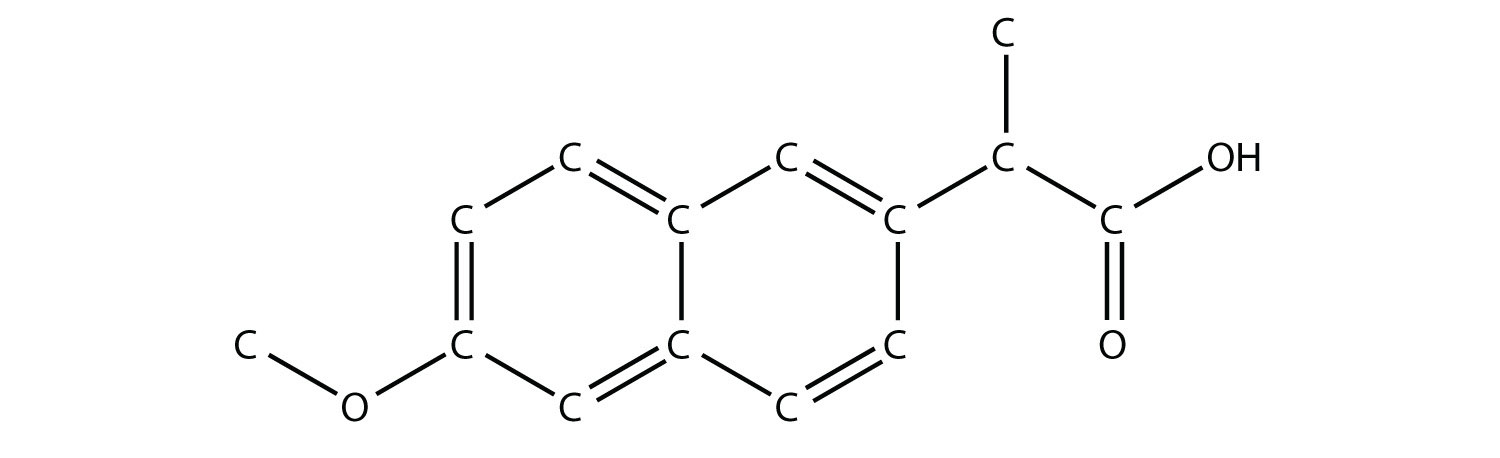 (Los átomos de H adicionales se omiten para mayor claridad). Identificar el grupo o grupos funcionales en esta molécula.
(Los átomos de H adicionales se omiten para mayor claridad). Identificar el grupo o grupos funcionales en esta molécula. - Identificar el éster hecho haciendo reaccionar estas moléculas.
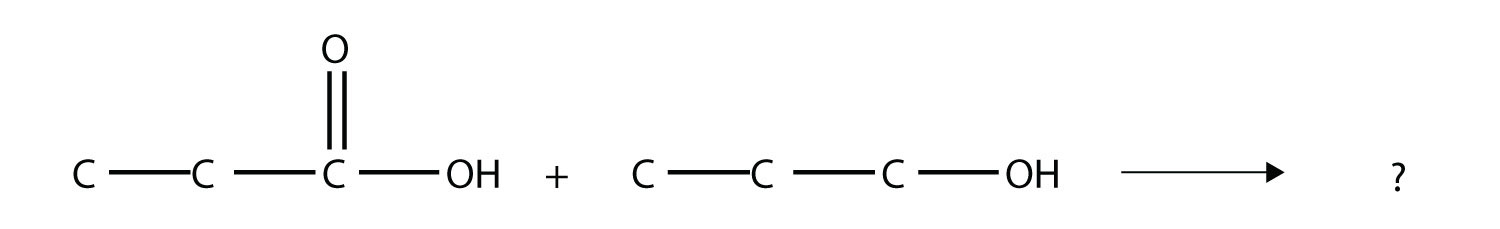
- Identificar el éster hecho haciendo reaccionar estas moléculas.
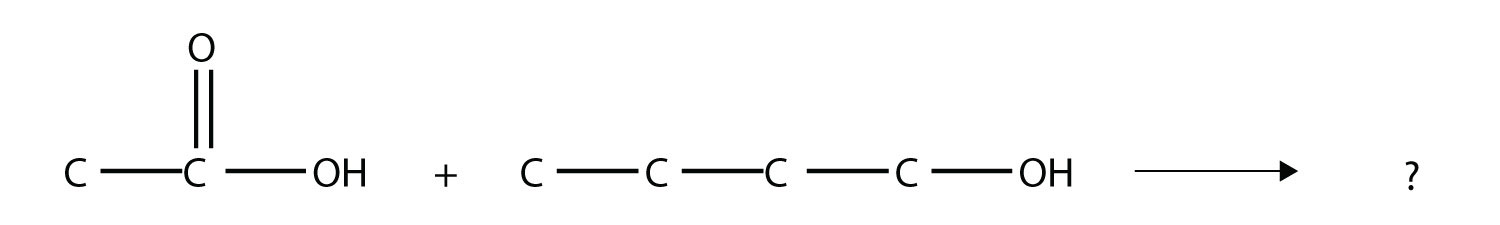



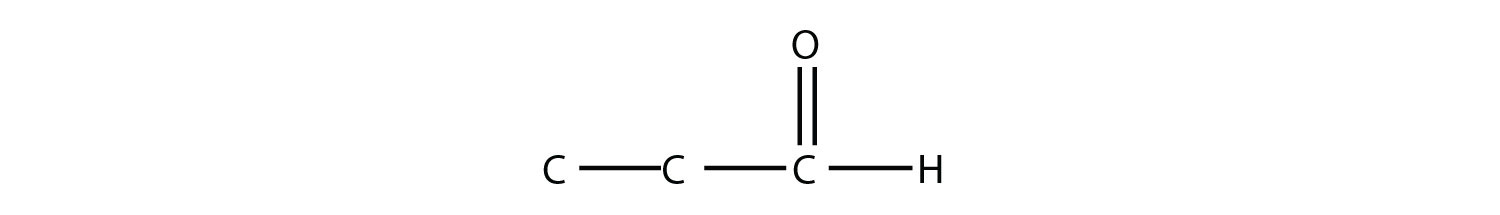
RESPUESTAS