1.5: Regla de Octeto - Enlace Iónico y Covalente (Revisión)
- Page ID
- 75922
Objetivo de aprendizaje
Dibujar, interpretar y convertir entre estructuras de Lewis (Kekule), Condensed y Bond-line
Nota: La revisión de química general en las secciones 1.3 - 1.6 se integra en el anterior Objetivo de Aprendizaje para la química orgánica en las secciones 1.7 y 1.8.
Para la química orgánica, el énfasis está en la química del carbono. La química del carbono se vuelve más interesante cuando el carbono está unido al oxígeno y/o nitrógeno u otros heteroátomos, átomos que NO son carbono o hidrógeno. Por lo tanto, la regla del octeto es un factor fuerte en la química orgánica y solo es violada por elementos no carbonados como hidrógeno, boro, aluminio, azufre y fósforo.
¿Por qué algunas sustancias son moléculas unidas químicamente y otras son una asociación de iones? La respuesta a esta pregunta depende de las estructuras electrónicas de los átomos y de la naturaleza de las fuerzas químicas dentro de los compuestos. Aunque no hay límites claramente definidos, los enlaces químicos se clasifican típicamente en tres tipos principales: enlaces iónicos, enlaces covalentes y enlaces metálicos. En este capítulo se discutirá cada tipo de enlace y las propiedades generales que se encuentran en las sustancias típicas en las que se presenta el tipo de enlace
- Los enlaces iónicos son el resultado de fuerzas electrostáticas que existen entre iones de carga opuesta. Estos enlaces típicamente implican un metal con un no metal
- Los enlaces covalentes son el resultado de la distribución de electrones entre dos átomos. Los enlaces típicamente implican un elemento no metálico con otro
- Enlaces metálicos Estos enlaces se encuentran en metales sólidos (cobre, hierro, aluminio) con cada metal unido a varios grupos vecinos y uniendo electrones libres para moverse a lo largo de la estructura tridimensional.
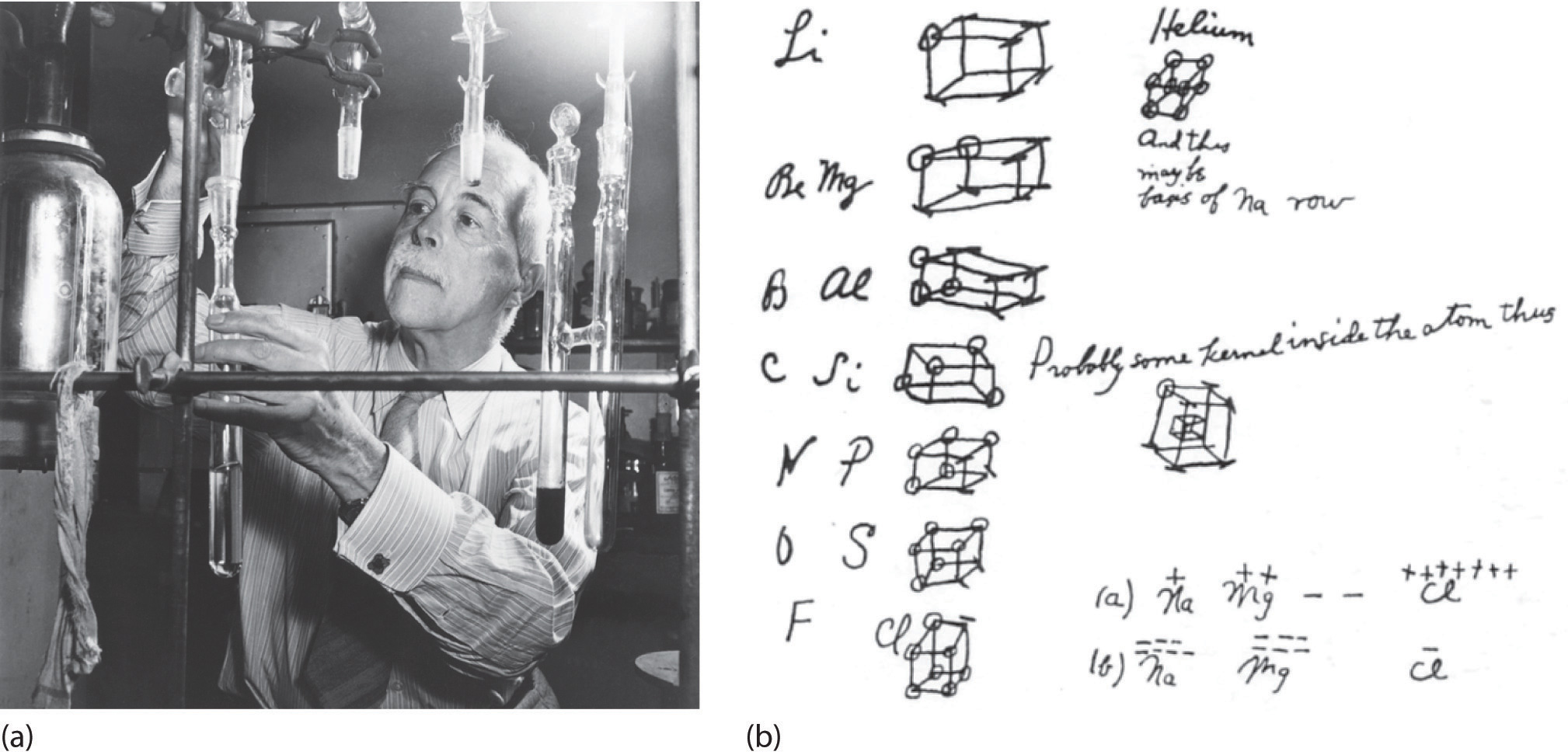
La regla del octeto
En 1904, Richard Abegg formuló lo que ahora se conoce como regla de Abegg, que establece que la diferencia entre las valencias máximas positivas y negativas de un elemento es frecuentemente de ocho. Esta regla fue utilizada más tarde en 1916 cuando Gilbert N. Lewis formuló la “regla del octeto” en su teoría de átomos cúbicos. La regla del octeto se refiere a la tendencia de los átomos a preferir tener ocho electrones en la capa de valencia. Cuando los átomos tienen menos de ocho electrones, tienden a reaccionar y formar compuestos más estables. Los átomos reaccionarán para ponerse en el estado más estable posible. Un octeto completo es muy estable porque todos los orbitales estarán llenos. Los átomos con mayor estabilidad tienen menos energía, por lo que una reacción que incremente la estabilidad de los átomos liberará energía en forma de calor o luz; las reacciones que disminuyan la estabilidad deben absorber energía, haciéndose más frías.
La regla del octeto: Los átomos a menudo ganan, pierden o comparten electrones para lograr el mismo número de electrones que el gas noble más cercano a ellos en la tabla periódica.
Al discutir la regla del octeto, no consideramos electrones d o f. Solo los electrones s y p están involucrados en la regla del octeto, convirtiéndola en una regla útil para los elementos del grupo principal (elementos que no están en los bloques de metal de transición o metales de transición internos); un octeto en estos átomos corresponde a configuraciones de electrones que terminan en s 2 p 6.
Ejemplo de enlaces iónicos
Los símbolos de punto de Lewis también se pueden usar para representar los iones en compuestos iónicos. La reacción del cesio con flúor, por ejemplo, para producir el compuesto iónico CsF se puede escribir de la siguiente manera:

No se muestran puntos en Cs + en el producto porque el cesio ha perdido su electrón de valencia simple al flúor. La transferencia de este electrón produce el ion Cs +, que tiene la configuración de electrones de valencia de Xe, y el ion F −, que tiene un total de ocho electrones de valencia (un octeto) y la configuración de electrones Ne. Esta descripción concuerda con la afirmación de que entre los elementos principales del grupo, los iones en compuestos iónicos binarios simples generalmente tienen las configuraciones electrónicas del gas noble más cercano. La carga de cada ion está escrita en el producto, y el anión y sus electrones están encerrados entre paréntesis. Esta notación enfatiza que los iones están asociados electrostáticamente; no se comparten electrones entre los dos elementos.

