3.6: Actividad óptica
- Page ID
- 72616
Las moléculas quirales, como aprendimos en la introducción a este capítulo, tienen una propiedad óptica interesante. Es posible que sepas por estudiar física que las ondas de luz son campos eléctricos y magnéticos oscilantes. En la luz ordinaria, la oscilación se orienta aleatoriamente en un número infinito de planos. Cuando la luz ordinaria pasa a través de un polarizador, todos los planos de oscilación se filtran excepto uno, lo que resulta en luz polarizada en el plano.
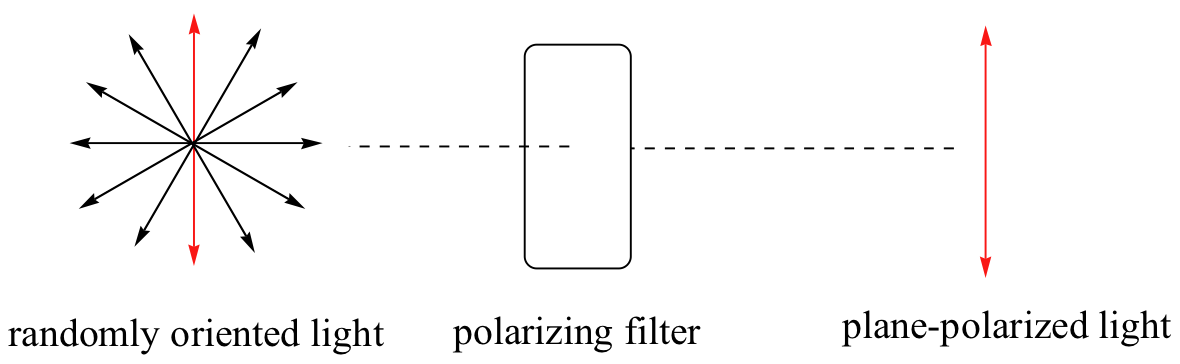
Un haz de luz polarizada en plano, al pasar a través de una muestra de un compuesto quiral, interactúa con el compuesto de tal manera que el ángulo de oscilación rotará. Esta propiedad se llama actividad óptica.
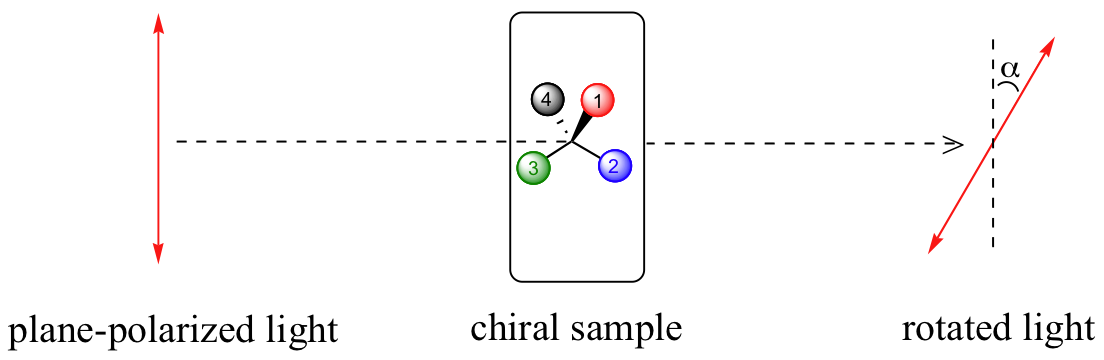
Si un compuesto gira la luz polarizada plana en el sentido de las agujas del reloj (+), se dice que es dextrorrotatorio, mientras que si gira la luz en sentido contrario a las agujas del reloj (-) es levorrotatorio. (Mencionamos los aminoácidos L y D en la sección anterior: los L-aminoácidos son levorrotatorios). La magnitud de la actividad óptica observada depende de la temperatura, la longitud de onda de la luz utilizada, el disolvente, la concentración de la muestra quiral y la longitud de la trayectoria del tubo de muestra (la longitud de la trayectoria es la longitud que la luz polarizada plana viaja a través de la muestra quiral). Por lo general, las mediciones de actividad óptica se realizan en un tubo de muestra de longitud de trayectoria de 1 decímetro (10 cm) a 25 ° C, utilizando como fuente de luz la llamada “línea D” de una lámpara de sodio, que tiene una longitud de onda de 589 nm. La rotación específica de un compuesto quiral puro a 25 ° se expresa por la expresión:
\[[\alpha]_{\mathrm{D}}^{25}=\frac{\alpha_{\mathrm{obs}}}{l c} \nonumber\]
donde\(\alpha_{obs}\) está la rotación observada,\(l\) es la longitud de la trayectoria en decímetros, y\(c\) es la concentración de la muestra en gramos por 100 mL. Es decir, la rotación específica de un compuesto quiral es la rotación óptica que se observa cuando se disuelve 1 g del compuesto en suficiente disolvente dado para hacer 100 mL de solución, y la rotación se mide en una cubeta de 1 dm a 25 o C usando luz de una lámpara de sodio.
Cada molécula quiral tiene una rotación específica característica, la cual se registra en la literatura química como una propiedad física al igual que el punto de fusión o densidad. Diferentes enantiómeros de un compuesto siempre rotarán la luz polarizada plana con una magnitud igual pero opuesta. El (S) -ibuprofeno, por ejemplo, tiene una rotación específica de +54.5 o (dextrorrotatorio) en metanol, mientras que el (R) -ibuprofeno tiene una rotación específica de -54.5 o. No existe relación entre la designación R/S del compuesto quiral y la dirección de su rotación específica. Por ejemplo, el enantiómero S del ibuprofeno es dextrorrotatorio, pero el enantiómero S del gliceraldehído es levorrotatorio.
Una mezcla 50:50 de dos enantiómeros (una mezcla racémica) no tendrá actividad óptica observable, ya que las dos actividades ópticas se cancelan entre sí. En un dibujo estructural, un enlace 'squigly' de un centro quiral indica una mezcla de ambas configuraciones R y S.

Las moléculas quirales a menudo se marcan de acuerdo con si son dextrorrotatorias o levorrotatorias, así como por su designación R/S. Por ejemplo, los enantiómeros puros del ibuprofeno están etiquetados (S) - (+) -ibuprofeno y (R) - (-) -ibuprofeno, mientras que (±) -ibuprofeno se refiere a la mezcla racémica, que es la forma en que se vende el medicamento a los consumidores.
La rotación específica de (R) -limoneno es +11.5 o en etanol. ¿Cuál es la rotación observada esperada de una muestra de 6.00 g (S) -limoneno disuelto en etanol a un volumen total de 80.0 mL en una cubeta de 1.00 dm (10.0 cm) de longitud de trayectoria?
Ejercicio 3.15
La rotación específica de (S) -carvona es de +61 °, medida 'pura' (muestra líquida pura, sin disolvente). La rotación óptica de una mezcla de R y S carvona se mide a -23 °. ¿Qué enantiómero está en exceso en la mezcla?
Soluciones a los ejercicios
Los veinte aminoácidos naturales, excepto la glicina, tienen un centro quiral en su a lpha-carbono (recordemos que la estructura básica de los aminoácidos y la terminología se introdujo en la sección 1.3). Prácticamente todos los aminoácidos que se encuentran en la naturaleza, tanto en forma de aminoácidos libres como incorporados a péptidos y proteínas, tienen lo que se denomina en la literatura bioquímica como la configuración 'L':
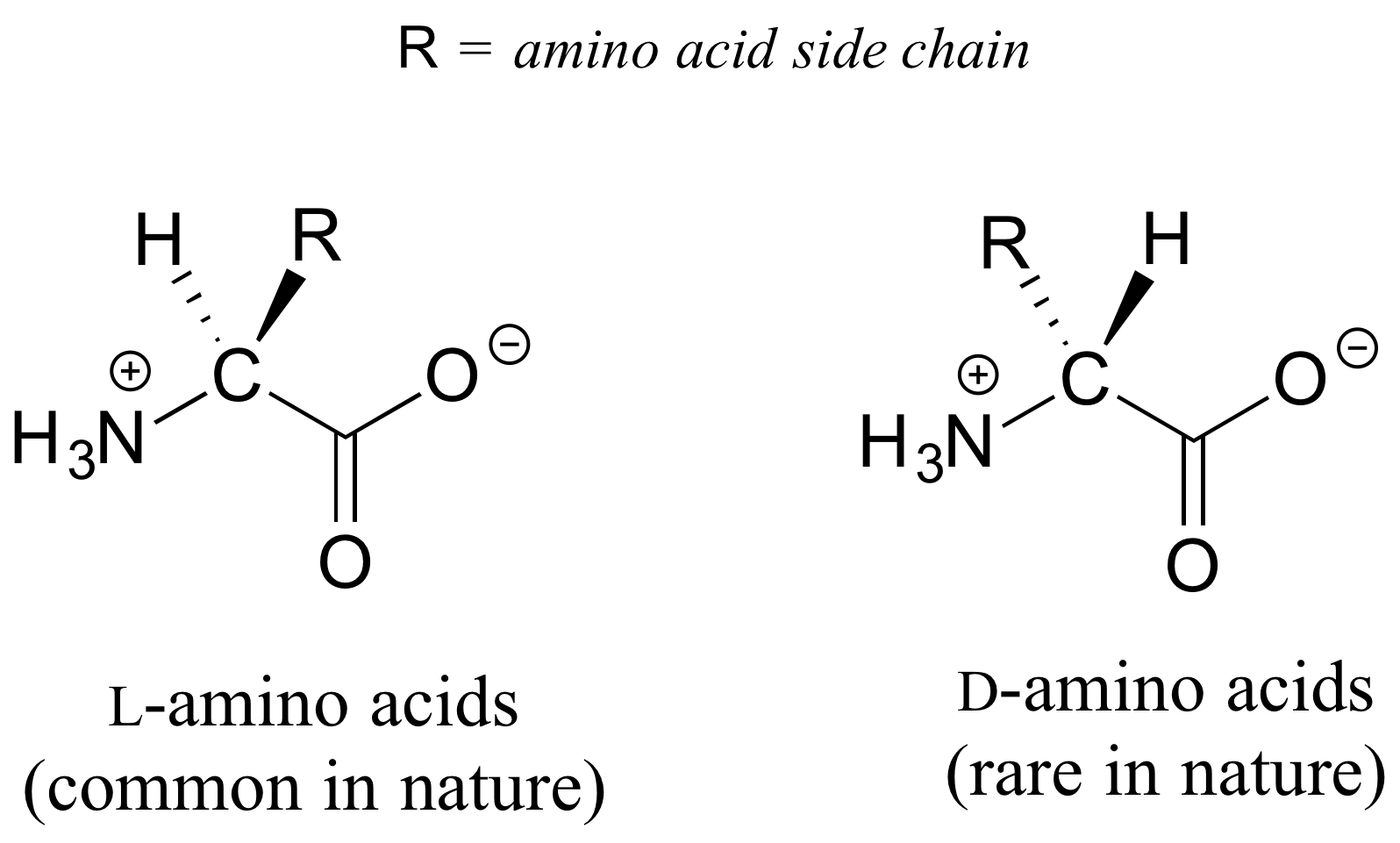
La 'L' indica que estos estereoisómeros de aminoácidos son levorrotatorios. Todos menos uno de los 19 L-aminoácidos tienen estereoquímica S en el carbono a-, utilizando las reglas del sistema de nomenclatura R/S.
Los D-aminoácidos (el D significa dextrorrotatorio) son muy raros en la naturaleza, pero aprenderemos sobre un ejemplo interesante de un péptido que contiene un residuo de D-aminoácido más adelante en el capítulo 12.
¿Cuál de los 20 L-aminoácidos comunes que se encuentran en la naturaleza tiene la configuración R? Consulte la tabla de aminoácidos para ver las estructuras.
Soluciones a los ejercicios


