16.7: Flavina como portador de un electrón
- Page ID
- 72068
En el capítulo 15 vimos cómo las coenzimas nicotinamida y flavina pueden actuar como aceptores o donantes de dos electrones en etapas redox de transferencia de hidruro. Recordemos que se mencionó que la flavina, (pero no la nicotinamida) también puede participar en etapas de transferencia de un solo electrón a través de un intermedio radical estabilizado llamado semiquinona.. Frey p. 162 fig 3-30; Silverman p. 122 sch. 3.34; J Phys Chem A. 2013, 117, 11136 fig 2)
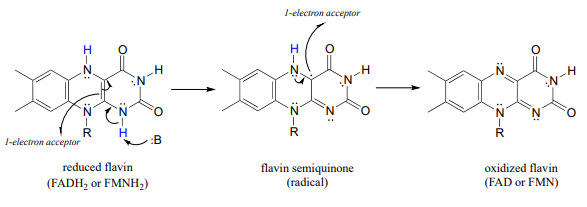
Obsérvese en esta reacción que en general, la flavina pierde o gana dos electrones y dos protones, al igual que en las reacciones redox dependientes de flavina que vimos en el capítulo 15. La diferencia aquí es que los electrones se transfieren uno a la vez, en lugar de emparejarse en forma de un ion hidruro.
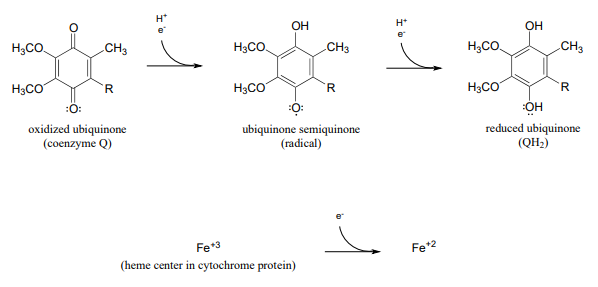
Dos ejemplos importantes de especies aceptoras de electrones simples en el metabolismo humano son la ubiquinona (coenzima\(Q\)) and the oxidized form of cytochrome. Ubiquinone is a coenzyme that can transfer single electrons via a semiquinone state analogous to that of flavin, and cytochrome is a protein containing a 'heme' iron center which shuttles between the \(Fe^{+3}\) (oxidized) and \(Fe^{+2}\) (reduced) state.
La discusión adicional de los mecanismos de las reacciones de flavina de un solo electrón está fuera de nuestro alcance aquí, pero cuando estudias la 'cadena respiratoria' en un curso de bioquímica, obtendrás una apreciación más profunda de la importancia de la flavina en los procesos de transferencia de electrones simples.


