16.E: Reacciones radicales (Ejercicios)
- Page ID
- 72052
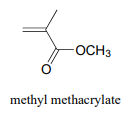
P16.1: El plexiglás es un polímero de metacrilato de metilo. Mostrar un mecanismo para las dos primeras etapas de propagación de la polimerización (usar\(X\cdot\) para denotar el iniciador de radicales), y mostrar una estructura para el polímero de plexiglás. Asumir un proceso de adición de alqueno similar al que se muestra en el texto para el polietileno.
P16.2: En la sección 16.3 vimos cómo la acrilamida polimeriza para formar la poliacrilamida utilizada en los geles de proteína PAGE. La poliacrilamida por sí misma no es suficiente por sí misma para formar el gel: las largas cadenas de poliacrilamida simplemente se deslizan una contra la otra, como los espaguetis hervidos. Para hacer un gel PAGE, con poros para que las proteínas se desplacen, necesitamos un entrecruzador, algo para unir las cadenas, formando una estructura tridimensional similar a una red. Por lo general, se agrega una pequeña cantidad de bis-acrilamida a la acrilamida en la mezcla de polimerización para este propósito.
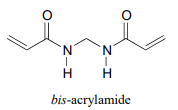
Proponer un mecanismo radical que muestre cómo la bis- acrilamida podría formar enlaces cruzados entre dos cadenas de poliacrilamida.
P16.3: El resveratrol es un antioxidante natural que se encuentra en el vino tinto (ver sección 16.5 para ver la estructura).
- Dibuje una estructura de resonancia para ilustrar cómo el radical resveratrol se deslocaliza por resonancia.
- Indica todos los carbonos en tu estructura a los que se puede deslocalizar el radical.
- Dibujar un radical resveratrol alternativo (uno en el que se haya abstraído un átomo de hidrógeno de uno de los otros dos grupos fenólicos). ¿A cuántos carbonos se puede deslocalizar este radical?
- La estructura de la curcumina se muestra en la misma figura que la del resveratrol, en la sección16.5. Dibujar dos contribuyentes de resonancia de un radical curcumina, uno en el que el electrón desapareado está en un oxígeno fenólico, y otro en el que el electrón desapareado está en un oxígeno cetónico.
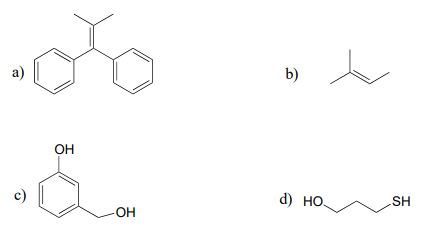
P16.4: Dibuja las especies intermedias radicales que esperarías formar cuando cada uno de los compuestos a continuación reaccione con un iniciador radical.
P16.5: Azobis (isobutirnitrilo) es un iniciador radical ampliamente utilizado que experimenta rápidamente descomposición homolítica cuando se calienta.
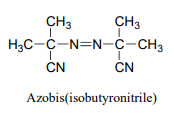
Predecir los productos de esta reacción de descomposición, y mostrar un mecanismo probable. ¿Cuál es la fuerza impulsora termodinámica para la escisión homolítica?
P16.6:
- Cuando el 2-metilbutano se somete a gas cloro y calor, se\(C_5H_{11}Cl\) pueden formar varios cloroalcanos isoméricos con la fórmula. Dibujar estructuras para estos isómeros, y para cada uno dibujar el radical alquilo intermedio que condujo a su formación.
- En la parte a), ¿cuál es el intermedio radical más estable?
- En la reacción de la parte a), la abundancia relativa de diferentes isómeros en el producto no es exclusivamente un reflejo de la estabilidad relativa de los intermedios radicales. Explique.
P16.7: Aprendimos en el capítulo 14 que\(HBr\) reaccionará con alquenos en reacciones de adición electrófila con regioselectividad 'Markovnikov'. Sin embargo, cuando el alqueno inicial contiene incluso una pequeña cantidad de peróxido contaminante (lo que ocurre cuando se le permite entrar en contacto con el aire), a menudo se observa una cantidad significativa de producto 'anti-Markovnikov'.
- Proponer un mecanismo para la formación del producto de adición anti-Markovnikov cuando el 1-buteno reacciona con\(HBr\) contener una pequeña cantidad de peróxido de benzoilo
- Predecir el producto y proponer un mecanismo para la adición de etanotiol al 1-buteno en presencia de peróxido.
P16.8: En la sección 11.5 aprendimos que la aspirina actúa bloqueando la acción de una enzima que cataliza un paso clave en la biosíntesis de prostaglandinas, una clase de moléculas de señalización bioquímica. La enzima en cuestión, la prostaglandina\(H\) sintasa (EC 1.14.99.1) cataliza la reacción a través de varios pasos de un solo electrón. Primero, un radical de oxígeno unido a hierro en la enzima extrae un átomo de hidrógeno del araquidonato. El radical araquidonato intermedio reacciona entonces con oxígeno molecular para formar un anillo que contiene oxígeno de cinco miembros, seguido del cierre de un anillo de ciclopentano para producir otro radical intermedio. (Bioquímica 2002, 41, 15451.)

Proponer un mecanismo para los pasos de la reacción que se muestran en esta figura.
P16.9: Algunas enzimas redox utilizan cobre para ayudar en las etapas de transferencia de electrones. Un ejemplo importante es la dopamina b-monooxigenasa (EC 1.14.1.1), que cataliza la siguiente reacción:
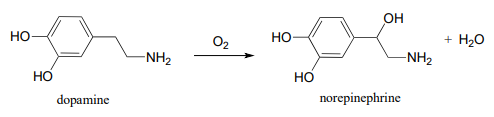
Se han propuesto los siguientes intermedios: (ver Biochemistry 1994, 33, 226) Silverman p. 222
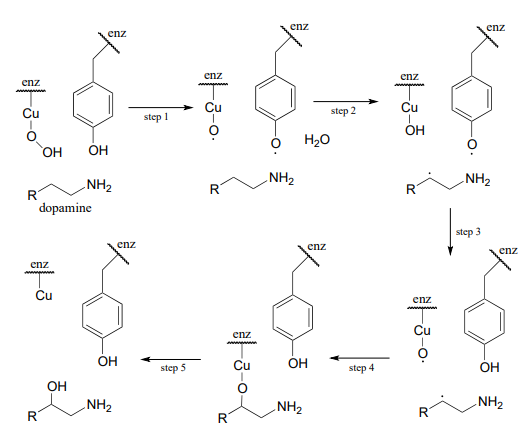
Dibuja flechas mecanicistas para los pasos 1-4.


