III. Tellurides
- Page ID
- 79963
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Los compuestos de organoteluro que se utilizan como precursores de radicales en la química de carbohidratos generalmente se sintetizan mediante una reacción de desplazamiento nucleofílico como la que se muestra en la ecuación 14. 79
.png)
La mayoría de los compuestos preparados de esta manera son telururos anoméricos. Los telururos de furanosilo son relativamente inestables y tienden a descomponerse en pocos días, 80—82 pero aunque sus homólogos de piranosilo pueden existir sin cambios en estado sólido durante meses, 79 calentar o exponer telururos de piranosilo a la luz UV provoca epimerización (eq 15). 83
.png)
Dos procedimientos, ambos de fotólisis, provocan una reacción radical de los telururos de carbohidratos. El primero de ellos es la homólisis fotoquímica de un enlace carbono-teluro, una reacción que genera el más estable de los dos posibles radicales centrados en carbono (Esquema 11).

Un ejemplo de reacción que se produce de esta manera se encuentra eq. 16. 83 El segundo procedimiento para la formación de radicales a partir de un telururo de carbohidrato exige la descomposición fotoquímica de la N- acetoxi-2-tiopiridona para producir un radical metilo que luego reacciona con el telururo (Esquema 12).
.png)
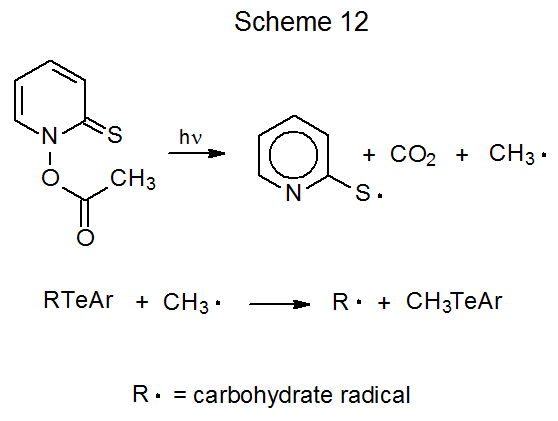
La ecuación 17 describe una reacción de ciclación iniciada de esta manera. 84 Las reacciones de los radicales carbohidrato formados a partir de telururos incluyen ciclación, adición 84,85, reducción 86—89, 83 y migración grupal. 83 Es razonable suponer que la reacción de un telururo de carbohidrato con un radical metilo implica, como indican los cálculos orbitales moleculares, la formación de un intermedio con un átomo de teluro hipervalente (Esquema 13). 90
.png)