3.3F: Solventes Mixtos
- Page ID
- 73978
Cuando no se puede encontrar un solo disolvente que cumpla con todos los criterios para la cristalización, puede ser posible usar un disolvente mixto. Se elige un par de solventes: uno en el que el compuesto es soluble (llamado el "solvente soluble “), y uno en el que el compuesto es insoluble (llamado el" solvente insoluble “). Los dos disolventes deben ser miscibles entre sí para que su solubilidad entre sí no limite las proporciones utilizadas. En el Cuadro 3.2 se muestra una lista de disolventes mixtos comunes utilizados en la cristalización.
| Par de Solventes |
|---|
| Metanol/Agua |
| Etanol/Agua |
| Acetona/Agua |
| Metanol/éter dietílico |
| Éter de petróleo (o hexanos)/éter dietílico |
| Hexanos/Acetato de etilo |
Para realizar una cristalización usando un disolvente mixto, el sólido a cristalizar se disuelve primero en la cantidad mínima de “disolvente soluble” caliente, luego se agrega gota a gota “disolvente insoluble” caliente hasta que la solución se vuelve ligeramente turbia. Luego se agrega una pequeña porción adicional de disolvente soluble en caliente para aclarar la solución, y la solución se reserva para que se enfríe y cristalice lentamente. En la Figura 3.13 se muestra un diagrama que describe este proceso.
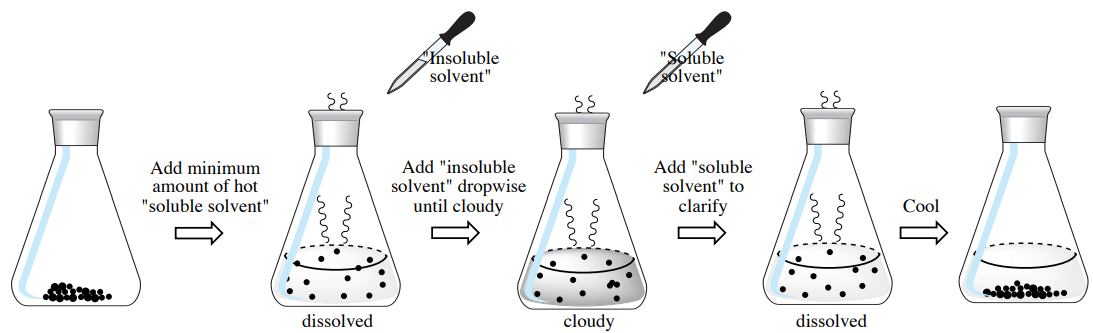
Aunque este procedimiento puede producir buenos resultados, cuando es posible suele ser mejor usar un solo disolvente para la cristalización. A medida que se calienta un disolvente mixto, la composición puede cambiar a medida que los disolventes se evaporan a diferentes velocidades, lo que puede afectar la solubilidad del compuesto en el disolvente mixto. También, las cristalizaciones a partir de disolventes mixtos a veces se “extraen aceite”, donde el compuesto disuelto sale de la solución por encima de su punto de fusión y forma un líquido en lugar de un sólido.
Para probar la cristalización de un disolvente mixto, utilice el procedimiento que sigue. Este proceso se demuestra cristalizando ácido trans-cinámico a partir de un disolvente mixto de agua y metanol (Figuras 3.14 + 3.15).

- Utilizar el método descrito anteriormente (\(100 \: \text{mg}\)compuesto en\(3 \: \text{mL}\) disolvente), para encontrar un par de disolventes: un disolvente en el que el compuesto es soluble y un disolvente en el que el compuesto es insoluble (Figura 3.14). Los disolventes deben ser miscibles entre sí.
- Colocar un fresco\(100 \: \text{mg}\) del sólido a cristalizar en un tubo de ensayo y agregar el “solvente soluble” gota a gota mientras se calienta (con un baño de vapor o baño de agua caliente, Figura 3.15a) hasta que el sólido solo se disuelva. La suspensión debe sumergirse en la fuente de calor después de cada gota, y se debe permitir algún tiempo entre adiciones para el proceso de disolución a veces lento.
- Añadir el “disolvente insoluble” gota a gota mientras se calienta hasta que la solución se vuelve débilmente turbia (Figura 3.15c).
- Agregar el “solvente soluble” gota a gota mientras se calienta hasta que la solución se aclare (transparente).
- Permita que el sistema se enfríe a temperatura ambiente (Figura 3.15e) y luego sumerja en un baño de hielo durante 10-20 minutos. Si los cristales regresan, el disolvente mixto puede funcionar para la cristalización.



