3.2: Elementos y Compuestos
- Page ID
- 55717
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
Si miras tu mano, ¿qué ves? Por supuesto, se ve piel, que consiste en células. Pero, ¿de qué están hechas las células de la piel? Como todas las células vivas, están hechas de materia. De hecho, todas las cosas están hechas de materia. La materia es cualquier cosa que ocupa espacio y tiene masa. La materia, a su vez, está conformada por sustancias químicas. Una sustancia química es una materia que tiene una composición definida y la misma composición en todo momento. Una sustancia química puede ser un elemento o un compuesto.

Elementos y átomos
Un elemento es una sustancia pura. No se puede descomponer en otro tipo de sustancias. Cada elemento está formado por un solo tipo de átomo.
Tabla Periódica de los Elementos
Hay casi 120 elementos conocidos. Como puede ver en la Tabla Periódica de los Elementos mostrados en la Figura\(\PageIndex{3}\), la mayoría de los elementos son metales. Ejemplos de metales son el hierro (Fe) y el cobre (Cu). Los metales son brillantes y buenos conductores de electricidad y calor. Los elementos no metálicos son mucho menos en número. Incluyen hidrógeno (H) y oxígeno (O). Carecen de las propiedades de los metales. El elemento más importante para la vida es el Carbono (C). Encuentra carbono en la tabla. ¿Qué tipo de elemento es, metal o no metálico?

Estructura de un átomo
Un átomo es la partícula más pequeña de un elemento que aún tiene las propiedades de ese elemento. Toda sustancia está compuesta por átomos. Los átomos son extremadamente pequeños, típicamente alrededor de una diezmil millonésima parte de un metro de diámetro. Sin embargo, los átomos no tienen límites bien definidos, como sugiere el modelo atómico que se muestra en la figura\(\PageIndex{2}\). Un átomo está compuesto por muchas partículas subatómicas. Solo discutiremos protones, neutrones y electrones.
| Partícula | Protón | Neutrón | Electron |
|---|---|---|---|
| Carga eléctrica | +1 | 0 | -1 |
| Ubicación | Núcleo | Núcleo | Fuera del núcleo |
| Masa | 1 amu | 1 amu | ~0 amu |

Si el número de protones y electrones en un átomo es igual, entonces un átomo es eléctricamente neutro porque las cargas positivas y negativas se cancelan. Si un átomo tiene más o menos electrones que protones, entonces tiene una carga general negativa o positiva, respectivamente, y se le llama ion.
Los electrones cargados negativamente de un átomo son atraídos hacia los protones cargados positivamente en el núcleo por una fuerza llamada fuerza electromagnética, por la cual se atraen cargas opuestas. La fuerza electromagnética entre protones en el núcleo hace que estas partículas subatómicas se repelan entre sí porque tienen la misma carga. Sin embargo, los protones y neutrones en el núcleo son atraídos entre sí por una fuerza diferente, llamada fuerza nuclear, que suele ser más fuerte que la fuerza electromagnética que repele los protones cargados positivamente entre sí.
Compuestos y Moléculas
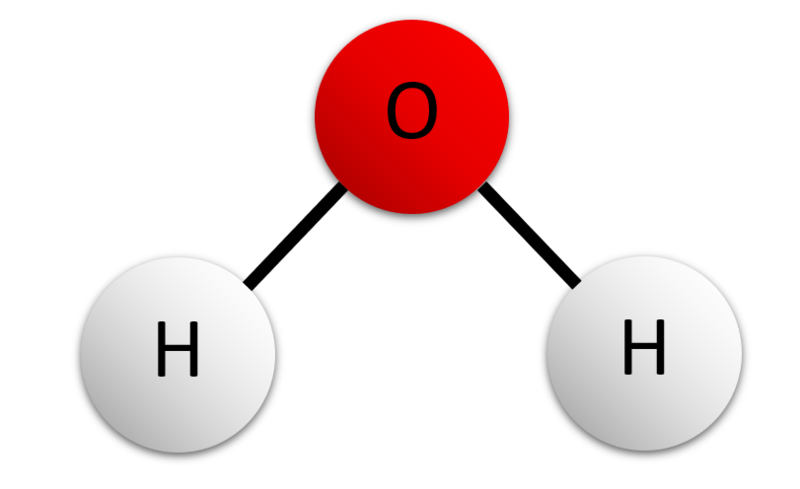
Un compuesto es una sustancia única que consiste en dos o más elementos combinados en proporciones fijas. Esto quiere decir que la composición de un compuesto es siempre la misma. La partícula más pequeña de la mayoría de los compuestos en los seres vivos se llama molécula. Considera el agua como ejemplo. Una molécula de agua siempre contiene un átomo de oxígeno y dos átomos de hidrógeno. La composición del agua se expresa mediante la fórmula química H 2 O. En la Figura se muestra un modelo de una molécula de agua\(\PageIndex{4}\). Observe que las moléculas pueden ser dibujadas de diferentes maneras, pero representan la misma molécula. En este caso, una molécula compuesta por un oxígeno y dos hidrógenos.
¿Qué causa que los átomos de una molécula de agua se “peguen”? La respuesta son los enlaces químicos. Un enlace químico es una fuerza que mantiene unidos los átomos de las moléculas. Los enlaces en las moléculas implican átomos que comparten electrones. Se forman nuevos enlaces químicos cuando las sustancias reaccionan entre sí.
Revisar
- ¿Qué es un elemento? Dar tres ejemplos.
- Definir compuesto. Explicar cómo se forman los compuestos.
- Comparar y contrastar átomos y moléculas.
- El compuesto llamado agua se puede descomponer en sus elementos constitutivos aplicándole una corriente eléctrica. ¿Qué proporción de elementos se produce en este proceso?
- Relacionar iones con elementos y átomos.
- ¿Cuál es el elemento más importante de la vida?
- El óxido de hierro a menudo se conoce como óxido, la sustancia rojiza que puede encontrar en el metal corroído. La fórmula química para este tipo de óxido de hierro es Fe2O3. Responda las siguientes preguntas sobre el óxido de hierro y explique brevemente cada respuesta.
- ¿El óxido de hierro es un elemento o un compuesto?
- ¿Una partícula de óxido de hierro sería considerada una molécula o un átomo?
- Describir la proporción relativa de átomos en el óxido de hierro.
- ¿Qué causa que el Fe y el O se peguen entre sí en óxido de hierro?
- ¿El óxido de hierro está hecho de átomos metálicos, átomos metaloides, átomos no metálicos o una combinación de alguno de estos?
- Explique por qué los iones tienen una carga positiva o negativa.
- Nombrar las tres partículas subatómicas descritas en esta sección.
Explora más
Mira el video a continuación para conocer más sobre el tamaño de un átomo.
Mira el video a continuación para conocer cuatro elementos recién descubiertos.
Atribuciones
- Diversidad y unidad por Frerieke, con licencia CC BY 2.0 vía Wikimedia Commons
- Licencia de átomo de carbono CC BY-SA 3.0 vía Ascension Glossary
- Tabla periódica por Dmarcus100, CC BY-SA 4.0 vía Wikimedia Commons
- Molécula de agua de Booyabazooka, liberada al dominio público vía Wikimedia Commons
- Texto adaptado de Biología Humana por CK-12 licenciado CC BY-NC 3.0


