6.2: El Modelo de Bohr
- Page ID
- 1846
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)habilidades para desarrollar
- Describir el Modelo de Bohr del átomo de hidrógeno.
- Usar la ecuación de Rydberg para calcular las energías de luz emitidas o absorbidas por los átomos de hidrógeno.
Siguiendo el trabajo de Ernest Rutherford y sus colegas a principios del siglo XX, la imagen de los átomos consistía en pequeños núcleos densos rodeados de electrones más ligeros y aún más pequeños que se movían continuamente alrededor del núcleo. Esta imagen se llamó el modelo planetario, porque representaba al átomo como un "sistema solar" en miniatura con los electrones orbitando el núcleo como planetas orbitando el sol. El átomo más simple es el hidrógeno, que consiste en solo un protón como el núcleo sobre el cual se mueve un solo electrón. La fuerza electrostática que atrae el electrón al protón depende solo de la distancia entre las dos partículas.
\[ F_{gravity} = G \dfrac{ m_1 m_2}{r^2} \]
con
- \(G\) es un constante gravitacional
- \(m_1\) y \(m_2\) son las masas de partícula 1 y 2, respectivamente.
- \(r\) es la distancia entre las dos partículas
La fuerza electrostática tiene la misma forma que la fuerza gravitacional entre dos partículas de masa, excepto que la fuerza electrostática depende de las magnitudes de las cargas en las partículas (+1 para el protón y -1 para el electrón) en lugar de las magnitudes de las masas de partícula que gobiernan la fuerza gravitacional.
\[ F_{electrostatic} = k \dfrac{ m_1 m_2}{r^2}\]
con
- \(k\) es un constante
- \(m_1\) y \(m_2\) son las masas de partícula 1 y 2, respectivamente.
- \(r\) es la distancia entre las dos partículas
Dado que las fuerzas se pueden derivar de potenciales, es conveniente trabajar con potenciales en su lugar, ya que son formas de energía. El potencial electrostático también se llama el potencial de Coulomb. Debido a que el potencial electrostático tiene la misma forma que el potencial gravitatorio, de acuerdo con la mecánica clásica, las ecuaciones de movimiento deberían ser similares, con el electrón moviéndose alrededor del núcleo en órbitas circulares o elípticas (de ahí la etiqueta del modelo “planetario” del átomo). Los potenciales de la forma V(r) que dependen solo de la distancia radial \(r\) se conocen como potenciales centrales. Los potenciales centrales tienen simetría esférica, por eso en lugar de especificar la posición del electrón en las coordenadas cartesianas habituales (x, y, z), es más conveniente usar coordenadas esféricas polares centradas en el núcleo, que consisten en una coordenada lineal r y dos coordenadas angulares, generalmente especificadas por las letras griegas theta (θ) y phi (Φ). Estas coordenadas son similares a las que se usan en los dispositivos de GPS y en la mayoría de los teléfonos inteligentes que rastran las posiciones en nuestra (casi) tierra esférica, con las dos coordenadas angulares especificadas por la latitud y la longitud, y la coordenada lineal especificada por la elevación del nivel del mar. Debido a la simetría esférica de los potenciales centrales, la energía y el momento angular del átomo de hidrógeno clásico son constantes, y las órbitas están obligadas a situarse en un plano como los planetas que orbitan alrededor del Sol. Sin embargo, esta descripción mecánica clásica del átomo es incompleta, porque un electrón que se mueve en una órbita elíptica se aceleraría (al cambiar de dirección) y, de acuerdo con el electromagnetismo clásico, debería emitir radiación electromagnética continuamente. Esta pérdida de energía orbital debería hacer que la órbita del electrón sea cada vez más pequeña hasta que llegue a un espiral en el núcleo, lo que implica que los átomos son inherentemente inestables.
En 1913, Niels Bohr intentó resolver la paradoja atómica ignorando la predicción del electromagnetismo clásico de que el electrón en órbita alrededor del hidrógeno emitiría luz continuamente. En cambio, se incorporó a la descripción de la mecánica clásica de las ideas de cuantización del átomo de Planck y al hallazgo de Einstein de que la luz consiste en fotones cuya energía es proporcional a su frecuencia. Bohr asumió que el electrón que orbita el núcleo normalmente no emitiría ninguna radiación (la hipótesis del estado estacionario), pero emitiría o absorbería un fotón si se moviera a una órbita diferente. La energía absorbida o emitida reflejaría diferencias en las energías orbitales de acuerdo con esta ecuación:
\[ |ΔE|=|E_f−E_i|=h\nu=\dfrac{hc}{\lambda} \label{6.3.1}\]
En esta ecuación, h es el constante de Planck y Ei y Ef son las energías orbitales inicial y final, respectivamente. Se usa el valor absoluto de la diferencia de la energía, ya que las frecuencias y las longitudes de onda siempre son positivas. En lugar de permitir valores continuos para el momento angular, la energía y el radio de la órbita, Bohr supuso que solo podrían ocurrir valores discretos para estos (en realidad, cuantificar cualquiera de estos implicaría que los otros dos también están cuantizados). La expresión de Bohr para las energías cuantificadas es:
\[E_n=−\dfrac{k}{n^2} \label{6.3.2}\]
con \(n=1,2,3, ...\)En esta expresión, \(k\) es un constante que compromete con constantes fundamentales como la masa y la carga del electrón y el constante de Planck. Insertando la expresión de las energías de órbita en la ecuación para \(ΔE\) da
o
\[ \dfrac{1}{\lambda}=\dfrac{k}{hc} \left(\dfrac{1}{n^2_1}−\dfrac{1}{n_2^2}\right) \label{6.3.4}\]
Los niveles de energía más bajos se muestran en la Figura \(\PageIndex{1}\). Una de las leyes fundamentales de la física es que la materia es más estable con la energía más baja posible. Por lo tanto, el electrón en un átomo de hidrógeno generalmente se mueve en la órbita \(n=1\), la órbita en la que tiene la energía más baja. Cuando el electrón está en esta órbita de energía más baja, se dice que el átomo está en su estado electrónico básico (o simplemente en el estado fundamental). Si el átomo acepta energía de una fuente externa, es posible que el electrón se mueva a una órbita con un valor mayor de \(n\) y que el átomo se encuentre ahora en un estado electrónico excitado (o simplemente un estado excitado) con un nivel más alto de energía. Cuando un electrón pasa de un estado excitado (órbita de mayor energía) a un estado menos excitado, o estado fundamental, la diferencia de energía se emite como un fotón. De manera similar, si un fotón es absorbido por un átomo, la energía del fotón mueve un electrón desde una órbita de energía más baja hasta una más excitada.
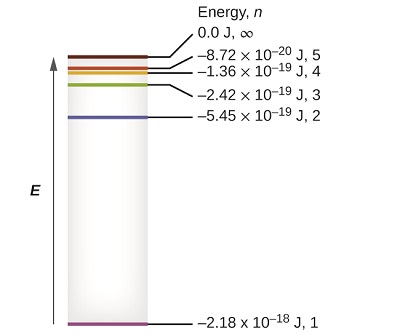
Podemos relacionar la energía de los electrones en los átomos con lo que aprendimos anteriormente sobre la energía. La ley de la conservación de la energía dice que no podemos crear ni destruir la energía. Por lo tanto, si se requiere una cierta cantidad de energía externa para excitar un electrón de un nivel de energía a otro, esa misma cantidad de energía se soltará cuando el electrón vuelva a su estado inicial (Figura \(\PageIndex{2}\)). En efecto, un átomo puede "almacenar" energía usándolo para promover un electrón a un estado con una energía más alta y soltarlo cuando el electrón vuelve a un estado más bajo. La energía se puede soltar como un cuanto de energía, a medida que el electrón regresa a su estado fundamental (por ejemplo, de \(n=5\) a \(n=1\)), o se puede soltar como dos o más cuantos a medida que el electrón cae a un estado intermedio, luego al estado fundamental (por ejemplo, de \(n=5\) a \(n=4\), emitiendo un cuanto, luego a \(n=1\), emitiendo un segundo cuanto).
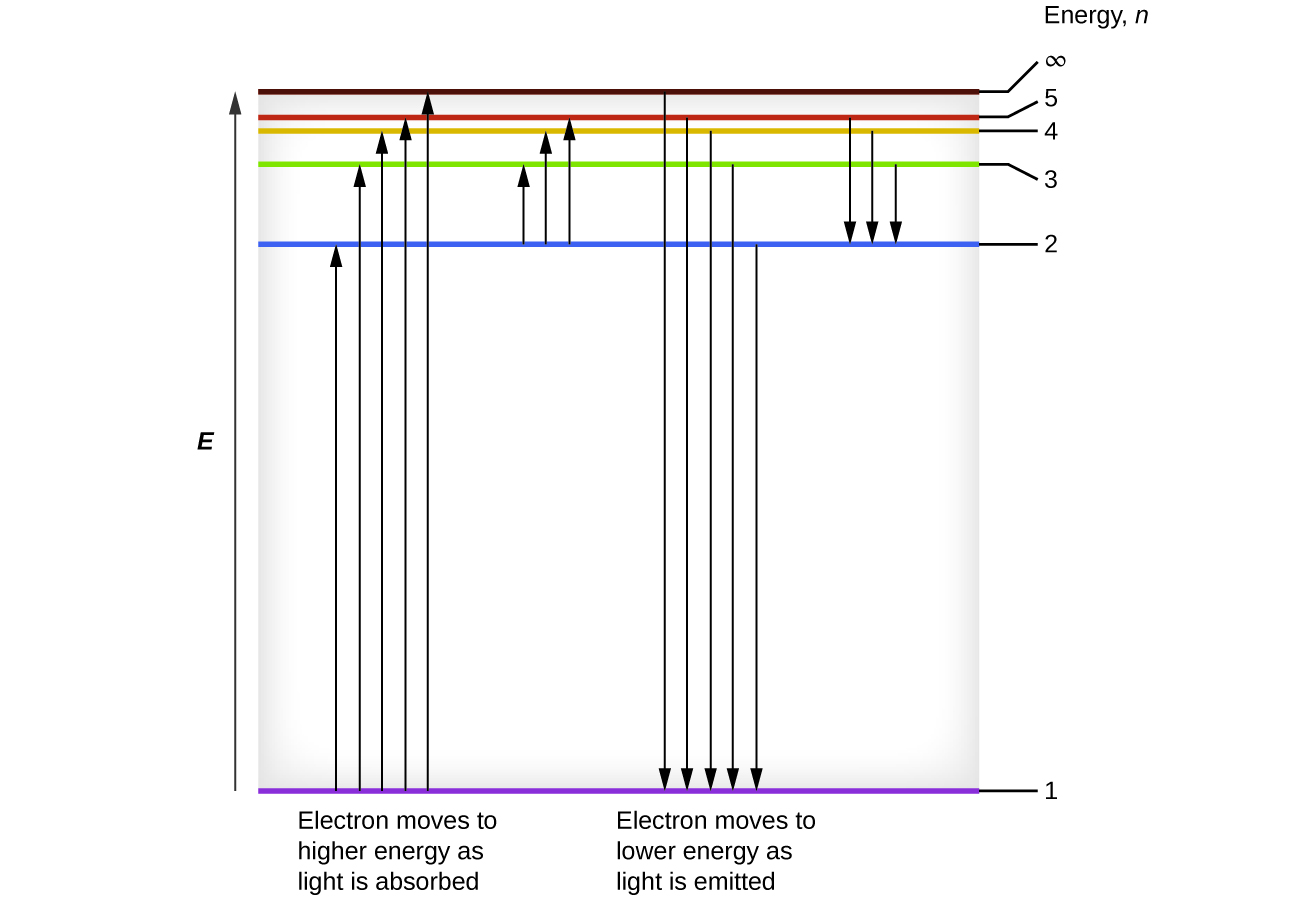
Dado que el modelo de Bohr solo involucraba un electrón, también se podría aplicar a los iones de un solo electrón He+, Li2+, Be3+, etc., que son diferente del hidrógeno solo en sus cargas nucleares, por lo que los átomos de un electrón y los iones se llaman colectivamente como átomos de hidrógeno. La expresión de energía para átomos similares al hidrógeno es una generalización de la energía del átomo de hidrógeno, donde \(Z\) es la carga nuclear (+1 para el hidrógeno, +2 para He, +3 para Li, etc.) y \(k\) tiene un valor de\(2.179 \times 10^{–18}\; J\).
\[ \color{red} E_n=−\dfrac{kZ^2}{n^2} \label{6.3.5}\]
Los tamaños de las órbitas circulares para átomos similares al hidrógeno se dan en términos de sus radios mediante la siguiente expresión, en la que \(a_o\) es un constante llamada el radio de Bohr, con un valor de \(5.292 \times 10^{−11}\; m\):
\[ \color{red} r=\dfrac{n^2}{Z} a_0 \label{6.3.6}\]
La ecuación también nos muestra que cuando aumenta la energía del electrón (a medida que aumenta \(n\), el electrón se encuentra a distancias más grande del núcleo. Esto está implicado por la dependencia inversa de \(r\) en el potencial de Coulomb, ya que, a medida que el electrón se aleja del núcleo, la atracción electrostática entre él electrón y el núcleo disminuye, y se mantiene menos apretada en el átomo. Tenga en cuenta que a medida que \(n\) aumenta de tamaño y las órbitas se hacen más grandes, sus energías se acercan a cero, por lo que los límites \(n⟶∞\) y \(r⟶∞\) implican que \(E= 0\) corresponde al límite de ionización donde el electrón se elimina completamente del núcleo. Por lo tanto, para el hidrógeno en el estado fundamental \(n=1\), la energía de ionización sería:
\[ ΔE=E_{n⟶∞} −E_1=0+k=k \label{6.3.7}\]
Con tres paradojas extremadamente desconcertantes ahora resueltas (radiación de cuerpo negro, el efecto fotoeléctrico y el átomo de hidrógeno), y todas involucrando el constante de Planck de una manera fundamental, quedó claro para la mayoría de los físicos en ese momento que las teorías clásicas que funcionaron tan bien en el mundo macroscópico tenían fallas fundamentales y no se podía extender hasta el dominio microscópico de los átomos y las moléculas. Desafortunadamente, a pesar del notable logro de Bohr al derivar una expresión teórica para el constante de Rydberg, fue incapaz de extender su teoría al siguiente átomo más simple, He, que solo tiene dos electrones. El modelo de Bohr tenía fallas severas, ya que aún se basaba en la noción de órbitas precisas de la mecánica clásica, un concepto que más tarde se descubrió como insostenible en el dominio microscópico, cuando se desarrolló un modelo adecuado de mecánica cuántica para reemplazar a la mecánica clásica.
Ejemplo \(\PageIndex{1}\): CÁLCULO DE LA ENERGÍA DE UN ELECTRÓN EN UNA ÓRBITA de BOHR
Los primeros investigadores estaban muy emocionados cuando pudieron predecir la energía de un electrón a una distancia particular del núcleo en un átomo de hidrógeno. Si una chispa promueve el electrón en un átomo de hidrógeno en una órbita con \(n=3\), ¿Cuál es la energía calculada, en julios, del electrón?
Solución
La energía del electrón está dada por la Ecuación \(\ref{6.3.5}\):
\[ E=\dfrac{−kZ^2}{n^2}\]
El número atómico, \(Z\), de hidrógeno es 1; \(k=2.179\ veces 10^{-18}\;J\); y el electrón se caracteriza por un valor n de \(3\). Así,
\[E=\dfrac{−(2.179 \times 10^{−18}\;J)×(1)^2}{(3)^2}=−2.421 \times 10^{−19}\;J\]
Ejercicio \(\PageIndex{1}\)
El electrón en el Ejemplo \(\PageIndex{1}\) en el estado \(n=3\) se promueve aún más a una órbita con \(n=6\). ¿Cuál es su nueva energía?
- Respuesta
-
TBD
Ejemplo \(\PageIndex{2}\): CÁLCULO DE LAS TRANSICIONES ELECTRÓNICAS EN UN SISTEMA DE UN ELECTRÓN
¿Cuál es la energía (en julios) y la longitud de la onda (en metros) de la línea en el espectro del hidrógeno que representa el movimiento de un electrón desde la órbita de Bohr con n = 4 a la órbita con n = 6? ¿En qué parte del espectro electromagnético encontramos esta radiación?
Solución
En este caso, el electrón comienza con \(n=4\), entonces \(n_1=4\). Viene a descansar en la órbita \(n=6\), entonces \(n_2=6\). La diferencia de energía entre los dos estados se da por esta expresión:
\[ΔE=E_1−E_2=2.179 \times 10^{−18}\left(\dfrac{1}{n^2_1}−\dfrac{1}{n_2^2}\right)\]
\[ΔE=2.179 \times 10^{−18} \left(\dfrac{1}{4^2}−\dfrac{1}{6^2}\right)\; J\]
\[ΔE=2.179 \times 10^{−18} \left(\dfrac{1}{16}−\dfrac{1}{36}\right)\;J\]
\[ΔE=7.566 \times 10^{−20}\;J\]
Esta diferencia de energía es positiva, lo que indica que un fotón ingresa al sistema (se absorbe) para excitar el electrón desde la órbita n = 4 hasta la órbita \(n=6\). La longitud de onda de un fotón con esta energía se encuentra en la expresión \(E=hc\lambda\). El reordenamiento da:
\[ \lambda=\dfrac{hc}{E}\]
De la figura de la radiación electromagnética, podemos ver que esta longitud de onda se encuentra en la porción infrarroja del espectro electromagnético.
Ejercicio \(\PageIndex{2}\)
¿Cuál es la energía en julios y la longitud de la onda en metros del fotón producido cuando un electrón cae desde \(n=5\) al nivel \(n=3\) en un ión (He^+\) (\(Z= 2\) para \(He^+\))?
- Respuesta
-
\(6.198 \times 10^{–19}\; J\) and \(3.205 \times 10^{−7}\; m\)
El modelo de Bohr del átomo de hidrógeno da información sobre el comportamiento de la materia a nivel microscópico, pero no tiene en cuenta las interacciones electrón-electrón en los átomos con más de un electrón. Introduce varias características importantes de todos los modelos utilizados para describir la distribución de electrones en un átomo. Estas características incluyen lo siguiente:
- Las energías de los electrones (niveles de energía) en un átomo se cuantifican, se describen mediante números cuánticos: números enteros que tienen solo un valor permitido específico y se usan para caracterizar la disposición de los electrones en un átomo.
- La energía de un electrón aumenta al aumentar la distancia del núcleo.
- Las energías discretas (líneas) en los espectros de los elementos resultan de energías electrónicas cuantificadas.
De estas características, la más importante es el postulado de los niveles de energía cuantificados para un electrón en un átomo. Como consecuencia, el modelo sentó las bases para el modelo mecánico cuántico del átomo. Bohr ganó un Premio Nobel de Física por sus contribuciones a nuestra comprensión de la estructura de los átomos y cómo esto se relaciona con las emisiones de los espectros de línea
Resumen
Bohr incorporó las ideas de cuantización de Planck y Einstein en un modelo del átomo de hidrógeno que resolvió la paradoja de la estabilidad del átomo y los espectros discretos. El modelo de Bohr del átomo de hidrógeno explica la conexión entre la cuantificación de los fotones y la emisión cuantificada de los átomos. Bohr describió el átomo de hidrógeno en términos de un electrón que se mueve en una órbita circular alrededor de un núcleo. Él postuló que el electrón estaba restringido a ciertas órbitas caracterizadas por energías discretas. Las transiciones entre estas órbitas permitidas resultan en la absorción o emisión de fotones. Cuando un electrón se mueve de una órbita de mayor energía a una más estable, la energía se emite en forma de un fotón. Para mover un electrón de una órbita estable a una más excitada, se debe absorber un fotón de energía. Usando el modelo de Bohr, podemos calcular la energía de un electrón y el radio de su órbita en cualquier sistema de un electrón.
Glosario
- El modelo de Bohr del átomo de hidrógeno
- Modelo estructural en el que un electrón se mueve alrededor del núcleo solo en órbitas circulares, cada una con un radio permitido específico; el electrón en órbita normalmente no emite radiación electromagnética, pero lo hace al cambiar de una órbita a otra.
- estado excitado
- Estado que tiene una energía mayor que la energía del estado fundamental.
- estado fundamental
- Estado en el que los electrones en un átomo, ion o molécula tienen la menor energía posible.
- número cuántico
- Número entero que tiene solo valores permitidos específicos y se utiliza para caracterizar la disposición de los electrones en un átomo.
Contribuyentes
- Template:ContribOpenStaxSpanishSpanish
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


