16.2: La entropía
- Page ID
- 1925
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\( \newcommand{\dsum}{\displaystyle\sum\limits} \)
\( \newcommand{\dint}{\displaystyle\int\limits} \)
\( \newcommand{\dlim}{\displaystyle\lim\limits} \)
\( \newcommand{\id}{\mathrm{id}}\) \( \newcommand{\Span}{\mathrm{span}}\)
( \newcommand{\kernel}{\mathrm{null}\,}\) \( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\) \( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\) \( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\id}{\mathrm{id}}\)
\( \newcommand{\Span}{\mathrm{span}}\)
\( \newcommand{\kernel}{\mathrm{null}\,}\)
\( \newcommand{\range}{\mathrm{range}\,}\)
\( \newcommand{\RealPart}{\mathrm{Re}}\)
\( \newcommand{\ImaginaryPart}{\mathrm{Im}}\)
\( \newcommand{\Argument}{\mathrm{Arg}}\)
\( \newcommand{\norm}[1]{\| #1 \|}\)
\( \newcommand{\inner}[2]{\langle #1, #2 \rangle}\)
\( \newcommand{\Span}{\mathrm{span}}\) \( \newcommand{\AA}{\unicode[.8,0]{x212B}}\)
\( \newcommand{\vectorA}[1]{\vec{#1}} % arrow\)
\( \newcommand{\vectorAt}[1]{\vec{\text{#1}}} % arrow\)
\( \newcommand{\vectorB}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vectorC}[1]{\textbf{#1}} \)
\( \newcommand{\vectorD}[1]{\overrightarrow{#1}} \)
\( \newcommand{\vectorDt}[1]{\overrightarrow{\text{#1}}} \)
\( \newcommand{\vectE}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash{\mathbf {#1}}}} \)
\( \newcommand{\vecs}[1]{\overset { \scriptstyle \rightharpoonup} {\mathbf{#1}} } \)
\( \newcommand{\vecd}[1]{\overset{-\!-\!\rightharpoonup}{\vphantom{a}\smash {#1}}} \)
\(\newcommand{\avec}{\mathbf a}\) \(\newcommand{\bvec}{\mathbf b}\) \(\newcommand{\cvec}{\mathbf c}\) \(\newcommand{\dvec}{\mathbf d}\) \(\newcommand{\dtil}{\widetilde{\mathbf d}}\) \(\newcommand{\evec}{\mathbf e}\) \(\newcommand{\fvec}{\mathbf f}\) \(\newcommand{\nvec}{\mathbf n}\) \(\newcommand{\pvec}{\mathbf p}\) \(\newcommand{\qvec}{\mathbf q}\) \(\newcommand{\svec}{\mathbf s}\) \(\newcommand{\tvec}{\mathbf t}\) \(\newcommand{\uvec}{\mathbf u}\) \(\newcommand{\vvec}{\mathbf v}\) \(\newcommand{\wvec}{\mathbf w}\) \(\newcommand{\xvec}{\mathbf x}\) \(\newcommand{\yvec}{\mathbf y}\) \(\newcommand{\zvec}{\mathbf z}\) \(\newcommand{\rvec}{\mathbf r}\) \(\newcommand{\mvec}{\mathbf m}\) \(\newcommand{\zerovec}{\mathbf 0}\) \(\newcommand{\onevec}{\mathbf 1}\) \(\newcommand{\real}{\mathbb R}\) \(\newcommand{\twovec}[2]{\left[\begin{array}{r}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\ctwovec}[2]{\left[\begin{array}{c}#1 \\ #2 \end{array}\right]}\) \(\newcommand{\threevec}[3]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\cthreevec}[3]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \end{array}\right]}\) \(\newcommand{\fourvec}[4]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\cfourvec}[4]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \end{array}\right]}\) \(\newcommand{\fivevec}[5]{\left[\begin{array}{r}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\cfivevec}[5]{\left[\begin{array}{c}#1 \\ #2 \\ #3 \\ #4 \\ #5 \\ \end{array}\right]}\) \(\newcommand{\mattwo}[4]{\left[\begin{array}{rr}#1 \amp #2 \\ #3 \amp #4 \\ \end{array}\right]}\) \(\newcommand{\laspan}[1]{\text{Span}\{#1\}}\) \(\newcommand{\bcal}{\cal B}\) \(\newcommand{\ccal}{\cal C}\) \(\newcommand{\scal}{\cal S}\) \(\newcommand{\wcal}{\cal W}\) \(\newcommand{\ecal}{\cal E}\) \(\newcommand{\coords}[2]{\left\{#1\right\}_{#2}}\) \(\newcommand{\gray}[1]{\color{gray}{#1}}\) \(\newcommand{\lgray}[1]{\color{lightgray}{#1}}\) \(\newcommand{\rank}{\operatorname{rank}}\) \(\newcommand{\row}{\text{Row}}\) \(\newcommand{\col}{\text{Col}}\) \(\renewcommand{\row}{\text{Row}}\) \(\newcommand{\nul}{\text{Nul}}\) \(\newcommand{\var}{\text{Var}}\) \(\newcommand{\corr}{\text{corr}}\) \(\newcommand{\len}[1]{\left|#1\right|}\) \(\newcommand{\bbar}{\overline{\bvec}}\) \(\newcommand{\bhat}{\widehat{\bvec}}\) \(\newcommand{\bperp}{\bvec^\perp}\) \(\newcommand{\xhat}{\widehat{\xvec}}\) \(\newcommand{\vhat}{\widehat{\vvec}}\) \(\newcommand{\uhat}{\widehat{\uvec}}\) \(\newcommand{\what}{\widehat{\wvec}}\) \(\newcommand{\Sighat}{\widehat{\Sigma}}\) \(\newcommand{\lt}{<}\) \(\newcommand{\gt}{>}\) \(\newcommand{\amp}{&}\) \(\definecolor{fillinmathshade}{gray}{0.9}\)Habilidades para desarrolar
- Definir entropía
- Explicar la relación entre la entropía y el número de microestados.
- Predecir el signo del cambio de entropía para los procesos químicos y físicos
En 1824, a la edad de 28 años, Nicolas Léonard Sadi Carnot (Figura \(\PageIndex{2}\)) publicó los resultados de un extenso estudio sobre la eficiencia de las máquinas térmicas de vapor. En una revisión posterior de los hallazgos de Carnot, Rudolf Clausius introdujo una nueva propiedad termodinámica que relaciona el flujo de calor espontáneo que acompaña a un proceso con la temperatura a la que pasa el proceso. Esta nueva propiedad se expresó como la relación entre el calor reversible (qrev) y la temperatura kelvin (T). El término proceso reversible se refiere a un proceso que pasa tan lentamente que siempre está en equilibrio y su dirección se puede cambiar (se puede "revertir") mediante un cambio infinitesimalmente pequeño en alguna condición. Tenga en cuenta que la idea de un proceso reversible es un formalismo necesario para apoyar el desarrollo de varios conceptos termodinámicos; ningún proceso real es verdaderamente reversible, sino que se clasifica como irreversible.

De manera similar a otras propiedades termodinámicas, esta nueva cantidad es una función de estado, por eso su cambio depende solo de los estados inicial y final de un sistema. En 1865, Clausius llamo esta propiedad la entropía (S) y definió su cambio para cualquier proceso de la siguiente manera
\[ΔS=\dfrac{q_\ce{rev}}{T} \label{Eq1}\]
El cambio de entropía para un proceso real e irreversible es entonces igual al del proceso teórico reversible que involucra los mismos estados iniciales y finales.
La entropía y los microestados
Después del trabajo de Carnot y Clausius, Ludwig Boltzmann desarrolló un modelo estadístico a escala molecular que relacionaba la entropía de un sistema con el número de microestados posibles para el sistema. Un microestado (\(\Omega\)) es una configuración específica de las ubicaciones y energías de los átomos o moléculas que componen un sistema como el siguiente:
\[S=k \ln \Omega \label{Eq2}\]
Aquí k es la constante de Boltzmann y tiene un valor de \(1.38 \times 10^{−23}\, J/K\).
En cuanto a otras funciones de estado, el cambio en la entropía de un proceso es la diferencia entre sus valores finales (Sf) e iniciales (Si):
\[\begin{align} ΔS &=S_\ce{f}−S_\ce{i} \nonumber \\[5pt] &=k \ln \Omega_\ce{f} − k \ln \Omega_\ce{i} \nonumber \\[5pt] &=k \ln\dfrac{\Omega_\ce{f}}{\Omega_\ce{i}} \label{Eq2a} \end{align}\]
Para procesos que involucran un aumento en el número de microestados del sistema, \(\Omega_f> \Omega_i\), la entropía del sistema aumenta, \(ΔS>0\). Por el contrario, los procesos que reducen el número de microestados en el sistema, \(\Omega_f<\Omega_i\), producen una disminución en la entropía del sistema, \(ΔS<0\). Esta interpretación de la entropía a escala molecular nos da un vínculo con la probabilidad de que ocurra un proceso, como se ilustra en los siguientes párrafos.
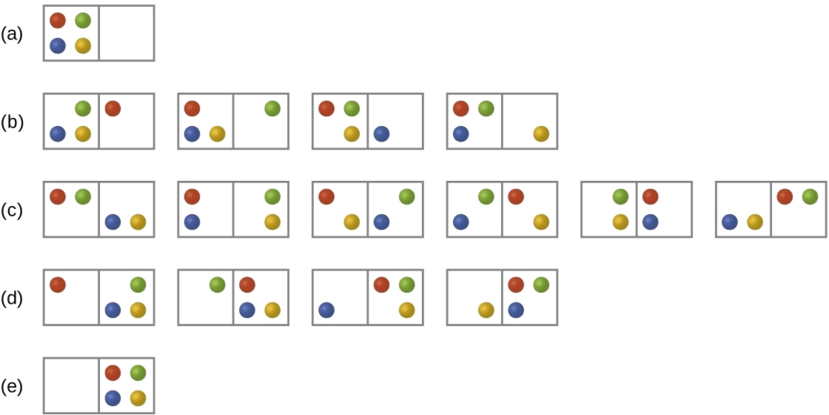
Considere el caso general de un sistema compuesto por N partículas distribuidas entre n cajas. El número de microestados posibles para tal sistema es nN. Por ejemplo, distribuir cuatro partículas entre dos cajas dará como resultado 24 = 16 microestados diferentes como se ilustra en la Figura \(\PageIndex{2}\). Los microestados con disposiciones de partículas equivalentes (sin considerar las identidades de partículas individuales) se agrupan y se llaman distribuciones (a veces llamadas macroestados o configuraciones). La probabilidad de que exista un sistema con sus componentes en una distribución dada es proporcional al número de microestados dentro de la distribución. Dado que la entropía aumenta logarítmicamente con el número de microestados, la distribución más probable es, por tanto, la de mayor entropía.
Para este sistema, la configuración más probable es uno de los seis microestados asociados con la distribución (c) donde las partículas se distribuyen uniformemente entre las cajas, es decir, una configuración de dos partículas en cada caja. La probabilidad de encontrar el sistema en esta configuración es
\[\dfrac{6}{16} = \dfrac{3}{8}\]
La configuración menos probable del sistema es la que tiene cuatro partículas en una caja, correspondientes a las distribuciones (a) y (d), cada una con una probabilidad de
\[\dfrac{1}{16}\]
La probabilidad de encontrar todas las partículas en un solo cuadro (ya sea el cuadro de la izquierda o el cuadro de la derecha) es entonces
\[\left(\dfrac{1}{16}+\dfrac{1}{16}\right)=\dfrac{2}{16} = \dfrac{1}{8}\]
A medida que se agregan más partículas al sistema, el número de microestados posibles aumenta exponencialmente (2N). Un sistema macroscópico (del tamaño de un laboratorio) consistiría típicamente en moles de partículas (N ~ 1023), y el número correspondiente de microestados sería enorme. Sin embargo, independientemente del número de partículas en el sistema, las distribuciones en las que se encuentran aproximadamente el mismo número de partículas en cada caja son siempre las configuraciones más probables.
La distribución más probable es, por tanto, la de mayor entropía.
La descripción anterior de un gas ideal que se expande hacia el vacío es un ejemplo macroscópico de este modelo de partículas en una caja. Para este sistema, se confirma que la distribución más probable es aquella en la que la materia se dispersa o distribuye más uniformemente entre los dos matraces. El proceso espontáneo por el cual el gas contenido inicialmente en un matraz se expande para llenar ambos matraces por igual, por lo tanto, aumenta la entropía del sistema.
Se puede usar un enfoque similar para describir el flujo espontáneo de calor. Considere un sistema que consta de dos objetos y cada uno contiene dos partículas y dos unidades de energía (representadas como "*") en la Figura \(\PageIndex{3}\). El objeto caliente está compuesto por partículas A y B e inicialmente contiene ambas unidades de energía. El objeto frío está compuesto por partículas C y D, que inicialmente no tiene unidades de energía. La distribución (a) muestra los tres microestados posibles para el estado inicial del sistema, con ambas unidades de energía contenidas dentro del objeto caliente. Si se transfiere una de las dos unidades de energía, el resultado es la distribución (b) que consta de cuatro microestados. Si se transfieren ambas unidades de energía, el resultado es la distribución (c) que consta de tres microestados. Y entonces, podemos describir este sistema por un total de diez microestados. La probabilidad de que el calor no fluya cuando los dos objetos entran en contacto, es decir, que el sistema permanezca en la distribución (a), es \(\frac{3}{10}\). Es más probable que el flujo de calor produzca una de las otras dos distribuciones, siendo la probabilidad combinada \(\frac{7}{10}\). El resultado más probable es el flujo de calor para producir la dispersión uniforme de energía representada por la distribución (b), siendo la probabilidad de esta configuración \(\frac{4}{10}\). En el ejemplo anterior de dispersión de materia, la extrapolación de este tratamiento a colecciones macroscópicas de partículas aumenta drásticamente la probabilidad de una distribución uniforme en relación con las otras distribuciones. Esto apoya la observación común de que colocar objetos fríos y calientes en contacto da como resultado un flujo de calor espontáneo que finalmente iguala las temperaturas de los dos objetos. Y, nuevamente, este proceso espontáneo también se caracteriza por un aumento en la entropía del sistema.
Ejemplo \(\PageIndex{1}\): La determinación de ΔS
Considere el sistema que se muestra aquí. ¿Cuál es el cambio en la entropía para un proceso que convierte el sistema de distribución de (a) a (c)?

Solución
Estamos interesados en el siguiente cambio:
El número inicial de microestados es uno, los últimos seis:
\[\begin{align} ΔS &=k \ln\dfrac{\Omega_\ce{c}}{\Omega_\ce{a}} \nonumber \\[5pt] &= 1.38×10^{−23}\:J/K × \ln\dfrac{6}{1} \nonumber \\[5pt] &= 2.47×10^{−23}\:J/K \nonumber \end{align} \nonumber \]
El signo de este resultado es consistente con la expectativa; dado que hay más microestados posibles para el estado final que para el estado inicial, el cambio en la entropía debería ser positivo.
Ejercicio \(\PageIndex{1}\)
Considere el sistema que se muestra en la Figura \(\PageIndex{3}\). ¿Cuál es el cambio en la entropía para el proceso en el que toda la energía se transfiere del objeto caliente (AB) al objeto frío (CD)?
- Respuesta
-
0 J/K
Prediciendo el signo de ΔS
Las relaciones entre la entropía, los microestados y la dispersión de la materia/energía descritas anteriormente nos permiten hacer generalizaciones sobre las entropías relativas de sustancias y predecir el signo de cambios de entropía para procesos químicos y físicos. Considere los cambios de fase ilustrados en la Figura \(\PageIndex{4}\). En la fase sólida, los átomos o moléculas están restringidos a posiciones casi fijas entre sí y solo son capaces de oscilaciones modestas alrededor de estas posiciones. Con ubicaciones esencialmente fijas para las partículas componentes del sistema, el número de microestados es relativamente pequeño. En la fase líquida, los átomos o moléculas se pueden mover libremente unos sobre otros, aunque permanecen relativamente cerca unos de otros. Esta libertad de movimiento da como resultado una mayor variación en las posibles ubicaciones de las partículas, por lo que el número de microestados es correspondientemente mayor que para el sólido. Como resultado, Sliquid> Ssolid y el proceso de convertir una sustancia de sólido a líquido (fusión) se caracteriza por un aumento en la entropía, ΔS>0. Por la misma lógica, el proceso recíproco (congelación) exhibe una disminución en la entropía, ΔS <0.
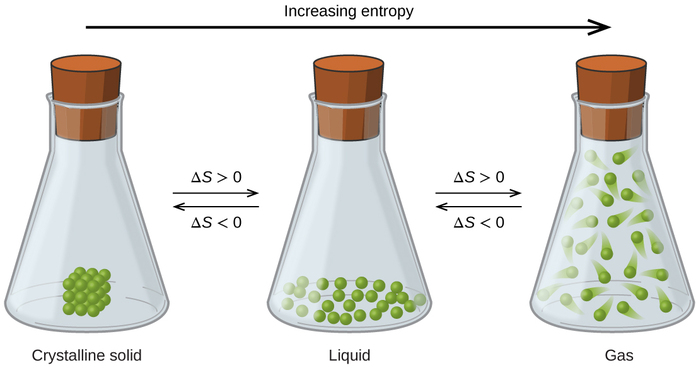
Ahora considere la fase del vapor o el gas. Los átomos o moléculas ocupan un volumen mucho más grande que en la fase líquida; por lo tanto, cada átomo o molécula se puede encontrar en muchas más ubicaciones que en la fase líquida (o sólida). En consecuencia, para cualquier sustancia, Sgas> Sliquid> Ssolid, y los procesos de vaporización y sublimación también involucran aumentos de entropía, ΔS> 0. Igualmente, las transiciones de fase recíprocas, condensación y deposición, involucran la disminucione de entropía, ΔS <0.
Según la teoría cinético-molecular, la temperatura de una sustancia es proporcional a la energía cinética promedio de sus partículas. El aumento de la temperatura de una sustancia dará como resultado vibraciones más extensas de las partículas en sólidos y traslaciones más rápidas de las partículas en líquidos y gases. A temperaturas más altas, la distribución de energías cinéticas entre los átomos o moléculas de la sustancia también es más extensa (más dispersa) que a temperaturas más bajas. Por tanto, la entropía de cualquier sustancia aumenta con la temperatura (Figura \(\PageIndex{5}\)).

La entropía de una sustancia está afectada por la estructura de las partículas (átomos o moléculas) que componen la sustancia. Con respecto a las sustancias atómicas, los átomos más pesados poseen mayor entropía a una temperatura dada que los átomos menos pesados, lo cual es una consecuencia de la relación entre la masa de una partícula y el espaciamiento de los niveles de energía traslacional cuantificados (que es un tema más allá del alcance de este capítulo). En el caso de las moléculas, un mayor número de átomos (independientemente de su masa) aumenta la forma en que las moléculas pueden vibrar y, por tanto, el número de posibles microestados y la entropía del sistema.
Finalmente, las variaciones en los tipos de partículas afectan la entropía de un sistema. En comparación con una sustancia pura, en la que todas las partículas son idénticas, la entropía de una mezcla de dos o más tipos de partículas diferentes es más grande. Esto se debe a las orientaciones e interacciones adicionales que son posibles en un sistema compuesto por componentes no idénticos. Por ejemplo, cuando un sólido se disuelve en un líquido, las partículas del sólido experimentan tanto una mayor libertad de movimiento como interacciones adicionales con las partículas de disolvente. Esto corresponde a una dispersión más uniforme de materia y energía y un número más grande de microestados. Por tanto, el proceso de disolución involucra un aumento en la entropía, ΔS> 0.
Considerar los factores diversos que afectan la entropía nos permite hacer predicciones informadas del signo de ΔS para varios procesos químicos y físicos como se ilustra en el Ejemplo \(\PageIndex{2}\).
Ejemplo \(\PageIndex{2}\): Prediciendo el signo de ∆S
Predecir el signo del cambio de entropía para los siguientes procesos. Indique la razón por cada una de sus predicciones.
- Un mol de agua líquida a temperatura ambiente \ (⟶ \) un mol de agua líquida a 50 °C
- \(\ce{Ag+}(aq)+\ce{Cl-}(aq)⟶\ce{AgCl}(s)\)
- \(\ce{C6H6}(l)+\dfrac{15}{2}\ce{O2}(g)⟶\ce{6CO2}(g)+\ce{3H2O}(l)\)
- \(\ce{NH3}(s)⟶\ce{NH3}(l)\)
Solución
- positivo, la temperatura aumenta
- negativo, reducción del número de iones (partículas) en solución, disminución de la dispersión de materia
- disminución neta de la cantidad de especies gaseosas
- positiva, transición de fase de sólido a líquido, aumento neto de la dispersión de materia
Ejercicio \(\PageIndex{2}\)
Predecir el signo del cambio de entropía para los siguientes procesos. Indique la razón por cada una de sus predicciones.
- \(\ce{NaNO3}(s)⟶\ce{Na+}(aq)+\ce{NO3-}(aq)\)
- the freezing of liquid water
- \(\ce{CO2}(s)⟶\ce{CO2}(g)\)
- \(\ce{CaCO}(s)⟶\ce{CaO}(s)+\ce{CO2}(g)\)
- Respuesta a
-
Positivo; El sólido se disuelve para dar un aumento de iones móviles en la solución.
- Respuesta b
-
Negativo; El líquido se vuelve en un sólido más ordenado.
- Respuesta c
-
Positivo; El sólido relativamente ordenado se convierte en un gas
- Respuesta d
-
Positivo; Hay una producción neta de un mol de gas.
Resumen
La entropía (\(S\)) es una función de estado que se puede relacionar con el número de microestados de un sistema (el número de formas en que se puede organizar el sistema) y con la relación entre el calor reversible y la temperatura kelvin. Se puede interpretar como una medida de la dispersión o distribución de materia y / o energía en un sistema, y a veces se describe como una representación del "desorden" del sistema. Para una sustancia dada, \(S_{sólido} <S_ {líquido}\ llS_{gas}\) en un estado físico dado a una temperatura dada, la entropía es típicamente más grande para átomos más pesados o moléculas más complejas. La entropía aumenta cuando se calienta un sistema y cuando se forman soluciones. Usando estas pautas, el signo de cambios de entropía para algunas reacciones químicas se puede predecir de manera confiable.
Ecuaciones Clave
- \(ΔS=\dfrac{q_\ce{rev}}{T}\)
- S = k ln W
- \(ΔS=k\ln\dfrac{W_\ce{f}}{W_\ce{i}}\)
Glosario
- entropía (S)
- Función de estado que es una medida de la dispersión de materia y / o energía dentro de un sistema, determinada por el número de microestados del sistema que a veces se describen como una medida del desorden del sistema.
- microestado (W)
- posible configuración o disposición de materia y energía dentro de un sistema
- proceso reversible
- proceso que pasa tan lentamente como para ser capaz de invertir la dirección en respuesta a un cambio infinitesimalmente pequeño en las condiciones; construcción hipotética que sólo se puede aproximar mediante procesos reales eliminados
Contribuyentes
Paul Flowers (Universidad de Carolina del Norte - Pembroke), Klaus Theopold (Universidad de Delaware) y Richard Langley (Stephen F. Austin Universidad del Estado) con autores contribuyentes. Contenido del libro de texto producido por la Universidad de OpenStax tiene licencia de Atribución de Creative Commons Licencia 4.0 licencia. Descarge gratis en http://cnx.org/contents/85abf193-2bd...a7ac8df6@9.110)."
Ana Martinez (amartinez02@saintmarys.edu) contribuyó a la traducción de este texto.


