14.2.3: Inserción migratoria-1,2-inserciones
- Page ID
- 81649
Las inserciones de\(\pi\) sistemas en enlaces M-X son atractivas en el sentido de que establecen dos nuevos\(\sigma\) enlaces en un solo paso, de manera estereocontrolada. Como vimos en el último post, sin embargo, debemos tener cuidado de distinguir estas inserciones migratorias completamente intramoleculares del ataque intermolecular de un nucleófilo o electrófilo sobre un ligando\(\pi\) de sistema coordinado. La reacción inversa de inserción migratoria,\(\beta\) -eliminación, no es lo mismo que la inversa del ataque nucleofílico o electrófilo a un\(\pi\) sistema coordinado.

Al igual que 1,1-inserciones, 1,2-inserciones generan un sitio vacante en el metal, que generalmente se llena con ligando externo. Para los alquenos asimétricos, es importante pensar en la selectividad del sitio: ¿qué átomo del alqueno terminará unido al metal y cuál al otro ligando? Para hacer predicciones sobre la selectividad del sitio podemos apelar a la imagen clásica del enlace M—X como M + X —. \(\pi\)Los ligandos asimétricos polarizados contienen un átomo con exceso de carga parcial; este átomo se engancha con el átomo complementario en el enlace M-R durante la inserción. ¡Resonancia es nuestro mejor amigo aquí!

Un buen estudio de Yu y Spencer ilustra estos efectos en reacciones homogéneas de hidrogenación catalizadas por paladio y rodio. Los alquenos inactivados generalmente presentan menor selectividad de sitio que los activados, aunque las diferencias estéricas entre los dos extremos del doble enlace pueden promover la selectividad.
Tendencias de reactividad en 1,2-inserciones
La termodinámica de 1,2-inserciones de alquenos depende fuertemente del alqueno, pero podemos obtener una gran comprensión al examinar la estructura del producto alquilo. Los alquenos coordinados que dan fuertes enlaces metal-alquilo después de la inserción migratoria tienden a someterse al proceso. Por lo tanto, los grupos aceptores de electrones, como los carbonilos y los átomos de flúor, tienden a fomentar la inserción migratoria; recuerde que los complejos alquílicos que llevan estos grupos tienden a tener enlaces M—C estables.
Las inserciones de alquenos tanto en M—H como en M—R (R = alquilo) se ven favorecidas termodinámicamente, pero la cinética de inserción de M—R es mucho más lenta. Esta observación refleja una tendencia generalizada en la química organometálica: los enlaces M—H reaccionan más rápidamente que los enlaces M—R. Lo mismo es cierto de lo contrario,\(\beta\) -eliminación. Incluso en los casos en que tanto la eliminación de hidruro como de alquilo se ven favorecidas termodinámicamente, la eliminación de\(\beta\) hidruro es mucho más rápida. Aunque la inserción en M-R es relativamente lenta, esta etapa elemental es crítica para las polimerizaciones de olefinas que forman polialquenos (polimerización Ziegler-Natta). ¡Esta reacción merece un post propio!
A medida que aumenta la fuerza del enlace M-X, disminuye la probabilidad de que un\(\pi\) ligando de tipo L se inserte en el enlace. Por lo tanto, mientras que las inserciones en M—H y M-C son relativamente comunes, las inserciones en los enlaces M—N y M—O son más raras. Se sabe que los lantánidos y el paladio promueven la inserción en M—N en algunos casos, pero los productos con conectividad idéntica pueden provenir del ataque externo de nitrógeno sobre un\(\pi\) ligando coordinado. La diastereoselectividad de estas reacciones proporciona una visión mecanicista, ya que la inserción migratoria es syn (ver abajo), se espera una relación syn entre Pd y N en los productos de inserción migratoria. Una relación anti indica ataque externo por nitrógeno u oxígeno.
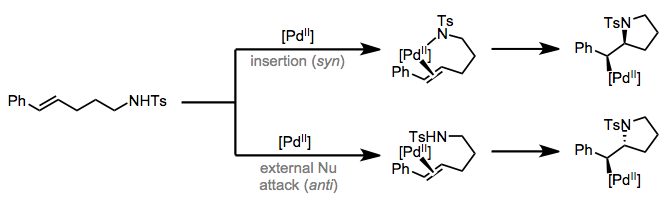
Estereoquímica de 1,2-inserciones
1,2-Inserción puede establecer dos estereocentros a la vez, por lo que la estereoquímica del proceso es crítica! Además, las 1,2-inserciones y\(\beta\) eliminaciones están unidas por importantes requisitos estereoelectrónicos. Se puede hacer una analogía con la eliminación E2 de la química orgánica, que también tiene estrictas demandas estereoelectrónicas. Para que continúe la inserción migratoria, el alqueno y el ligando tipo X deben ser sincoplanarios durante la inserción; como consecuencia de este alineamiento, X y MLn terminan en la misma cara del alqueno después de la inserción. En otras palabras, las inserciones en alquenos tienen lugar de manera syn. Los complejos que tienen dificultades para lograr una disposición coplanar de C=C y M—X se insertan muy lentamente, si es que lo hacen.
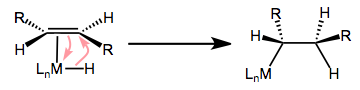
(Michael Evans)
Esta observación tiene implicaciones importantes para\(\beta\) -eliminación, también- la eliminación de X y el metal debe tener la capacidad de alinear syn.
Inserciones de Otros\(\pi\) Sistemas
Para cerrar esta publicación, examinemos brevemente las inserciones en\(\pi\) ligandos distintos a los alquenos. Las inserciones de alquinos en enlaces metal-hidruro son conocidas y a veces están involucradas en reacciones a las que me refiero colectivamente como “hidrorellenilación”: hidrosililación, hidroesterificación, hidrogenación y otras adiciones netas de H-X a través del\(\pi\) enlace. Curiosamente, algunas inserciones de alquinos producen productos trans, aunque los productos cis se esperan de la adición syn de M—X; los mecanismos de estos procesos implican la adición inicial de syn seguida de isomerización al complejo trans a través de una interesante forma de resonancia. El complejo cis es el producto cinético, pero con el tiempo se isomeriza al complejo trans más termodinámicamente estable.
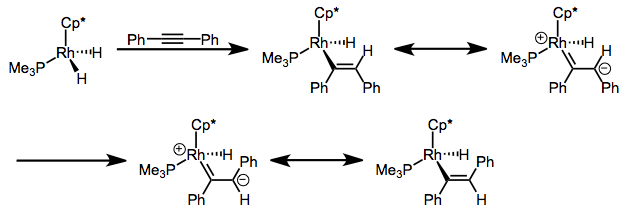
El ligando Cp * fuertemente donador apoya la legitimidad de la forma de resonancia zwitteriónica, ¡y sugiere que el enlace C=C puede ser más débil de lo que parece al principio!
Los polienos pueden participar en la inserción migratoria, y las inserciones de polienos suelen ser bastante favorecidas porque resultan complejos estabilizados\(\pi\) -alilo. En un caso alucinante, ¡un areno coordinado se inserta en un enlace M—Me de una manera syn!
¿Alguna vez se ha detenido a considerar que la adición de metillitio a un aldehído es una inserción formal del grupo carbonilo en el enlace Li-Me? ¡Es verdad! Podemos pensar en éstas como reacciones (muy) tempranas de “inserción” de metales. A pesar de este precedente, las reacciones de inserción migratoria de carbonilos e iminas en enlaces de hidruro metálico tardío y alquilo son sorprendentemente difíciles de conseguir. El rodio es el metal más famoso que puede hacer que esto suceda; el rodio se ha utilizado en complejos para la arilación y la vinilación, por ejemplo. La inserción de X=C en el enlace M—R suele ir seguida de la eliminación de\(\beta\) -hidruro, lo que tiene el efecto ingenioso de reemplazar H en aldehídos y aldiminas con un grupo arilo o vinilo.


